автордың кітабын онлайн тегін оқу Хирурги, святые и психопаты. Остросюжетная история медицины
Стивен Уэстаби
Хирурги, святые и психопаты. Остросюжетная история медицины
Surgeons, Saints and Psychopaths:
The Epic History of Heart Surger
by Stephen Westaby
Copyright © Stephen Westaby 2023
© Ляшенко О. А., перевод на русский язык, 2023
© ООО «Издательство «Эксмо», 2024
Предисловие
В 1896 году доктор Стивен Пэджет[2] в своем великолепном учебнике «Surgery of the Chest» писал: «Операции на сердце уже достигли пределов, установленных природой. Ни один новый метод и ни одно открытие не смогут преодолеть естественные трудности, сопровождающие повреждение сердца».
К тому моменту, когда я полвека спустя увидел этот мир – а точнее, закоулки северного сталелитейного городка, – почти ничего не изменилось. Кардиохирургии для практических целей все еще не существовало.
Тем солнечным июльским утром в родовой палате моя дорогая мама взяла меня на руки – розового, теплого, ревущего во всю мощь только что раскрывшихся легких. Я родился крепким четырехкилограммовым младенцем, генетически запрограммированным на выживание и процветание. Однако несчастной малышке в соседней кроватке была уготована иная судьба.
Единственный плюс, у ее матери не случилось разрыва промежности в процессе родов – девочка была крошечной.
Она появилась на свет с хныканьем, а не ревом. Все новорожденные синие, но, когда они плачут и сопротивляются давлению родовых путей, их легкие впервые втягивают воздух и раскрываются. Вдыхаемый кислород окрашивает эритроциты в ярко-красный цвет, и тельце ребенка розовеет. Только не в этот раз.
Опытная акушерка сразу поняла, в чем проблема.
– У вас прекрасная малышка, – пробормотала она, – но мне нужно позвать врача.
Минуты ожидания тянулись мучительно долго. Врач наконец пришел, правда, не с радостной вестью.
– Мне жаль, у вас «синий» ребенок, – констатировал он, осторожно передав младенца матери. Термин «синий младенец» ничего не говорил бедной женщине. Да и откуда ей было знать?
– Что это значит? – спросила она, подняв на врача испуганные глаза. В это время моя счастливая мать всеми силами старалась отгородиться от их диалога.
– Это значит, что-то мешает крови поступать в легкие и, вероятно, в сердце у ребенка есть отверстие, – сухо пояснил он, пока акушерка с отрешенным видом сверлила взглядом потолок.
Женщина видела, как я сосу материнскую грудь, и из ее сосков тоже выделялось молозиво. Естественно, она попыталась покормить свою синюшно-фиолетовую малютку, но безрезультатно. Девочка захныкала, срыгнула, подавилась молоком, а ее кожа приобрела зловещий сероватый оттенок. Через несколько часов, когда солнце опустилось за доменные печи, малышка обмякла в руках матери и затихла. Акушерка унесла ее в коробке для обуви. Женщина разрыдалась. Моя мать тоже. Мужчина не успел поприветствовать своего первенца. Он работал в вечернюю смену на сталелитейном заводе. Тогда отгул в день рождения ребенка не предоставляли. На дворе был 1948 год, год создания Национальной службы здравоохранения Великобритании.
Как я узнал об этом? Каждый год, в день моего рождения, выпадавший на школьные каникулы, мы с мамой покупали цветы и ехали на автобусе через весь город, чтобы возложить их на порог дома той несчастной женщины.
Она наблюдала, как я расту, а своих детей так и не родила. Первая попытка оказалась для нее слишком травматичной.
Когда я был ребенком, мы жили в муниципальном доме прямо через дорогу от бабушки и дедушки по материнской линии. Я проводил с ними немало времени, потому что мама работала кассиром в сберегательном банке на главной улице города.
Дедушка, увидев, что я амбидекстр, научил меня рисовать карандашами и красками. Во время Второй мировой войны дед был уполномоченным по гражданской обороне и, подобно остальным мужчинам того времени, много курил и трудился в удушающей дымке литейных цехов. В восемь лет я впервые стал свидетелем его боли в груди. Мы выгуливали собаку в парке. Он придумал оправдание, чтобы остановиться и стереть пот со лба. Когда он наклонялся, ему становилось хуже – сейчас я понимаю, что это были типичные симптомы ишемической болезни, недостаточного кровоснабжения сердечной мышцы.
Однажды все изменилось. Дед вдруг схватился за грудь, ослабел и упал на колени. В возрасте 59 лет у него произошел сердечный приступ. Оторвавшаяся атеросклеротическая бляшка закупорила жизненно важную коронарную артерию, и, пока я с трудом пытался довести деда до дома, миллиарды мышечных клеток его сердца гибли.
Семейный врач, приехавший к нам на черном автомобиле «Остин-Хили», прописал деду строгий постельный режим. В течение последующих нескольких недель большой участок мертвого миокарда заместила рубцовая фиброзная ткань, которая не сокращалась, а только растягивалась. Левый желудочек плохо расслаблялся и сокращался, поэтому деда мучили одышка и отеки ног и накопление жидкости в животе. Таблетки не помогали. В те годы в продаже был лишь дигоксин[3], полученный из наперстянки, а эффективных диуретиков еще не существовало. Вскоре дедушкину кровать перенесли на первый этаж и поставили перед камином, но из-за одышки дед не мог лежать на спине. Ему было комфортнее проводить ночи сидя в кресле.
Чем еще мы могли ему помочь? Нам говорили, что ничем. Жизнь с сердечной недостаточностью стала для дедушки невыносимой, а нам оставалось лишь наблюдать, как он угасает у нас на глазах, что было мучительно больно. Вскоре, как это всегда бывает в терминальной стадии сердечной недостаточности, у него развилась почечная недостаточность.
Возвращаясь из школы холодным декабрьским днем, я снова увидел «Остин-Хили» у нашего дома. Сквозь неплотно задернутые шторы я смог заглянуть внутрь. По обеим сторонам кровати сидели убитые горем мама и бабушка, сжимавшие ледяные, влажные руки дедушки. Его посеревшее лицо исказила гримаса боли, а из его рта и ноздрей шла пена с примесью крови. Врач вводил деду большую дозу морфия с твердым намерением положить конец страданиям больного. Ему это удалось. Добрый поступок неравнодушного врача для умирающего пациента в эпоху, когда больше ничего нельзя было сделать.
Мне нелегко было забыть эту сцену, произошедшую за несколько дней до Рождества. Честно говоря, я хранил ее в своей памяти на протяжении всей моей карьеры. Если бы вы могли помочь человеку в подобной ситуации, неужели бы вы отказались?
В те времена сердечную недостаточность вызывали не только ишемическая болезнь и врожденные пороки сердца. Жизнь многих здоровых молодых людей разрушила банальная стрептококковая ангина, за которой последовала острая ревматическая лихорадка[4]. В результате иммунной реакции здоровые клапаны сердца сужались или начинали протекать. Сифилис, широко распространившийся во Вторую мировую войну, тоже приводил к заболеванию сердечных клапанов и аневризмам аорты[5]. Ни одно из этих заболеваний не реагировало на препараты – в итоге чтобы найти решение, отчаявшиеся и скептически настроенные врачи обратились к хирургам.
Чтобы отвлечь меня от трагичной смерти дедушки, родители купили в дом первый телевизор. У него был черно-белый экран шириной чуть более 20 см, но всего один документальный фильм, который я на нем посмотрел, навсегда изменил мою жизнь. В феврале 1958 года в передаче «Ваша жизнь в их руках»[6] показали одну из первых операций на сердце, проведенную в Хаммерсмитской больнице. Хирурги вперили взгляды в распахнутую грудную клетку, а камера на мгновение запечатлела больное сердце, сокращающееся в фиброзном мешке. Хирурги собирались взять под контроль кровообращение пациента с помощью аппарата искусственного кровообращения (АИК), и, помню, я подумал: «Ну почему это нельзя было сделать много лет назад?» Для того времени это были весьма шокирующие кадры: кардиохирургия по большей части оставалась недоступной для широкой публики. Разумеется, цель заключалась в повышении медицинской грамотности, но в определенных кругах такие методы народного просвещения, мягко говоря, не одобряли. Настолько, что на следующий день в парламенте разгорелись бурные дебаты.
Хансард[7], 28 февраля 1958 года. Сэр Йен Кларк Хатчинсон выступил против генерал-почтмейстера мистера Марплса с заявлением: «Многие врачи сочли, что отвратительная программа “Ваша жизнь в их руках” негативно влияет на зрителей. Не могли бы вы любезно попросить ВВС воздержаться от показа подобных передач?»
В ответ генерал-почтмейстер проинформировал палату, что администрация канала ВВС заранее консультировалась с Королевским колледжем хирургов, Королевским колледжем врачей и Колледжем врачей общей практики и получила их одобрение.
Член парламента Генри Моррисон поддержал столь красочную презентацию: «Знает ли уважаемый господин, что я смотрел эту программу вчера вечером? В ней показывали операцию на сердце, и я подумал, что все было сделано очень осторожно и уважительно. Это была образовательная передача, отснятая в сотрудничестве с администрацией больницы. Могу ли я попросить генерал-почтмейстера выйти из-под чрезмерного влияния своего уважаемого друга?»
Между тем под влияние попал я. Именно тогда, в возрасте девяти лет, я принял решение стать кардиохирургом.
Спустя двадцать лет я проводил операции на сердце с той же бригадой в Хаммерсмитской больнице, а еще через двадцать – сам стал героем программы «Ваша жизнь в их руках». В Королевской больнице Бромптона я имплантировал совершенно новый тип искусственного сердца пациенту с сердечной недостаточностью, имевшему много общего с моим несчастным дедом.
Как говорится, что посеешь, то и пожнешь. Думаю, дед гордился бы мной.
Почему же именно операции на сердце были такими сложными и противоречивыми?
Давайте начнем с некоторых фактов о великолепной машине, с которой я работал на протяжении всей своей карьеры. Сердце выполняет поразительно простую функцию: оно перекачивает кровь. Но стоит насосу выйти из строя, жизнь человека превращается в настоящий кошмар. Давящая боль в груди, сильная одышка, задержка жидкости и хроническая усталость – последствия болезней сердца, поражающих все возрастные группы. Здоровое сердце взрослого человека весит около 300 граммов. В школе, на уроках биологии, нам рассказывали, что оно состоит из четырех частей: двух тонкостенных собирающих камер (правого и левого предсердий), а также двух толстостенных насосных камер (правого и левого желудочков).
Вот и все, что я знал о сердце.
Это не совсем верно, потому что предсердия тоже перекачивают кровь. Люди с фибрилляцией предсердий – распространенным нарушением сердечного ритма – не только имеют повышенный риск инсульта из-за турбулентности и тромбов, но и ощущают упадок сил, поскольку предсердия утрачивают способность сокращаться синхронно. На иллюстрациях в учебниках камеры обычно изображают так, будто они находятся бок о бок, что тоже не соответствует действительности. Я предлагаю другую аналогию – представить сердце как дом с двумя спальнями сверху и кухней и гостиной внизу. Почему? Потому что желудочки очень отличаются друг от друга. Они скорее не левое и правое, а переднее и заднее.
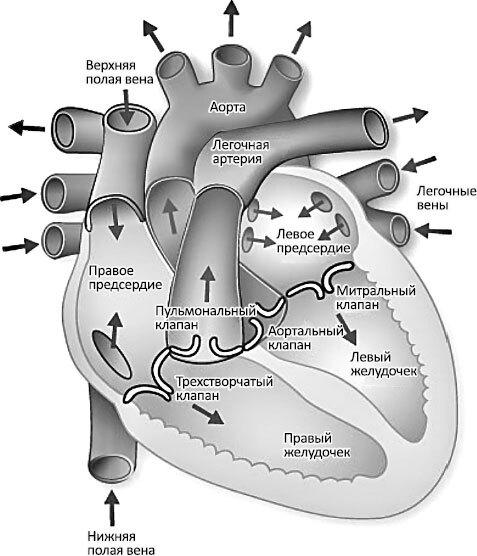
Предисловие. Рисунок 1. Строение сердца.
Более толстый и мощный левый желудочек имеет конусообразную форму и состоит из круговых пучков мышечных волокон, которые энергично сокращают и вращают камеру. В нем около пяти миллиардов клеток, и более половины из них составляют кардиомиоциты – сократительные клетки. Кардиомиоциты тесно связаны друг с другом межклеточными контактами, благодаря чему сердце словно опутано тончайшей электрической сетью. Внутри кардиомиоцита находятся тщательно организованные молекулы белка, которые скользят друг по другу, вызывая укорочение и сокращение мышц.
Оба желудочка должны генерировать мощную силу, чтобы быстро проталкивать кровь по циркуляторной системе артерий, вен и капилляров. Сократившись, они расслабляются, и после каждого сокращения камеры вновь заполняются кровью. В состоянии покоя сердце совершает около 70 ударов в минуту, но при интенсивных физических нагрузках этот показатель может повыситься до 180. В ответ на нервную и гормональную стимуляцию к 75 триллионам клеток нашего тела ежеминутно поступает от 5 до 20 литров крови. Если вдуматься, цифры поражают. Ежедневно 100 тысяч ударов распределяют 7600 литров крови. За год сердце совершает 35 миллионов ударов, а за жизнь средней продолжительности – 2,5 миллиарда. В сутки эритроцит преодолевает по сосудистой системе около 20 000 км, что в четыре раза превышает расстояние от западной до восточной границы США.
Несмотря на миллиарды ударов, совершенных за жизнь человека, половина кардиомиоцитов, присутствовавших при его рождении, сохранятся и к моменту его смерти. Они успеют израсходовать достаточно энергии, чтобы на грузовике доехать до Луны и обратно.
Только 1 % кардиомиоцитов ежегодно обновляется в младших возрастных группах. Сравните эти трудолюбивые «вечные» клетки с теми, что выстилают кишечник и живут меньше недели.
Мускульное сокращение и расслабление не так просты, как кажется на первый взгляд. Когда левый желудочек сокращается во время систолы, полость одновременно сужается и укорачивается, чтобы вытолкнуть кровь. Через выпускной клапан она попадает в аорту и проходит по всему телу. Поразительно, но за жизнь средней продолжительности по организму человека проходит около 158 987 295 литров крови. Этого достаточно, чтобы заполнить более трех супертанкеров. Во время расслабления, или диастолы, камера одновременно расширяется и удлиняется. Создаваемое отрицательное давление втягивает кровь из левого предсердия через митральный клапан, получивший свое название из-за сходства с митрой священнослужителя. Хотя это, на мой взгляд, вполне уместная метафора, некоторые предпочитают сравнивать его с женским поясом с подвязками.
Правый желудочек работает совсем по-другому. При меньшем давлении и сопротивлении он перекачивает в легкие тот же объем крови через пульмональный клапан. Правый желудочек более тонкостенный. Он имеет серповидную форму и обернут вокруг передней части левого желудочка. Стенка левого желудочка – межжелудочковая перегородка – разделяет сердца на левый и правый желудочек, поэтому она является стенкой и того, и того желудочка. Правый желудочек похож на полумесяц и как бы обнимает левый сбоку. Таким образом, функция двух этих полостей во многом зависит друг от друга и целостности их электропроводящей системы.
Сердечный цикл – это настоящее аргентинское танго, с одним отличием: каждый тщательно синхронизированный удар занимает меньше секунды, и танец продолжается всю жизнь.
Искусно скоординированный ритм оркестрируется скоплениями пейсмейкерных клеток, или водителями ритма, которые условно делятся на 4 порядка: водитель первого порядка – синоатриальный узел в стенке правого предсердия, водитель второго порядка – атриовентрикулярный узел, расположенный между предсердиями и желудочками, а также водители тертьего и четвертого порядка – ножки пучка Гиса и волокна Пуркинье соотвественно. Сигналы передаются с помощью непрерывного электрического тока, который проходит через внешние оболочки пейсмейкерных клеток. Этим последние отличаются от обычных кардиомиоцитов – они «бьются» только при наличии стимула. Электрические токи лежат в основе электрокардиографии (ЭКГ), с помощью которой можно оценить многие аспекты здоровья сердца, включая толщину стенок, историю сердечных приступов и заболевания сердечной мышцы.
Больные сердца́ не любят, когда их трогают, отсюда и трудности с проведением кардиохирургических операций. Сердце возмущается, нарушает свои синхронизированные движения, совершает дополнительные, или эктопические удары, переходит на ускоренный ритм или даже начинает бесконтрольно извиваться (это называется фибрилляцией желудочков). Без экстренного электрического шока фибрилляция приводит к смерти человека, а дефибрилляторы стали применяться только в 1950-х годах. В случае остановки сердца кровь перестает циркулировать по 96 500 км кровеносных сосудов, мгновенно лишая ткани кислорода и жизненно важных питательных веществ. Быстро накапливаются токсичные метаболиты, такие как углекислый газ и молочная кислота, и со временем клетки разрушаются. Игра окончена.
Сердечная мышца поразительно хорошо адаптируется. Когда мы интенсивно тренируем руки и ноги, скелетные мышцы устают и деревенеют из-за скопления молочной кислоты. О кардиомиоцитах нельзя сказать то же самое. Эти клетки обладают невероятной способностью сокращаться по 70–150 раз в минуту на протяжении всей жизни, беспрестанно. Лишь нарушение кровоснабжения или сердечное заболевание могут изменить установленный сценарий. Само сердце, благодаря двум крошечным коронарным артериям, получает лишь 5 % от всей протекающей по телу крови. Сравните это с 20 %, получаемыми головным мозгом, – комком нервных клеток, неподвижно лежащем в черепной коробке. С возрастом коронарные артерии могут закупориваться холестериновыми бляшками, которые накапливают кальций. Неправильное питание и курение повышают риск развития атеросклероза. Если коронарные артерии закупориваются, во время физических нагрузок усиления кровотока не происходит, в результате чего возникает ишемия, и из-за недостатка кислорода образуется молочная кислота. Это ведет к давящей боли в груди, известной как стенокардия. В состоянии покая боль стихает. По крайней мере, мы на это надеемся.
Даже здоровый орган может кардинально измениться.
В результате регулярных интенсивных тренировок сердце спортсмена становится на 20–30 % толще, но не за счет роста числа кардиомиоцитов, а за счет увеличения их в размере.
Полость левого желудочка может увеличиться в объеме в два раза при циркуляторной перегрузке во время беременности, а в течение десяти дней после родов сократиться на целых 40 %. Все это происходит в ответ на механический стресс и адаптацию формы и размера кардиомиоцитов, а не на рост числа клеток.
Напротив, сердечный приступ обернется катастрофой, если в течение часа пациент не пройдет лечение в катетеризационной лаборатории. Когда трудолюбивые мышечные клетки резко лишаются крови и кислорода из-за перекрытой коронарной артерии, приходит беда. Отдельные кардиомиоциты накапливают токсичные вещества, из-за которых многие разрушаются, а их содержимое вытекает из разорванных оболочек. Это приводит к сильной боли и смерти целых двух миллиардов клеток. Небольшая часть выживших кардиомиоцитов, возможно, начнет делиться, но этого все равно слишком мало для устранения повреждений. Одновременно фибробласты, составляющие структурный каркас нашего сердца, тоже начнут стремительно делиться, образуя рубцовую ткань. Это позволяет предотвратить разрыв сердца, но далеко не всегда – в таких случаях пациент неожиданно умирает через несколько дней. Внезапная фибрилляция желудочков, вызванная потерей стабильности проводящей системы сердца, – наиболее распространенная причина смерти после сердечного приступа.
Можно ли предотвратить фатальную последовательность событий? Да, но только с помощью умелых интервенционных кардиологов. Через аорту они введут катетер в закупоренную артерию, чтобы установить стент и расширить просвет сосуда. Умирающая сердечная мышца снова начинает получать кровь и оказывается спасена, но все зависит от быстрого доступа к кардиологической клинике и наличия свободного специалиста. Не у всех есть такая возможность, особенно в рамках Национальной службы здравоохранения. Соотношение миокарда и рубцовой ткани после сердечного приступа напрямую указывает на качество оказанной медицинской помощи.
Во второй половине ХХ века для этих проблем было найдено постоянно совершенствующееся хирургическое решение.
К сожалению, фиброзная ткань нестабильна. Находясь под постоянным давлением в полости левого желудочка, она растягивается. Поврежденная камера расширяется, и, согласно законам физики, с увеличением камеры растет и давление на ее стенку. Затем митральный клапан начинает протекать, и давление в левом предсердии и легочных венах возрастает. Появляется одышка. По мере развития сердечной недостаточности страдают и другие органы. Ухудшается работа почек, развивается асцит (водянка). Ноги и живот со временем наполняются жидкостью, а печень растягивается из-за повышения давления в венах, отводящих кровь от нижней части тела. Бесконечные страдания, свидетелем которых довелось стать и мне.
Сколько живут другие органы после остановки сердца? Важнейший вопрос, краеугольный камень трансплантологии. Смерть наступает постепенно из-за метаболического хаоса, вызыванного прекращением поступления кислорода и глюкозы к тканям. Известно, что органы грудной клетки – сердце и легкие – остаются жизнеспособными вне тела в течение 4–6 часов. Печень живет до 12 часов, а почки – до 36. Естественно, ткани с более низкой скоростью обмена веществ, например кожа, сухожилия, сердечные клапаны и роговица, сохраняют жизнеспособность гораздо дольше. А что насчет мозга?
Хотя на мозг приходится всего лишь 2 % от общей массы тела, он потребляет около 20 % кислорода из крови. Нервным клеткам также требуется большой запас глюкозы для удовлетворения их энергетических потребностей. В условиях кислородного голодания, или гипоксии, организм человека быстро утрачивает способность метаболизировать глюкозу, а в результате чего – и нервную функцию. Поэтому через 10–15 секунд после остановки кровообращения человек теряет сознание.
Через 4 минуты, или всего 240 пропущенных ударов сердца спустя, начинается повреждение головного мозга, которые через 10 минут после остановки кровообращения становятся необратимыми. Дыхание прекращается через полторы минуты после остановки кровообращения.
Для возникновения гипоксии не нужна полная остановка сердца. К кислородному голоданию способны привести серьезные нарушения сердечного ритма и очень низкое артериальное давление.
Не менее любопытно то, что происходит в сознании человека во время остановки сердца. Электроэнцефалография (ЭЭГ) – мозговой эквивалент электрокардиографии (ЭКГ). Американские врачи проводили ЭЭГ 87-летнему пациенту, которому после травмы головы требовалась операция на мозге, чтобы устранить сгусток крови. К несчастью, у мужчины случился сердечный приступ, и он скончался прямо во время исследования, но специалисты продолжали наблюдать за мозгом пациента в течение пятнадцати минут после его смерти. Результаты изучения электрической активности его мозга оказались впечатляющими. Сосредоточившись на тридцати секундах до и после остановки сердца, врачи заметили те же изменения в электрических волнах, что наблюдаются у людей, когда они спят, видят флешбэки или обрабатывают воспоминания. Мозговые волны, записанные во время сердечного приступа и сразу после него, позволяют предположить, что у пациента в голове пронеслись воспоминания о жизни, аналогичные тем, что сопровождают околосмертные переживания.
Описывая свои наблюдения в журнале Frontiers in Aging Neuroscience, один из авторов статьи пришел к следующему выводу: «Человеческий мозг, скорее всего, обладает способностью генерировать координированную активность в процессе умирания. И действительно, это предположение подтверждают аналогичные наблюдения, сделанные в ходе контролируемых экспериментов на крысах».
Его слова резонируют со множеством историй, услышанных мной от пациентов на более поздних этапах моей карьеры.
Мозг и сердце – неразлучные товарищи, но смерть может наступать не так быстро, как мы раньше думали.
Согласно прежним представлениям, клетки мозга умирают в течение 5–10 минут, однако современные данные свидетельствуют об обратном: оставленные в покое нейроны умирают на протяжении многих часов или даже нескольких дней после остановки сердца и смерти человека. Парадоксально, но именно восстановление притока кислорода к тканям во время реанимационных мероприятий приводит к гораздо более быстрой гибели клеток. Врачи называют это реперфузионным повреждением. Чем дольше у человека длится остановка сердца, тем сильнее будут повреждены клетки. Человек, в мозг которого кровь не поступала менее пяти минут, имеет гораздо больше шансов на спасение и восстановление, чем человек, испытавший более долгую гипоксию. Вообще, это вполне логично и связано со свободными радикалами[8].
Будучи младшим врачом в крупной клинической больнице Лондона, я всегда добровольно дежурил в бригаде, работавшей с пациентами с остановкой сердца. Днем и ночью дежурило по три человека, и большинство членов нашей бригады были ветеранами регби. Два терапевта, потому что в дневное время хирурги обычно заняты в операционных, и стажер-анестезиолог, задача которого состояла в том, чтобы вводить пациентам в дыхательные пути эндотрахеальную трубку и нагнетать кислород в легкие. Спортивная подготовка играла ключевую роль в нашей работе. Когда поступал экстренный вызов, мы мчались по коридорам, взлетали по лестницам и со всех ног бежали по отделению. Время решало все. С каждой секундой лишенный крови мозг умирал, и тогда мы еще ничего не знали о свободных радикалах.
Представьте себе медсестру, которая сидит на животе лежащего на койке пациента и, скрестив ладони на груди, совершает ритмичные, но робкие компрессии.
Когда Мрачный Жнец ждет у изголовья кровати, робость неуместна. Итак, регбийная команда жестко приступает к делу. Хрусть-хрусть-хрусть-хрусть.
При неистовых компрессиях грудина приближается к грудному отделу позвоночника, зажимая недвижимое сердце. Даже энергичный непрямой массаж сердца позволяет достичь лишь 20 % эффективности нормальной его работы. Одновременно с этим принудительное движение грудной клетки приводит сначала к втягиванию, а затем к выпусканию воздуха, поэтому в искусственном дыхании изо рта в рот нет необходимости.
Реанимационная медсестра принесла мне шприц с адреналином и длинную иглу для люмбальной пункции. Приостановив компрессии, я ввел иглу через грудную стенку, целясь в полость левого желудочка. Введя мощный стимулятор, я продолжил вжимать грудную клетку, чтобы доставить препарат в сосуды организма для подъема артериального давления и увеличения потока крови в мозг и сердце. Это вызывало сердечный ритм даже у тех, у кого линия ЭКГ была абсолютно ровной. Когда этого не происходило, асистолия сменялась на фибрилляцию желудочков – бурный электрический хаос, который более восприимчив к разряду дефибриллятора. Разряд! Мышцы пациента резко сократились, из-за чего спина выгнулась, а тело приподнялось. К тому моменту анестезиолог успевал установить катетер и ввести дозу бикарбоната натрия для нейтрализации кислоты в крови.
Вообще, нам редко встречались сердца, которые не удавалось перезапустить. Часто сердце снова начинало фибриллировать из отвращения к столь жестокому обращению, но мы пускали еще один разряд. Обычно к тому моменту, как пациент опять оказывался на матрасе, его сердечный ритм более-менее приходил в норму. Тут уставший орган нужно было оставить в покое, чтобы дать ему собраться с силами.
Мы гордились восстановлением кровообращения и воскрешением мертвых, но сами пациенты платили за второй шанс высокую цену. Многочисленными сломанными и смещенными ребрами. Были ли наши усилия своевременными, и удалось ли нам предотвратить катастрофическое повреждение головного мозга в условиях гипоксии? Такой результат приговорил бы живое тело к стойкому вегетативному состоянию. Статистика красноречива: только один из четырех пациентов выживал, а у большинства имелись повреждения мозга. Однако некоторые восстанавливались, что все-таки оправдывало наши усилия. Воспринимала ли наша спортивная реанимационная бригада лежащее перед нами тело как живого человека? Это не входило в план. Кто-то нажимал на сигнал тревоги, и мы на него отвечали. Мы проводили все мероприятия, но после, как правило, больше не видели пациента. Его отвозили в отделение интенсивной терапии, а мы расходились по своим углам. У нас не было посттравматического стресса, о котором пишут в современных статьях. Мы просто спасали следующего пациента.
Возможно, по своей природе хирурги другие. Конечно, терапевты считали нас неполноценным видом.
Я остался работать с больными сердцами, и многие мои товарищи-регбисты из нашей реанимационной бригады тоже стали хирургами. Тут возникает резонный вопрос: если мозг серьезно повреждается в течение всего нескольких минут после остановки кровообращения, как можно проводить сложные операции на больном и раздраженном сердце, которое заполнено кровью под давлением и находится в непрерывном движении? Решение было найдено, но оно потребовало времени… и блестящих умов.
Большим толчком к развитию кардиохирургии послужила Вторая мировая война с ее проникающими ранениями грудной клетки и совместной работой британских и американских хирургов в Европе, которые извлекали пули и осколки. Обмен идеями между союзниками вдохновил решительно настроенных молодых мужчин вернуться домой и заняться поиском более эффективных методов хирургического лечения тяжелых пороков сердца. Дальнейшие эпохальные события шокировали и профессионалов, и обывателей. Мрачный Жнец сидел на плече каждого хирурга, а главных героев этой истории окрестили безрассудными психопатами. Хотя статистику скрывали от СМИ, все знали, что под скальпелем умирало больше, чем выживало.
Парадоксальным образом я и случайно, и намеренно стал сначала учеником, а затем и коллегой многих пионеров кардиохирургии по обе стороны Атлантики. Поскольку их воспоминания показались мне крайне захватывающими, я решил написать учебник на эту тему. Книга «Вехи кардиохирургии» была издана в 1997 году, ровно через 100 лет после первого успешного хирургического лечения ножевого ранения сердца в Германии. Однако ножевые ранения оказались пределом возможностей кардиохирургии на следующие полвека, да и медицинское лечение оставалось таким же примитивным. Сердечные заболевания становились смертным приговором. В учебнике по медицине 1913 года знаменитый оксфордский профессор Уильям Ослер резюмировал информацию о врожденных пороках сердца всего на четырех страницах. Он дал лишь одну рекомендацию по лечению: «Ребенка нужно тепло одевать и оберегать от любых обстоятельств, способных привести к бронхиту. При приступе ургентного[9] диспноэ (одышки) с синюшностью (посинение лица) следует пустить кровь. Солевые слабительные тоже полезны. Наперстянку следует использовать с осторожностью: иногда она действенна на более поздних стадиях».
За свою 50-летнюю карьеру я прооперировал бесчисленное множество больных сердец – в одном только Оксфорде более десяти тысяч. Одни были крошечными и деформированными, другие огромными после месяцев тяжелой сердечной недостаточности. Сердца были быстрыми и медленными, жирными и тощими.
Каждое сердце уникально, но его непрерывное биение поистине впечатляет. Кишечник просто извивается, легкие наполняются и сдуваются, но сердце – танцует. Для меня это как «Лебединое озеро» в груди, только в гораздо более быстром темпе.
Мне выпала честь ремонтировать сердца и улучшать жизнь пациентов с помощью техник, разработанных при моей жизни.
Мне кажется, рассказ о том, как хирурги учились оперировать сердце, – одна из величайших историй в мире. Я считаю, что в наше мрачное время, когда «проснувшийся» самоанализ подвергает сомнению все, а медицина вынуждена занимать оборонительную позицию и доказывать свою правоту, эта история вызовет интерес у широкой публики. Моя книга о кардиохирургии похожа на триллер, но с гораздо, гораздо бо́льшим числом трупов.
Острая ревматическая лихорадка – системное заболевание соединительной ткани с преимущественной локализацией поражений в сердечно-сосудистой системе (кардит, клапанные пороки сердца), развитием суставного (артрит), кожного (ревматические узелки, аннулярная эритема) и неврологического (хорея) синдромов, возникающее на фоне иммунного ответа организма на стрептококк группы А. – Прим. науч. ред.
Дигоксин – кардиотоническое и антиаритмическое лекарственное средство, сердечный гликозид. – Прим. науч. ред.
«Ваша жизнь в их руках» (Your Life in Their Hands) – документальный сериал телеканала BBC на тему хирургии, в котором хирургическая практика рассматривалась как с точки зрения хирургов, так и пациентов. – Прим. науч. ред.
Аневризма аорты – расширение участка аорты, обусловленное патологическим изменением соединительнотканных структур ее стенок вследствие атеросклеротического процесса, воспалительного поражения, врожденной неполноценности или механических повреждений. – Прим. науч. ред.
Свободные радикалы – частицы, содержащие один или несколько неспаренных электронов на внешней электронной оболочке. Они провоцируют процесс окисления, атакуя обычные клетки и пытаясь отнять у них один электрон. Затронутая клетка сама становится свободным радикалом, распространяя окислительную реакцию на прилегающие клетки, или разрушается. – Прим. науч. ред.
Хансард – официальный отчет о заседаниях парламента в англоязычных странах. – Прим. науч. ред.
Ургентное состояние – угрожающее жизни состояние, требующее немедленной медицинской помощи. – Прим. науч. ред.
Стивен Пэджет (1855–1926) – британский хирург, основоположник теории метастазирования рака (теория «семени и почвы»). – Прим. науч. ред.
Марк Митчелл Равич (1910–1989) – американский хирург, пионер торакальной хирургии. – Прим. науч. ред.
Несбыточная мечта
Нет ничего невозможного. В самом этом слове заключена возможность!
Одри Хепберн
Когда посетители, не являющиеся медицинскими работниками, входят в операционную и осторожно заглядывают за хирургические простыни, их реакция всегда одинаковая. Они не могут оторвать взгляд от сердца, бьющегося в своей блестящей фиброзной оболочке между металлическими зеркалами торакального расширителя. Большинство замирают, загипнотизированные его красотой и ритмичным движением. Цвет сокращающейся мышцы и маслянистого жира на фоне испачканной кровью голубой простыни. Некоторые интересуются, где какая камера, и любуются крошечными коронарными артериями, змеящимися по поверхности органа. Другие так далеко не заходят. Они падают в обморок прямо у ног анестезиолога или, почувствовав головокружение, извиняются и спешно покидают операционную, испугавшись видов и звуков незнакомой обстановки. Конечно, многие из тех, кто все же решается посмотреть, отворачиваются, как только начинается кровотечение.
Через подобный опыт прошло большинство наших стажеров.
Сколько бы они ни занимались общей хирургией, перспектива наложить первый стежок на стенку напряженной, пульсирующей аорты или дрожащее ушко правого предсердия оказывается достаточной, чтобы обмочиться.
А мысль о том, чтобы рассечь их и контролировать кровотечение, и вовсе наводит настоящий ужас. Это чистая правда. Кардиохирургия всегда была такой. Чтобы заниматься ей, нужно обладать определенным складом характера, а те, кто делал первые робкие шаги в этой сфере, мало взаимодействовали с сердцем. В основном это были хирурги общего профиля, но неизменно альфа-самцы. Смелые люди, работавшие в тяжелых условиях, когда операция была единственным шансом на спасение. Наверное, их можно назвать безрассудными в какой-то степени, поскольку с хирургической точки зрения сердце тогда считалось неприкасаемым, и многочисленные неудачи лишь подкрепляли это убеждение.
Сердце – труднодоступный орган, так как он находится между жесткой грудиной и позвоночником, в капсуле из легких и ребер. Целостность грудной стенки имеет большое значение. При вдохе в грудной полости создается отрицательное давление, и воздух засасывается в легкие. Затем ребра сжимаются, выталкивая втянутый в легкие воздух с его побочным продуктом – углекислым газом. Если грудную стенку повредить ножом, пулей или скальпелем, на вдохе воздух попадет в новообразованное отверстие, и произойдет коллапс легкого. Это называется травматическим пневмотораксом: в результате его пациент начинает задыхаться, испытывает респираторный дистресс-синдром[10] и утрачивает способность сотрудничать с врачом. Кроме того, на заре торакальной хирургии анестетиков не существовало. Чтобы отключиться, пациенту нужно было либо потерять много крови, либо влить в себя внушительную дозу алкоголя (я с теплом вспоминаю подобные ситуации со времен учебы в медицинской школе).
Добраться к сердцу хирургу проще всего через грудину: нужно сдвинуть остатки вилочковой железы и напрямую вскрыть перикард внизу. Так можно избежать проникновения в плевральную полость и контакта с легкими. В 1897 году Герберт Мильтон из больницы Каср-эль-Айни в Каире отправил в журнал Lancet статью с описанием разреза грудины.
Мильтон отметил: «Хирургия сердца находится еще в зачаточном состоянии, но не нужно обладать бурной фантазией, чтобы представить себе пластические операции на пораженных клапанах».
В идеале для стернотомии (рассечения грудины) требовалась высокоскоростная осциллирующая пила, но в те годы ее не существовало, поэтому работу приходилось выполнять острым долотом и молотком. Несомненно, более простым вариантом был разрез грудной стенки с левой стороны с последующим широким разведением ребер. Несмотря на изобретение анестезии в 1846 году, подобные операции все еще было сложно себе представить из-за отсуствия системы искуственной вентиляции легких. При рассечении грудины происходил коллапс легкого и пациенты задыхались.
Легендарный военный хирург Наполеона, барон Доминик Ларрей, привык причинять пациентам боль.
За один день Бородинского сражения в 1812 году он провел двести ампутаций конечностей пьяным, но бодрствующим раненым солдатам и не испугался попробовать вскрыть грудную клетку без анестезии.
Один из его пациентов, тридцатилетний пехотинец по имени Бернар Сент-Онь, попытался ударить себя ножом в сердце, когда его обвинили в преступлении, которое он не совершал. Нож разорвал левое легкое и перикард, но солдат выжил, поскольку лезвие не задело камеру сердца. Однако у мужчины произошел коллапс легкого, и из-за инфекции грудная полость оказалась заполнена гноем.
Из-за усиливающихся лихорадки и боли Ларрей провел сначала растирание камфорным маслом, а затем вскрыл грудную стенку и пустил кровь. Эти действия не возымели большого эффекта, поскольку гной к тому времени уже заполнил перикард и начал сдавливать сердце. Состояние Сент-Оня ухудшалось: его ноги и живот сильно отекли, поскольку давление на правое предсердие затруднило ток венозной крови. Другими словами, у него произошла тампонада сердца[11]. Пациенты могут выжить при проникающих ранениях правого предсердия или желудочка, если давление вокруг сердца совпадает с давлением внутри камер и кровотечение прекращается. Поэтому мы настаиваем на том, чтобы не переливать кровь таким пациентам до операции – гемотрансфузия только усилит кровотечение.
Диагностировав сдавление сердца, Ларрей смело вскрыл грудную клетку пациента слева, между пятым и шестым ребрами. К счастью, из-за гноя, скопившегося в грудной полости, легкое прилипло к грудной стенке, поэтому резкого коллапса с его ужасающим воздействием на бодрствующего пациента не произошло. При разрезе перикарда сердце выбрызнуло значительное количество зеленовато-желтого гноя. Успех! В течение нескольких дней после операции Сент-Онь, казалось, шел на поправку, но затем в рану на груди попала инфекция, и стали очевидны признаки повторного сдавления сердца. Бесстрашный Ларрей провел вторую операцию, однако в силу того, что тогда не было ни антисептиков, ни антибиотиков, инфекция одержала победу. Несчастный Сент-Онь умер более чем через два месяца после самонанесенного ранения, пожалев, что вообще это сделал.
Чтобы повысить качество и безопасность операций на органах грудной клетки, требовалось изобрести три вещи: анестетики, антисептики и антибиотики. У Ларрея из этого не было ничего.
И так было еще долгие годы.
В книге «Мемуары о военной хирургии и военных кампаниях», изданной в 1812 году, Ларрей описал шестерых выживших после ран перикарда, одним из которых был 24-летний солдат. Готовясь к попытке дренировать кровь из области вокруг сердца, Ларрей протестировал свой подход на трупах. Убедившись в правильности выбранной стратегии, он вырезал мертвую инфицированную ткань в месте проникновения пули, а затем, визуализировав растянутый перикард, ввел через оболочку эластичную резиновую трубку, чтобы удалить жидкость. Несмотря на отсутствие анестезии и антисептика, процедура прошла успешно, и мужчина выздоровел.
Разумеется, в Великобритании были свои выдающиеся хирурги. Известный как «Быстрейший скальпель Вест-Энда», доктор Роберт Листон якобы ампутировал гангренозную ногу пациента менее чем за две минуты.
К сожалению, скорость далась ценой точности, и вместе с конечностью пациента отрезали два пальца ассистента. Через несколько дней и пациент, и ассистент скончались от тяжелой стрептококковой инфекции. Но были ситуации и похуже: войдя в раж, Листон порезал окровавленным ножом пальто одного из зрителей – тот рухнул в обморок и скончался от сердечного приступа. Смертность в результате одной операции достигла 300 %, что до сих пор остается рекордом. Листон, с бравадой оперировавший на глазах изумленной публики, с готовностью размахивал своим острым скальпелем, восклицая: «Засеките время, джентльмены! Засеките время!»
Однажды, ампутируя без анестезии ноги выше колена, он случайно отрезал бедолаге яички. В другой раз рассек аневризму на шее мальчика, спутав ее с кистой, за чем последовало эффектное кровотечение. Несмотря на все это, Листон был решительным джентльменом и самым выдающимся хирургом своего времени. Его стремительный темп работы снижал смертность от кровопотери на операционном столе – именно этот фактор в итоге приобрел ключевое значение в кардиохирургии.
Термин «тампонада сердца» ввел лишь пятьдесят лет спустя немецкий хирург с типично английским именем Эдмунд Розе. Розе опубликовал статью, где перечислил характерные признаки сдавления сердца сгустками крови, обнаруженные у 23-х раненых пациентов, часть из которых выжила без хирургического вмешательства. Он пришел к выводу, что проникающие ранения сердца не всегда смертельны, как полагали ранее. В октябре 1872 года в больнице Святого Варфоломея в лондонском Ист-Энде хирург впервые целенаправленно оперировал травмированное сердце. После драки в трактире 31-летний портной ощутил острую боль в левой половине грудной клетки и не смог найти поразительно длинную иглу, которую обычно носил в кармане пальто. Первое посещение больницы ничего не дало, поскольку рентгенографии в то время еще не существовало. Девять дней спустя сильная боль сохранялась, когда он двигал левой рукой, – на этот раз мужчину госпитализировали, и врачи обнаружили у него скрытую колотую рану.
Хирург общей практики Джордж Каллендер сделал надрез между ребрами и нашел пропавшую иглу: она пронзила перикард вблизи верхушки левого желудочка. Иглу удалили без кровотечения. В наложении швов не было необходимости, и здоровье портного быстро восстановилось. Скромный Каллендер не рассказывал об прецеденте, и представление о неприкосновенности сердца сохранялось. Сам этот миф возник во многом благодаря Теодору Бильроту, бесспорному мастеру хирургии органов брюшной полости, который на заседании Венского медицинского общества в 1880 году заявил: «Любой хирург, желающий сохранить уважение своих коллег, никогда не попытается наложить швы на сердце».
Несомненно, главным достижением, способствовавшим развитию хирургии как профессии, стала анестезия. Почему? Потому что перспектива проведения длительной и мучительно болезненной операции на извивающемся пациенте никогда не была привлекательной.
Ларрей знал, что можно ампутировать конечность за несколько минут, но чтобы удержать пациента требовалась недюжинная сила нескольких крепких ассистентов.
С доисторических времен алкоголь, изготовленный из сброженного фруктового сока или зерна, применялся для облегчения боли. В студенческие годы я часто использовал его при зубной боли и регбийных травмах. Для приготовления обезболивающих снадобий использовались и травы: белена, белладонна, болиголов, мак и мандрагора, а китайский хирург Хуа То для облегчения агонии бодрствующих пациентов во время операций на органах брюшной полости применял седативное вещество скополамин[12]. В рукописи VIII века из Монтекассино[13] описана смесь из опия, мандрагоры, свежих маковых листьев и сока белены, которая вводила пациентов в бессознательное состояние. В XII веке к ингридиентам добавили сок плюща, шелковицу, салат и семена щавеля. При дистилляции этой смеси образовывалась очень крепкая алкогольная жидкость. Нужно было смочить ей губку, высушить, а затем прикладывать к носу и рту больного, чтобы тот лишился чувств. Для пробуждения в ноздри пациента закапывали уксус. Не пытайтесь повторить это дома, какой бы недоступной ни казалась вам медицинская помощь.
В 1776 году фермер и химик Джозеф Пристли открыл два газа: углекислый газ и закись азота.[14] В то время корнуоллский аптекарь Гемфри Дэви имел привычку испытывать на себе новые препараты и обнаружил, что закись азота вызывает чувство эйфории и благополучия, которое сменяется мигренью. Тем не менее он был заинтригован тем, что сильная боль от сломанного зуба исчезла вскоре после вдыхания газа. Практического применения это замечательное открытие не имело вплоть до 1844 года, когда в Хартфорде, штат Коннектикут, в число ярмарочных развлечений вошли «мужчины, которые не могут перестать смеяться» из-за вдыхания закиси азота. Бостонский дантист Хорас Уэллс наблюдал за увеселительным зрелищем с долей презрения, как вдруг один из идиотов упал со сцены и сломал себе руку. Уэллса удивил тот факт, что мужчина не кричал от боли, а истерически хихикал, не обращая внимания на страшную травму. Врач решил проверить гипотезу – и действительно, веселящий газ облегчал боль при удалении зубов.
Находясь под большим впечатлением от своей находки, Уэллс организовал демонстрацию для местных дантистов и хирургов. К сожалению, в тот раз оксид азота был подготовлен плохо, и разочарованный пациент взревел от боли. Дальнейшие эксперименты с веселящим газом имели смешанные и зачастую забавные результаты, и другой бостонский стоматолог, по имени Уильям Мортон, в качестве ингаляционного анестетика предложил использовать эфир. Для этого он разработал маску для лица: в нее наливали жидкий эфир, и пациент вдыхал его пары.
Известно, что 14 октября 1846 года Мортон применил эфирный анестетик на пациенте Гилберте Эбботе, у которого была большая опухоль на шее.
Эббот оставался без сознания на протяжении всего процесса, и хирург Джон Уоррен успешно его прооперировал. На следующий день эту технику повторили во время ортопедической процедуры, проведенной Генри Бигелоу в Массачусетской больнице общего профиля. Оригинальный дагеротип, запечатлевший саму операцию, до сих пор висит в Бостонской медицинской библиотеке. Общая анестезия с помощью эфира, в корне изменившая хирургическую практику, вскоре стала свободно использоваться в США, а всего через пару месяцев пришла и в Европу.
В ноябре 1847 года Джеймс Янг Симпсон, эдинбургский хирург и профессор акушерства, впервые использовал пары хлороформа для облегчения родовой боли.
Через месяц он сообщил о пятидесяти случаях применения хлороформа во многих гинекологических процедурах, что вызвало большой интерес. Принц Альберт узнал о пользе хлороформа от шотландского врача Джона Сноу, когда его супруга, королева Виктория, готовилась произвести на свет восьмого ребенка. Всего через два дня в замке Балморал у нее начались схватки, и Сноу срочно вызвали к королеве. Дыша хлороформом, которым был пропитан прижатый к ее лицу носовой платок, Виктория в полубессознательном состоянии, не чувствуя боли, родила принца Леопольда. Это стало для нее истинным откровением после семи предыдущих мучительных родов.

Рисунок 1.1: А. Джеймс Янг Симпсон. Б. Ингалятор с хлороформом.
Новость о хлороформе разлетелась мгновенно, и уже через пару недель французские и английские бригады скорой помощи использовали его на раненых солдатах во время боев за Севастополь.
Именно тогда американский врач Уэнделл Холмс-старший ввел термин «анестезия», образованное от греческого «без чувства».
Однако все было не так просто. В январе 1848 года в Ньюкасле во время удаления воспаленного ногтя на ноге внезапно скончалась 15-летняя Ханна Гринер, после чего опасность «хлороформного обморока» стала популярной для обсуждения темой в медицинских журналах. Мнения разделились. Сноу полагал, что смерть пациентки наступила из-за сердечной недостаточности, вызванной высокой концентрацией токсичных паров, но Симпсон и Джозеф Листер подозревали, что девушка погибла из-за угнетения дыхания.
Иногда несчастья приводят к положительным результатам. Так, 3 июля 1849 года хирург Чарльз Блик удалил грудь, пораженную раковой опухолью, 42-летней женщине, находившейся под действием хлороформа. Мастэктомия заняла всего четыре минуты, но при последнем движении скальпеля пациентка замертво упала на пол. Блик не смог нащупать пульс, женщина не дышала. Она не реагировала на холодную воду и аммиак, поднесенный к носу, поэтому Блик инстинктивно приступил к искусственному дыханию. После четвертого мощного вдувания женщина резко вдохнула воздух и вернулась к жизни. Бесстрашный хирург сразу приступил к удалению увеличенного лимфоузла в подмышечной впадине, во время чего пациентка ревела от боли и жаловалась на его резкий запах изо рта. Возможно, во всем был виноват аммиак, и, хотя это первый зафиксированный случай реанимации во время анестезии, Французская академия наук еще с 1740 года рекомендовала искусственное дыхание для приведения в чувства. Правда, распространялась эта рекомендация лишь на жертв утопления.
Вскоре после этого американский хирург Джеймс Меткалф рассказал о таком же достижении Нью-Йоркской медицинской академии: «Я сразу прижался губами к губам пациента, правой рукой придерживая его рот открытым, а левой закрывая нос. Я нагонял воздух в легкие медленно и осторожно, чтобы имитировать естественное дыхание. После 15–20 вдуваний пациент сделал слабый вдох, и из артерии в хирургическом разрезе брызнула кровь».
Меткалф порекомендовал искусственное дыхание для всех пациентов в хлороформном обмороке, и, хотя эфир оставался предпочтительным вариантом с точки зрения безопасности, хлороформ действовал быстрее, был доступнее для пациента и оказывал меньшее снотворное действие на хирурга.
Со временем стало очевидно, что смерть во время анестезии эфиром наступала из-за угнетения дыхания и что пациент реагировал на вентиляцию с положительным давлением. Смерть от хлороформа, напротив, была результатом сердечной недостаточности и требовала более масштабных реанимационных мероприятий. В 1870 году Мориц Шифф, профессор физиологии из Флоренции, предложил вскрывать между ребрами левую половину грудной клетки, чтобы делать прямой массаж сердца. Он практиковал это на собаках. «Необходимо совершать ритмичные движения рукой, держа сердце целиком», – писал он. Проявив удивительную проницательность, Шифф предположил, что возвращение к жизни происходило благодаря восстановлению тока крови по коронарным артериям, а не только механической стимуляции. Он даже предложил пережимать во время прямого массажа главную артерию тела, брюшную аорту, чтобы кровь направлялась преимущественно к мозгу и сердцу.
Прошло еще тридцать лет, прежде чем в 1901 году появилось сообщение об успешном массаже сердца. В тот раз хлороформ использовали на 43-летней женщине с раком матки, у которой в конце гистерэктомии[15] произошла остановка сердца. После неудачного искусственного дыхания норвежский хирург Кристиан Игельсруд быстро провел левую торакотомию[16] и сделал массаж желудочков большим, средним и указательным пальцами. Через минуту кровоснабжение сердечной мышцы восстановилось. Орган напрягся и начал сокращаться. Более того, женщина смогла пережить этот мучительный опыт и полностью восстановилась.
Через два года в Лондоне сэр Уильям Арбетнот Лейн повторил успех своего коллеги во время проведения операции на кишечнике у 65-летнего пациента. Когда сердце мужчины остановилось из-за анестезии эфиром, Лейн просунул руку в разрез в животе и стал через диафрагму прижимать сердце к грудине. Вместе с искусственным дыханием этого оказалось достаточно для восстановления циркуляции крови, и пациент пришел в себя.
В 1903 году доктор Джордж Крайл сообщил о первом успешном применении наружных компрессий грудной клетки для реанимации пациента в США.
На протяжении большей части XIX века операции проводились только при острой необходимости, и на то была веская причина. О связи между бактериями и инфекциями еще не подозревали. Инфицирование раны и нагноение считались нормальными этапами заживления, однако они приводили к высокой смертности после хирургических вмешательств. Ходили даже разговоры о том, чтобы вовсе запретить операции во многих больницах из-за последствий сепсиса. Сэр Джон Эриксен, президент Королевского колледжа хирургов, настаивал: «Для мудрого и гуманного хирурга живот, грудь и мозг навсегда останутся закрытыми для вторжения». Это была эпоха, когда больничное белье и лабораторные халаты не стирали, а хирургические инструменты мыли только перед тем, как убрать их на хранение. Один и тот же металлический зонд использовался во время больничного обхода для исследования очагов нагноения у множества пациентов. Эриксен считал, что воспаление и гной возникали из-за зловещих миазмов, которые исходили из самой раны и концентрировались в воздухе. По его убеждению, в палате, где лежало 10 пациентов, инфицированные раны у половины из них насыщали атмосферу опасными газами, вызывавшими гангрену. Гангренозные конечности приходилось ампутировать.
Увлеченный хирург-стажер по имени Джозеф Листер работал ассистентом у сэра Джеймса Сайма. В возрасте всего 33 лет Листер, сын выдающегося члена Королевского общества, стал профессором хирургии в Университете Глазго благодаря своему раннему интересу к воспалению и экспериментам в этой области.
Интеллектуальный прорыв произошел, когда, по совету профессора химии, он прочел статью Луи Пастера «Исследования о брожениях». Эта работа на тему бактериального механизма ферментации побудила Листера задуматься, могут ли микроорганизмы участвовать в нагноении хирургических ран и развитии гангрены после открытых переломов конечностей.

Рисунок 1.2: А. Джозеф Листер. Б. Диффузор карболовой кислоты.
Он пришел к выводу, что инфекция развивалась, когда кости и подкожные ткани становились уязвимы к заражению при нарушении целостности кожного покрова. Огромная разница в выживаемости пациентов зависела от того, какой была травма – открытой или закрытой.
Узнав, что креозот[17] применяется для дезинфекции сточных вод, Листер впервые использовал карболовую кислоту в качестве кожного антисептика. Он прилагал усилия, чтобы уменьшить число бактерий в хирургической палате: обрабатывал руки и инструменты дезинфицирующим средством, распылял его над операционным столом. Листер продемонстрировал, что раны могут заживать без инфицирования, которое раньше считалось неотъемлемым звеном периода восстановления.
«Было бы неправильно и дальше скрывать этот факт от профессионального сообщества», – писал хирург.
Результаты он изначально представил в двух публикациях в журнале Lancet в 1867 году, а затем в том же году их вынесла на обсуждение Британская медицинская ассоциация в Дублине. Листер объяснял зачарованной аудитории: «До ее введения [техники дезинфекции] две большие палаты, где находится большинство моих ортопедических и травматологических случаев, были одними из самых больных во всем хирургическом отделении Королевского госпиталя Глазго. Однако с тех пор, как в полную силу стала проводиться антисептическая обработка, состояние этих палат полностью изменилось. За последние девять месяцев в них не было ни единого случая пиемии[18], гангрены или рожи». Прекрасные результаты, учитывая, что до открытия антибиотиков оставалось 60 лет.
Если ранее хирурги оперировали загрязненными инструментами, на которых порой даже оставалсь запекшаяся кровь, принципы дезинфекции Листера быстро повысили шансы на выживание всех хирургических пациентов. Лидировала Германия, за ней следовали США и Франция – только Великобритания скептически отнеслась ко все этой затее. Собственно, как всегда! Возможно, такая реакция объяснялась тем, что Листер славился своим тяжелым характером. Он отказался делиться открытием с коллегами, был против женщин в хирургии и резко критиковал обучение медицине во Франции. Он был типичным хирургом из привилегированной семьи, которого в итоге удостоили титула пэра.
Хорошо известной чертой хирургов (и врачей в целом) является способность трубить об успехах и забывать о неудачах.
Так было и с доблестными усилиями по спасению пациентов с ранениями сердца. Мы знаем лишь о некоторых из них, но о многих – нет. Более того, предположения о том, что операции на сердце были невозможны из-за романтической фантазии о сердце как вместилище души, полнейшая чепуха. Проблема была в том, что хирургам не хватало уверенности оперировать движущуюся цель. Американец Чарльз Эльсберг сказал: «Нельзя забывать, что нам приходится иметь дело с постоянно движущимся органом, который считается очень чувствительным к любым механическим повреждениям или травмам. Все боялись, что при малейшей манипуляции сердце может внезапно остановиться и что простого прохождения иглы достаточно, чтобы привести к ужасающим последствиям». Даже добраться до сердца было крайне трудно. При вскрытии грудной клетки у пациентов неизбежно случался коллапс легкого с последующими трудностями с дыханием. Требовалось настолько большое количество анестетика, что хирург тоже вдыхал немалую дозу.
В 1876 году гамбургский врач Готхард Бюлау стал вводить трубки между ребрами для удаления скопившейся крови, воздуха или гноя. Важным дополнением к этой процедуре стал сифонный подводный дренаж, предотвращающий попадание воздуха в грудную полость через дренажную трубку. Стоящая у постели бутылка с водой позволяла удалять внутриплевральные скопления вокруг легкого, не вызывая коллапса, и стала стандартным дополнением к любым видам торакальной хирургии.
В 1895 году молодой норвежский хирург Аксель Каппелен должен был оказать помощь 24-летнему пациенту с ножевым ранением левой половины грудной клетки. Из-за болевого шока пациент был без сознания, и Каппелен решил, что ничего не потеряет, если исследует рану. Он обнаружил, что нож прошел через грудную стенку рядом с грудиной, и, когда хирург удалил четвертое ребро, кровь хлынула через отверстие в перикарде. Под ним был разрыв левого желудочка длиной более 2 см: сердце продолжало истекать кровью при каждом ударе, несмотря на падение артериального давления. Более того, лезвие рассекло дистальный[19] конец крупной коронарной артерии, и он кровоточил отдельно. Бесстрашный Каппелен, внутри которого зашкаливал адреналин, стал зашивать рану кетгутовой нитью, осторожно накладывая швы на трепещущий под рукой орган. По факту это не очень сложная задача, но в медицинской литературе того времени не было описано ни единого случая успешного наложения швов на сердце, поэтому Каппелен действовал инстинктивно.
Кетгут годился для человеческого кишечника, но не сердца. Вдобавок натяжение, примененное к каждому узлу, было критическим. Очень легко перетянуть нить и разрезать ей травмированную мышцу так, что кровь брызнет вам в лицо. Сердечный ритм нарушается из-за манипуляций и протыкания иглой. К сожалению, Каппелену пришлось лигировать[20] поврежденную артерию, оставив значительную область сердечной мышцы без кровоснабжения. В те времена переливание крови не проводилось, поэтому пациенту ввели солевой раствор, чтобы поднять артериальное давление. К радости врачей, мужчина пришел в сознание, но спустя два дня после операции умер от сердечной недостаточности. Вскрытие подтвердило, что ножевое ранение было зашито надежно, но длительная ишемия привела к отмиранию миокарда в левом желудочке.
Слава ускользнула от Каппелена просто потому, что была повреждена коронарная артерия. Правый желудочек с низким давлением находится непосредственно за грудиной и чаще становится жертвой ножевых ранений, так что чествование кардиохирурга-первопроходца было лишь вопросом времени. В итоге удача улыбнулась немецкому хирургу Людвигу Рену. Рен к тому моменту и так внес важный вклад в медицину, заметив, что работники красильной промышленности, подверженные длительному воздействию анилина, имеют повышенный риск развития рака мочевого пузыря. В сентябре 1896 года он прооперировал 22-летнего солдата, которого уволили из армии из-за ревматической болезни клапанов сердца. Во время пьяной драки мужчину ударили ножом: лезвие прошло через переднюю грудную клетку и пронзило правый желудочек. Естественно, травма привела к сильному кровотечению, но, когда кровь скопилась в перикарде, оно замедлилось и давление в камере упало.
Хрупкий баланс, который часто останавливает сильное кровотечение при резаных ранах, оставил Рена в ситуации «побеждает отважный».
Когда Рен вскрыл грудную клетку слева между ребрами и удалил сгусток крови из перикарда, возобновившееся кровотечение подсказало ему, куда накладывать швы. Всего трех оказалось достаточно. Следуя антисептическим принципам Листера, Рен обложил грудную клетку марлей, пропитанной йодом, прежде чем зашить разрез, благодаря чему пациент выжил. У солдата все же скопился гной вокруг левого легкого, но известно, что через десять лет после операции он все еще был жив. Ознаменовал ли успех Рена начало кардиохирургии, как заявляют многие историки? Вовсе нет. На протяжении веков больше пациентов с ранениями сердца выживали без хирургического вмешательства, а не с ним. В книге Anatomical Observations, изданной в 1604 году, французский хирург Бартелеми Каброл описал множество сердец со шрамами от старых проникающих ранений, которые были изучены во время посмертного патологоанатомического исследования. В The Surgery of the Chest Пэджета, опубликованной в 1923 году, автор рекомендовал больным с ранениями сердца «полный покой тела и разума, легкую диету и в некоторых случаях морфин». Если это оказывалось безуспешным, «можно было постучать по перикарду или сделать в нем небольшой разрез, чтобы облегчить тампонаду сердца». Естественно, большинство пациентов не доживали до этого момента.
В США первая операция на открытом сердце состоялась 14 сентября 1902 года. На первый взгляд, удивительно поздно, учитывая, что гражданская война в Америке 1860-х годов привела к 750 тысячам смертей, большинство из которых наступили в результате инфицирования ран или дизентерии. Так получилось, что хирург, о котором идет речь, прошел обучение в Великобритании с Джозефом Листером и, подобно Рену, следовал антисептическим принципам своего начальника. Лютер Хилл из Монтгомери, штат Алабама, был приглашен домой к тринадцатилетнему мальчику, получившему пять ножевых ранений в грудь. Хилл увидел его «задыхающимся, возбужденным, в шоковом состоянии, с едва прощупываемым пульсом и непрослушиваемыми звуками сердца». Диагностировав тампонаду сердца и помня об успехе Рена, он вскрыл грудную клетку под светом масляной лампы. Он описал тот случай в статье, опубликованной в медицинском журнале:
«Рана на груди была около трех восьмых дюйма в длину[21], при каждой систоле из нее вытекала струя крови. В час ночи, спустя восемь часов после получения ножевых ранений, я переложил мальчика с постели на стол и приступил к дезинфекции операционного поля и создал вокруг пациента настолько благоприятные условия, насколько позволяла негритянская хижина. Начав разрез приблизительно в половине дюйма от левой границы грудины, я вел его вдоль третьего ребра, и в итоге его длина составила четыре дюйма. Второй разрез был начат на том же расстоянии от грудины, прошел вдоль шестого ребра и также составил в длину четыре дюйма. Затем я сделал вертикальный разрез вдоль передней подмышечной линии, соединив первые два разреза. Я поднял костно-мышечный лоскут, и реберные хрящи (рядом с грудиной) выполнили функцию шарниров. Крови в плевральной полости не оказалось, но перикард был чрезвычайно растянут. Я расширил рану перикарда до двух дюймов и извлек оттуда около восьми унций[22] крови. Пульс сразу улучшился (когда тампонада была устранена), как сказал доктор Л. Д. Робинсон, успешно и умело применивший хлороформ. Я попросил доктора Р. С. Хилла, моего брата, просунуть руку в полость перикарда, приподнять сердце и стабилизировать его настолько, чтобы я мог зашить кетгутовой нитью центральную часть раны и взять под контроль кровотечение. Я очистил перикард солевым раствором и наложил на рану семь прерывистых стежков. Плевральную полость я также промыл солевым раствором и дренировал марлей с йодоформом. Операция продлилась 45 минут. На момент перекладывания в постель пульс пациента составлял 145, частота дыхания – 56. Я ввел стрихнин[23] подкожно и провел аутотрансфузию[24]. 17 сентября состояние пациента стало улучшаться, выздоровление проходило без осложнений».

Рисунок 1.3: А. Людвиг Рен. Б. Лютер Хилл.
В статье, опубликованной в журнале Medical Record 29 ноября 1902 года, представлена таблица из 37 других случаев экстренных операций на раненых сердцах, проведенных по всему миру с 1896 по 1902 год. Одиннадцать пациентов выжили. Хилл пришел к выводу, что «любая операция, сокращающая смертность почти на 30 %, заслуживает своего места в хирургии» и что «любая рана сердца должна быть незамедлительно прооперирована». Это был оптимистичный шаг вперед после Бильрота и Пэджета, но до Второй мировой войны ситуация почти не менялась. Кардиохирургия была отложена до дальнейших достижений в области анестезии, диагностики и борьбы с инфекциями.
8 ноября 1895 года Вильгельм Рентген, профессор физики из Вюрцбургского университета, совершенно случайно открыл рентгеновские лучи. Неведомое излучение из катодной трубки могло проходить через ткани и оставлять изображение на фотопластинке. Первым рентгеновским снимком стал снимок кисти супруги физика с обручальным кольцом, сделанный 22 декабря 1895 года. Это открытие оказало большое влияние на мир медицины, и Рентген получил Нобелевскую премию.
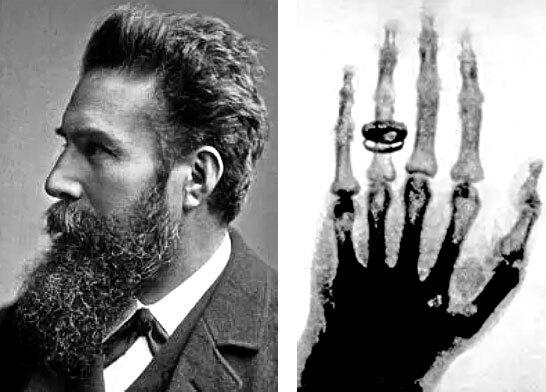
Рисунок 1.4: А. Вильгельм Рентген. Б. Первый рентгеновский снимок с изображением руки жены Рентгена.
Впервые рентгеновские лучи использовали в целях диагностики через год, когда в лондонскую больницу доставили пьяного моряка с ножом в спине. Он был парализован, и рентгеновский снимок позвоночника показал, что кончик лезвия вошел между двумя позвонками и проник в позвоночный канал. После операции по удалению инородного предмета паралич разрешился.
В 1903 году французский хирург Теодор Тюффье с помощью рентгеновских лучей обнаружил пулю в груди раненого солдата. Тюффье, сторонник торакотомии для проведения прямого массажа сердца, идентифицировал пулю внутри границ тканей сердца и во время хирургического вмешательства нашел ее среди фибринозных спаек в перикарде. Само сердце не было повреждено, и он смог извлечь пулю пальцами. Мужчина выздоровел.
Электрокардиография появилась на рубеже веков, когда Виллем Эйнтховен из Лейдена модифицировал струнный гальванометр и разместил электроды на грудной стенке, чтобы считать электрические импульсы сердца. В 1903 году он определил характерные зубцы P, Q, R и S, соответствующие циклам сердечных сокращений, и обнаружил изменения в электрокардиограмме пациентов с заболеваниями сердца. Так к гальванометру присоединили чернильный полиграф для изучения механизма нарушений сердечного ритма, однако лишь в 1919 году врач Джеймс Херрик описал электрокардиографические изменения, наблюдаемые при тромбозе коронарных артерий и инфаркте миокарда. Результаты вскрытия подтвердили его предположения.
Вскоре провели первую визуализацию сердца и кровеносных сосудов, причем по инициативе уролога. Вернер Форсман хотел попробовать вводить трубки в кровеносные сосуды, чтобы во время чрезвычайных ситуаций на операционном столе доставлять в сердце пациентам стимулирующие препараты. Ему был доступен только мочевой катетер. С легкостью добравшись до правого предсердия через вену на руке трупа, Форсман попросил ассистента помочь ему провести катетеризацию собственной вены.
У ассистента сдали нервы, и Форсман сам надрезал себе вену на сгибе левой руки и через иглу с большим отверстием протолкнул в кровоток тонкую трубку.
Наблюдая в зеркало за рентгеновским экраном, он по вене протолкнул катетер к правой половине сердца, а затем поднялся в рентгенологическое отделение больницы, чтобы подтвердить свое достижение.
Через два года Форсман успешно использовал йодосодержащий контрастный препарат для визуализации кровеносных сосудов у собак. К сожалению, когда он решил повторить эксперимент на себе, все прошло не так хорошо: у него началась аллергическая реакция, которая чуть не привела к летальному исходу. Только в 1938 году нью-йоркские рентгенологи применили йодосодержащий контрастный препарат для визуализации правых камер сердца и кровеносных сосудов легких. Вскоре была проведена ангиография левых камер сердца и крупных артерий, послужившая мощным толчком в развитии исследовательской кардиологии и плановой хирургии.
Одним из важнейших достижений в области анестезии стала концепция обратимого двигательного паралича, осуществимая с помощью кураре[25]. Она позволила контролировать дыхание посредством ритмичного раздувания легких, и в 1910 году эту технику дополнили введением эндотрахеальной трубки. Инструмент под названием ларингоскоп был разработан для визуализации голосовых связок, особую популярность он обрел во время Первой мировой войны, когда британские анестезиологи Магилл и Роуботам применили интубацию трахеи и вентиляцию легких с положительным давлением на пациентах, которым сэр Гарольд Гиллис проводил пластические операции. В случаях, когда лицо, голова и шея пациента были сильно обожжены или изранены, пластические операции могли длиться много часов, и анестезия с помощью маски была неподходящей.
Следующей деталью мозаики стало появление антибиотиков – это событие кардинально изменило всю медицинскую практику.
В 1928 году в больнице Святой Марии в Лондоне бактериолог Александр Флеминг случайно открыл пенициллин, когда выращивал бактерии стафилококка.
Сотрудники лаборатории находились в отпуске, и чашки Петри простояли на столе три недели. В них разрослась таинственная плесень, споры которой, видимо, залетели через окно. По возвращении Флеминг увидел, что колонии стафилококков, контактировавшие с плесенью, погибли. Какой бы ни была природа этого чужеземца, он обладал способностью уничтожать опасный источник инфекции. Флеминг назвал плесень пеницилином и из любопытства решил вырастить ее отдельно. Затем он добавил ее к другим бактериям, включая стрептококки, пневмококки, гонококки, менингококки и дифтерийную палочку, каждая из которых ежегодно убивала огромное число людей. Во всех случаях при контакте с пенициллином бактериальные колонии гибли, но здоровым животным пенициллин не наносил никакого вреда.
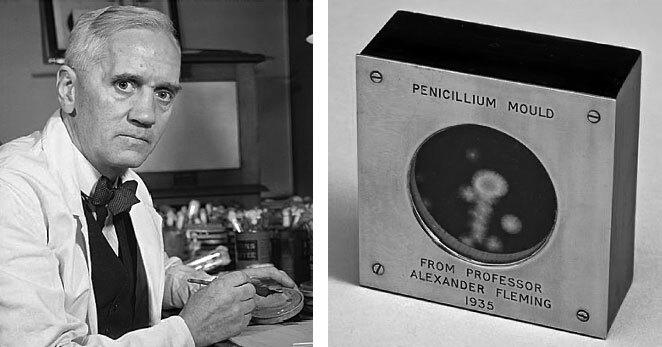
Рисунок 1.5: А. Александр Флеминг. Б. Оригинальная чашка Петри.
Флеминга злило, что он не в состоянии изолировать активный компонент плесени, а когда он смешивал ее в пробирке с кровью, бактерицидный эффект, похоже, исчезал. Написав короткую статью на эту тему в 1929 году, он оставил исследования – в итоге тысячи пациентов продолжили умирать от простых хирургических инфекций.
Вернемся в Оксфорд. В 1937 году Говард Флори, талантливый молодой выпускник одного из австралийских университетов, был назначен руководителем Школы патологии сэра Уильяма Данна. Во время войны Флори заинтересовался борьбой с сепсисом и принял на работу еврейского биохимика Эрнеста Чейна, бежавшего
