автордың кітабын онлайн тегін оқу Как мы стареем
Колин Мёрфи
Как мы стареем. Наука о долголетии
Copyright © 2023 by Princeton University Press
All rights reserved. No part of this book may be reproduced or transmitted in any form or by any means, electronic or mechanical, including photocopying, recording or by any information storage and retrieval system, without permission in writing from the Publisher
© Т. Мосолова, перевод на русский язык, 2026
© А. Бондаренко, художественное оформление, макет, 2026
© ООО “Издательство Аст”, 2026
Издательство CORPUS ®
* * *
Посвящается моим родителям
Вступление
Часто там, где есть несоответствие, кроется нечто особенно интересное!
Эвелин Уиткин, американский генетик, отпраздновавшая столетний юбилей 9 марта 2021 г.
В конце 1990-х годов я была аспиранткой в лаборатории Джима Спудича на биохимическом факультете Стэнфордского университета. Я изучала функцию двигательного белка миозина – молекулярного мотора, обеспечивающего движение наших мышц и насосную функцию сердца: меняла местами фрагменты миозина из “медленных” и “быстрых” организмов и проверяла, как это влияет на их активность. Мне нравился этот белок; в то время меня больше всего интересовало, как правильно организованная последовательность аминокислот позволяет получать энергию и превращать ее в движение, потихоньку перемещая “плечо рычага”. Но когда на вечеринках меня спрашивали, чем я занимаюсь, и я объясняла суть моих исследований, мне в ответ кивали и вежливо улыбались, а потом интересовались, когда я закончу учебу. На этом разговор заканчивался.
Все изменилось через несколько месяцев, когда я услышала потрясающий доклад профессора Синтии Кеньон из Калифорнийского университета в Сан-Франциско. Синтия живо и увлеченно рассказывала об исследованиях старения и продолжительности жизни маленького червя – нематоды Caenorhabditis elegans. В ее лаборатории установили, что замена одного-единственного гена может удвоить продолжительность жизни этого животного[1], и она показала видеозапись ползающих мутантных червей такого возраста, в котором нормальные черви уже дряхлеют и умирают. Это было просто потрясающе, и было ясно, что речь идет не о продлении старости, а скорее об удлинении молодой и здоровой части жизни, о чем мечтает каждый из нас. Этот ген, названный daf-2, кодирует рецептор инсулина/инсулиноподобного фактора роста 1 (ИФР-1) и, следовательно, может иметь значение и для человека, поскольку в нашем теле тоже вырабатывается инсулин. Выслушав доклад, я поняла, чем хочу заниматься: меня интересовало, почему этот мутантный червь был таким здоровым. Вскоре я спросила у Синтии, нельзя ли мне устроиться на работу в ее лабораторию после защиты диссертации[2], и она разрешила. С этого момента, когда меня спрашивали, чем я занимаюсь, все было совсем иначе. Выяснилось, что тема старения интересует буквально всех, и у каждого на этот счет есть личное мнение. Вскоре я поняла: вероятность, что человек поддерживает идею исследований старения, коррелирует с его возрастом, – и меня неоднократно призывали “работать побыстрее”.
Книгу я решила написать после того, как составила для Принстонского университета курс “Молекулярные механизмы долгожительства: генетика, геномика и клеточная биология старения”, чтобы рассказывать студентам о моей области исследований. Подготавливая материал для лекций, я осознала, что за последние двадцать лет мы (королевское “Мы” с заглавной буквы – исследователи в области старения и долгожительства) открыли много молекулярных механизмов, которые неплохо было бы разъяснить широкому кругу людей. Рынок популярных книг о долгожительстве перенасыщен (было выпущено несколько отличных вводных изданий, а мнение очередной знаменитости по вопросам старения или еще одна книга о правильном питании никому не требуется), но вот понять смысл современных достижений в этой области на молекулярном уровне кому-то может быть интересно. Как я расскажу далее, за последние двадцать лет мы МНОГОЕ узнали о регуляции продолжительности жизни, и это может подсказать нам, как замедлить приближение старости. Теперь нам больше известно о генетических путях и клеточных процессах, регулирующих межклеточную коммуникацию, которая определяет скорость старения, и мы стали лучше понимать, почему старение вообще подвергается регуляции. Новые открытия помогли придумать, как замедлить возрастные изменения, и у нас наметилось несколько хороших мишеней для медикаментозного воздействия. Некоторые из этих новых открытий недавно вылились в серьезные биотехнологические разработки, и за последние годы появилось много компаний, занятых вопросами старения и продолжительности жизни.
Мне повезло, и я оказалась в центре этих исследований в 2000-е годы, как раз когда были открыты новые гены, контролирующие продолжительность жизни. Начало нового тысячелетия стало поистине поворотным моментом: вслед за бактериями и дрожжами был прочитан геном первого многоклеточного организма, C. elegans, а вскоре пришла очередь дрозофилы. Эти крупномасштабные программы – прямое следствие разработки технологий, способствовавших реализации проекта по секвенированию генома человека, – помогли биологам проводить невозможные ранее эксперименты на уровне целых геномов. Механизм РНК-интерференции (РНКи), вызывающий разрушение матричной РНК (мРНК) конкретного гена, впервые был подробно описан для C. elegans Крейгом Мелло и Эндрю Файром в 1998 году[3] и вскоре начал применяться в экспериментах с червями для проверки всех генов генома в поисках любых интересных признаков (включая старение) с помощью новых методов отключения экспрессии генов[4]. Возможность быстро анализировать большое количество генов червей привела к революции в функциональной геномике (теперь можно проверять связь всех генов генома с конкретной функцией), и с тех пор эта область исследований расширяется по многим направлениям.
Я стала заниматься старением, поскольку меня увлек вопрос, каким образом продолжительность жизни и старение контролируются на генетическом и биохимическом уровне. В это время появились новые инструменты, такие как микрочипы для анализа экспрессии генома и РНКи, которые обеспечили не существовавшую ранее возможность изучать долгоживущих мутантов (животных с изменениями в ДНК, затрагивающими какой-то конкретный ген) и понимать, что происходит у них внутри. Определение полных геномных последовательностей всех этих организмов ускорило развитие новых геномных технологий (микрочипы ДНК и позднее секвенирование нового поколения), что позволило одновременно анализировать все гены организма и изучать внутреннюю работу клеток по мере их старения. С тех пор объем доступных для исследователей данных неимоверно расширился. Генетические и геномные методы анализа проникли в область исследований продолжительности жизни, и крупномасштабные исследования метаболизма тоже способствовали расширению наших знаний. Кроме того, новые молекулярные инструменты, например редактирование генома CRISPR и стволовые клетки, раскрыли удивительные перспективы для изменения человека с целью улучшения его здоровья[5].
Тематика направления – изучение механизмов старения – такова, что это чрезвычайно обширная область исследований. Рассматривать проблемы старения можно в самых разных аспектах: демография, популяционная генетика, эволюция, генетика модельных систем, молекулярная биология, клеточная биология, диетология и фармакология. Все эти аспекты помогают понять, как происходит старение и как можно его замедлить. Я расскажу о том, как продвигается работа в моей лаборатории (и постараюсь говорить не только о нашей лаборатории), а также о последних достижениях в этой области исследований в целом. Направление быстро развивается, постоянно совершаются новые открытия, и поэтому неизбежно какие-то вопросы останутся незатронутыми, но я попытаюсь объяснить не только что мы знаем, но и как мы это узнаем, – расскажу, как работают ученые, чтобы разобраться в проблеме.
В книге вы не найдете описания того, что я ем, или что едят другие ученые, или сколько мы весим, или как часто занимаемся спортом, – здесь нет такой информации, которая фактически стала нормой в научно-популярных книгах и статьях о старении и об исследователях, изучающих эту проблему. Я занимаюсь наукой и не хочу читать все эти непонятные результаты, полученные для одного пациента, поэтому о подобных вещах говорить не буду: это плохо сделанная наука. Кроме того, я заметила странный “культ личности” вокруг некоторых книг о старении, в результате которого на вклад женщин-ученых часто не обращают внимания. И еще я не отношусь к числу проповедников долгожительства, так что не стану пытаться вам что-либо продать – никаких биологических добавок, лекарств или растительных диет. Я хочу только рассказать, что мы знаем о старении и как мы это узнали.
Наконец, я постараюсь избегать выражений типа “…по крайней мере, у червей и дрозофил”, которые столь часто встречаются в книгах о старении. Я активная сторонница использования модельных систем по одной простой причине: почти все, что нам известно о механизмах контроля (регуляции) продолжительности жизни на молекулярном уровне, изначально было установлено на модели беспозвоночных животных, а затем проверено на более крупных организмах (на таких млекопитающих, как мыши), но об этом часто забывают. Кроме того, все инструменты, позволяющие нам делать эту работу и продвигаться к человеческим клеткам, поначалу были идентифицированы, охарактеризованы и проверены на простых модельных системах, и лишь потом их адаптировали для работы с млекопитающими (возможно, самый яркий пример – система CRISPR, впервые обнаруженная у бактерий). Вообще говоря, без модельных систем наше понимание регуляции продолжительности жизни было бы весьма ограниченным. И по этой причине я буду рассказывать не только об исследованиях на людях и о какой-то предварительной проверке на мышах, но попытаюсь описать, как на самом деле мы установили молекулярные закономерности процессов внутри всех наших клеток – а это было сделано в результате исследований на модельных системах маленьких беспозвоночных животных. Наверное, Сару Пэйлин, которая не признает вклад фундаментальных (“базовых”) исследований в медицину[1], это бы шокировало, но всем остальным, надеюсь, это даст возможность лучше понять, как ученые постигают устройство мира и как мы можем применить наши знания, чтобы помочь людям жить лучше, – и, как сказала бы Пэйлин, я не шучу.
Надеюсь, эта книга даст вам представление о том, что мы узнали о долгожительстве за последние годы. Но прежде чем погрузиться в научные рассуждения, хочу объяснить, почему нужно изучать старение: возможно, это понятно не сразу, но изучение старения полезно нашему обществу в долгосрочном плане, в том числе в экономическом (первая глава), поскольку долгожительство – прерогатива не только миллионеров. Есть много эволюционных теорий, объясняющих, почему мы стареем (вторая глава), но современные молекулярные методы помогают лучше понять этот процесс и соответствующие теории. В третьей главе мы начнем обсуждать, каким образом современная генетика и геномика способны раскрыть секреты долгожительства людей, перешагнувших столетний рубеж. Но для экспериментальной проверки гипотез нам нужны модельные организмы, то есть хорошо изученные животные, которых можно выращивать в лаборатории и с которыми можно производить генетические манипуляции (четвертая глава). Чтобы понимать, о чем идет речь при изучении старения и как анализируют возрастные изменения, нам придется ввести несколько определений (пятая глава). В последующих главах я подробно расскажу о том, что нам сегодня известно о механизмах долгожительства и о возможностях воздействия на эти механизмы (главы с шестой по десятую), и вы узнаете о некоторых молекулах, которые служат мишенями в клинической практике (семнадцатая глава). Взаимоотношения полов и репродукция неразрывно связаны с продолжительностью жизни, и об этом мы поговорим в одиннадцатой и двенадцатой главе. Наши чувства тоже определяют продолжительность нашей жизни (тринадцатая глава), а старение изменяет наши чувства и когнитивную функцию (четырнадцатая глава). Некоторые самые новые концепции показывают, что мы наследуем от наших предков какие-то факторы, которые влияют на старение (пятнадцатая глава); также немаловажную роль играют наша пища и микробы у нас в кишечнике (шестнадцатая глава). Наконец, обсудим современное состояние биотехнологических исследований в области долгожительства и поиски лечения для борьбы с возрастными изменениями (семнадцатая глава).
Исследования процессов регуляции старения находятся на подъеме, и это замечательный период, поскольку мы все еще продолжаем делать открытия. Я не хочу сказать, что мы знаем ответы на все вопросы. Но надеюсь передать вам то, что мы действительно знаем, и, что еще важнее, откуда мы это знаем, и что мы можем сделать со всеми этими данными. С такими знаниями нам проще будет принимать мудрые решения относительно продолжительности собственной жизни.
“Вы слышали о некоторых таких проектах с домашними животными, в них нет большого смысла, и иногда деньги направляют на проекты, которые не имеют никакого или почти никакого отношения к общественным нуждам. На такие вещи, как исследования дрозофил в Париже, во Франции. Я не шучу” – отрывок из высказывания Сары Пэйлин, процитированного в статье Адама Резерфорда “Пэйлин и дрозофилы”, Guardian, 27 октября 2008, https://www.theguardian.com/commentisfree/2008/oct/27/sarahpalin-genetics-fruit-flies. (Сара Пэйлин – американский политик и журналист, сторонница идеи креационизма. – Прим. перев.)
Глава 1
Этика и экономика долгожительства.
Нужно ли изучать старение?
Удивительно, что мысль о долгой жизни нравится всем, но мысль о старении не нравится никому.
Энди Руни, тележурналист
Поисками бессмертия занимались представители всех культур во все времена. Древние тексты повествовали о долгой жизни вождей, переживших много поколений: в Ветхом Завете сказано, что Мафусаил прожил 969 лет, в соответствии с индийским эпосом Бхишме было 128 лет, в поэме о Гильгамеше утверждается, что царь Месопотамии правил 126 лет, гунн Аттила якобы прожил 124 года, и поговаривали, что Александр Великий дошел до райской реки. (Считалось, что Хуан Понсе-де-Лион прибыл во Флориду в поисках источника вечной молодости, однако скорее им двигало желание найти золото, дешевую рабочую силу и землю для испанской короны.) Даже сегодня в племенах, не регистрирующих рождения, нередко встречаются люди, якобы давно преодолевшие столетний рубеж, хотя их возраст кажется изрядно преувеличенным (например, я почти уверена, что старой женщине, с которой мы познакомились в деревне племени масаев, было не 105 лет, но кто я такая, чтобы это утверждать?). Поиски секрета долголетия продолжают занимать наше воображение. Однако вместе с тем они подпитывают наши страхи, отображенные Оскаром Уайльдом в “Портрете Дориана Грея”. Да и тот факт, что Голлум прожил 598 лет благодаря свойствам своего кольца, вряд ли может послужить рекламой здорового увеличения срока жизни. Следует спросить самих себя: разумно ли стремиться к долголетию?
На сегодняшний день мы применяем немыслимые диеты, сомнительные методы лечения, препараты и крионику[2], а в Кремниевой долине развиваются многочисленные проекты, направленные на поиски возможных путей борьбы со старением. Эти поиски способов “излечения от старости” дополнительно ускорились с новыми научными достижениями, в свете которых перспектива менять свою судьбу выглядит все более заманчивой. Однако перспектива эта требует от нас умения отличать реальные возможности замедлить старение от шарлатанства. Прежде чем обсудить, как мы узнаем о механизмах, контролирующих продолжительность жизни, нам следует рассмотреть плюсы и минусы самих этих изысканий.
То, от чего мы умираем, зависит от того, кто мы такие
В XX веке произошло, по-видимому, самое значительное в истории США увеличение средней продолжительности жизни: от 48 до 74 лет для мужчин и от 51 до 80 лет для женщин[1]. Слыша выражение “продолжительность жизни”, мы обычно думаем о преклонном возрасте, однако по большей части этот невероятный скачок был достигнут благодаря улучшению бытовых условий и медицинской помощи, снизившему уровень смертности детей и младенцев, а не благодаря повышению качества лечения в старости. В целом это продление произошло за счет устранения факторов, укорачивавших жизнь молодых и здоровых людей. Например, один из самых ощутимых ударов по средней продолжительности жизни в недавней истории был нанесен в 1918 году вирусом гриппа, который в основном поражал молодых людей[3].
Усовершенствования в сфере общественного здравоохранения, снизившие смертность среди молодых людей и людей среднего возраста, такие как общие санитарные нормы (мытье рук, очистка воды, туалеты) и доступность антибиотиков, уменьшили и общие показатели смертности. Медицинская помощь в ранний период жизни, особенно прививки против детских болезней, в значительной степени снизила детскую смертность. В целом эти изменения санитарных норм, возможностей общественного здравоохранения и вакцинации намного повысили вероятность долгой жизни. С увеличением продолжительности жизни умножились и возрастные заболевания, снижающие качество жизни в преклонном возрасте. И только недавно мы смогли увеличить продолжительность жизни за счет повышения качества лечения пожилых людей с сердечно-сосудистыми заболеваниями и раком.
Также приходится признать, что, хотя продолжительность жизни неуклонно возрастает, происходит это неравномерно. Улучшения пока касаются не всех – помимо развивающихся стран, “за бортом” остаются и некоторые группы населения Соединенных Штатов, исторически дискриминируемые[2]. К примеру, вопиющее исключение из общей тенденции к увеличению продолжительности жизни – показатель для чернокожих мужчин. Эпидемиолог Шерман Джеймс описывает эффект Джона Генри, при котором борьба человека с бытовыми трудностями сопровождается постоянным стрессом, приводящим к ускоренному накоплению возрастных заболеваний (болезней сердца, диабета и гипертензии) и преждевременной смерти[3]. Неравенство усугубилось во время пандемии COVID-19, когда национальные меньшинства (коренные американцы, латиноамериканцы и афроамериканцы) становились жертвой первой волны пандемии непропорционально чаще остальных[4], причем особенно часто умирали чернокожие мужчины, что привело к снижению показателя средней продолжительности жизни на два с половиной года.
В других демографических группах средняя продолжительность жизни, возможно, уже достигла максимального значения и теперь будет снижаться. Экономист и лауреат Нобелевской премии сэр Ангус Дитон и экономист Энн Кейс из Принстона в 2015 году показали, что в последние годы употребление алкоголя и наркотиков белыми американцами среднего возраста привело к увеличению числа случаев передозировки и самоубийств (“смертей от отчаяния”) и это стало причиной остановки роста средней продолжительности жизни и тенденции к ее снижению. В 2015 году Центр по контролю заболеваемости (CDC) объявил, что впервые за 22 года средняя продолжительность жизни американцев начала сокращаться, что связано с ростом смертности среди людей, не достигших 65 лет. Эйлин Кримминс из Университета Южной Калифорнии установила, что продолжительность жизни американцев коррелирует с их доходами[5]: в частности, в штатах с преобладающим влиянием демократов продолжительность жизни выше, что связано с более высокими доходами, менее выраженным неравенством и более эффективным здравоохранением, тогда как в республиканских штатах чаще встречаются случаи ожирения и нарушений обмена веществ, что снижает продолжительность жизни. Анализ результатов голосования и здоровья, проведенный в 2017 году, продемонстрировал, что показатели слабого здоровья (диабет, избыточное употребление спиртного, ожирение, недостаток физической активности) характерны для 43 % людей, голосовавших за Трампа[6].
Таким образом, мы уже знаем, как увеличить продолжительность жизни: улучшение профилактической медицины, прививки против детских заболеваний, сокращение неравенства, снижение распространения курения и ожирения, снижение уровня стресса и улучшение других аспектов образа жизни могут повысить современный показатель продолжительности жизни… однако эти изменения требуют не только индивидуальных действий, но и политических решений и инвестиций в социально-экономическую сферу в дополнение к таким основополагающим вещам, как равенство в доступности питания и наличие работы. К числу подобных инвестиций относятся усилия системы здравоохранения, направленные на всеобщую вакцинацию, воспитательные программы с разъяснением факторов риска и прекращение распространения наркотиков. В отношении последнего пункта наконец появились хорошие новости: попытки отслеживать употребление наркотических препаратов и ограничение их предписаний привели к снижению числа смертей, связанных с приемом опиоидов. Мы могли бы увеличить продолжительность жизни в США, если бы направляли больше усилий на сокращение неравенства.
В среднем женщины живут дольше мужчин, но одна опасность в жизни женщин, которой не существует для мужчин, заключается в рождении детей[4]. Беременность и роды несут в себе самый большой риск для здоровья женщин, что отражается в показателе материнской смертности, который определяется как смерть в результате беременности, наступившая в течение 42 дней после окончания беременности. Этот риск в значительной степени зависит от места проживания и частично от этнического происхождения. В целом материнская смертность сильно сократилась после 1950-х годов и в некоторых странах стала редкостью. Например, в Финляндии, Греции, Исландии и Польше этот показатель составляет 3 смерти на 100 тысяч родов, но в некоторых частях Африки он достигает нескольких сотен, и лидирует в этом списке Сьерра-Леоне – 1360 смертей на 100 тысяч родов[7]. Впрочем, материнская смертность остается проблемой не только в развивающихся странах. Соединенные Штаты отличаются весьма неприятным показателем материнской смертности[8] – таким же, как в Катаре, и выше, чем повсюду в Европе и других развитых странах. Более того, этот показатель вырос за последнее время от 7,2 смерти на 100 тысяч родов в 1987 году до 18 смертей в 2014-м.
Риск материнской смертности зависит от возраста женщины и описывается U-образной кривой: он минимален в двадцатилетнем возрасте. Во всем мире в группу максимального риска попадают молодые женщины, забеременевшие в возрасте от 10 до 14 лет, что в странах с “хрупкой системой здравоохранения” (по определению ВОЗ) связано еще и с другими медицинскими проблемами. Однако в США риск для этой возрастной группы может повышаться в связи с увеличением числа жертв изнасилований и запретом на аборты в некоторых штатах после принятия Верховным судом кошмарного решения об отмене постановления по делу “Роу против Уэйда” (постановление закрепляло право женщины на прерывание беременности). Конечно же, другие страны признают, что легальное прерывание беременности должно быть частью системы здравоохранения, и теперь аборты легализованы в Ирландии, Гибралтаре и Сан-Марино в Европе, а также в Мексике, Аргентине, Уругвае, Колумбии и Чили в Северной и Южной Америке, что привело к соответствующему снижению показателей материнской смертности[9]. В развитых странах главный фактор риска материнской смертности – старение: риск максимален для женщин старше 35 лет[10]. “Старородящие” (этот неприятный термин я услышала, когда была беременна первым ребенком в 38 лет) вносят значительный вклад в повышение показателя материнской смертности. Анализ, проведенный в округе Колумбия с 2008 по 2014 год, показал, что в группу самого высокого риска попадают женщины старше 40 лет: показатель материнской смертности для них составляет 142 смерти на 100 тысяч родов.
В значительной степени плохая статистика в США объясняется шокирующе высоким показателем материнской смертности среди чернокожих женщин: он в четыре раза выше соответствующего показателя для белых женщин, и часто смерти в таких случаях предшествует преэклампсия[5]. Данная проблема не объясняется только социально-экономическими факторами: сообщалось, что даже Серена Уильямс, одна из ведущих теннисисток мира, осталась без должного внимания врачей и чуть не умерла после родов; семикратная олимпийская чемпионка спринтер Эллисон Феликс тоже страдала от преэклампсии и вынуждена была родить ребенка на 32-й неделе беременности. Младенческая смертность и смертность чернокожих детей после хирургических операций соответствуют той же тенденции (обычно мужчины лучше восстанавливаются после операций, чем женщины). Хотя отчасти это может быть связано с различиями в некоторых факторах риска (повышенное артериальное давление, диабет, ожирение, возраст) и отчасти с различиями в пренатальной медицинской помощи, все же в какой-то степени тенденция объясняется недостаточным вниманием медицинского персонала к состоянию чернокожих женщин, разницей в количестве времени, уделяемого докторами чернокожим и белым пациентам, а также качеством медицинской помощи в больницах, которые по большей части обслуживают чернокожих пациентов. В некоторых штатах, таких как Калифорния, показатели материнской смертности улучшились благодаря более тщательному постродовому мониторингу, но для улучшения показателей в Соединенных Штатах в целом такие меры, а также высококачественное пренатальное медицинское обслуживание должны внедряться равномерно по всей стране.
Короче говоря, увеличение продолжительности жизни по-прежнему не сводится только к продлению жизни пожилых людей – здесь важно и улучшение показателей выживаемости детей и подростков, а в отношении женщин еще и обеспечение безопасной беременности и родов[6].
Достигли ли мы плато на кривой средней продолжительности жизни?
Поскольку мы уже знаем кое-что о том, как жить дольше, резонно задать вопрос: не достигли ли мы предела возможной продолжительности жизни? В 2016 году биолог Ян Вейг из Медицинского колледжа Альберта Эйнштейна и его коллеги вызвали горячие споры, заявив, что все больше людей доживают до ста, но мало кто живет дольше 115 лет, значит, видимо, 115 лет – предельный возраст человека[11]. Однако некоторые демографы быстро заметили, что эта оценка держится на единственном показателе: в модели учитывалась исключительная продолжительность жизни знаменитой французской сверхдолгожительницы Жанны Кальман, достигшей рекордного возраста 122 года[12]. Этот пример показывает, что иногда в печати появляются сомнительные и непроверенные научные данные, но еще – до какой степени людей интересует, сколько же может жить человек как биологический вид. Вскоре после заявления Вейга демограф Джеймс Ваупел с коллегами предположили, что смертность, то есть вероятность умереть в любой момент времени, на самом деле после 105 лет снижается[13]. Смысл такой, что после этого порога трудно предсказать момент смерти. И если учесть эти данные, непонятно, каков же максимальный предел долголетия.
Из рассуждений о “максимальной продолжительности жизни” выпадает один очень важный аспект: нынешние долгожители не пользовались современными возможностями влияния на молекулярные механизмы долгожительства, так что гипотетическая вероятность прожить “всего 115 лет”, реальна она или нет, не учитывает преимуществ антивозрастной медицины. Главная задача изучения молекулярных механизмов старения – создание препаратов для борьбы с возрастными заболеваниями. Исследования в области старения и долголетия нацелены на продление здорового существования, что приведет к превышению порога максимальной продолжительности жизни, о котором говорят современные демографы. И даже если мы достигли максимального значения, возможного при современном уровне терапевтических методов и лекарств, специалисты надеются сдвинуть этот показатель или хотя бы продолжительность здорового отрезка жизни в правильном направлении.
Этично ли изучать старение?
Люди проявляют огромный интерес к изучению старения и возможностям его замедления. Когда я начала проводить исследования в этой области, большинство людей, слышавших о моей работе, невероятно возбуждались и сразу понимали суть проблемы. Однако время от времени встречался кто-нибудь, кого идея изучения механизмов старения отталкивала по той причине, что манипулировать скоростью старения “неэтично”. Дискуссия на эту тему разгорается вновь и вновь (как минимум в социальных сетях) каждый раз, когда выясняется, что какой-то миллиардер из Кремниевой долины создал очередную компанию, занимающуюся проблемами долголетия, а иногда и специалисты в других областях науки говорят, что финансирование исследований старения – напрасная трата денег.
С одной стороны, заявления критиков понятны: в экстраполяции можно представить себе общество, в котором состоятельные люди никогда не стареют, поскольку могут пользоваться дорогими лекарствами “против смерти”, тогда как менее обеспеченные заболевают и умирают рано. Но давайте взглянем правде в глаза: в Соединенных Штатах эта проблема в какой-то степени существует уже сейчас из-за неравного доступа к медицинской помощи и медицинской страховке, что дает богатым более высокие шансы преодолеть почти любую болезнь и в результате жить дольше, как подтверждает работа Кримминс. Эту социально-экономическую проблему мы должны решить вне связи с возможностями увеличения продолжительности жизни.
Еще один довод против исследований старения предполагает дополнительный вклад в избыточный рост населения. Однако такое следствие кажется маловероятным, ведь рост продолжительности жизни не будет сопровождаться ростом рождаемости, так как коснется населения пострепродуктивного возраста (если только не ставится задача удлинения репродуктивного периода, см. главу 8, но и это не должно вызвать масштабного роста численности населения). Если бы мы научились излечивать всех больных раком, болезнями сердца и диабетом, это тоже привело бы к росту численности населения, однако большинству из нас показалось бы нелепым прекращать изучение этих болезней.
Наконец, существуют экономические проблемы, связанные с поддержкой стареющего населения, – в частности, рост числа пенсионеров. Однако задача большинства серьезных исследований в области старения – продлить здоровую жизнь[14]. В книге “Старение: преимущества долгожительства” Джей Ольшански и его коллеги утверждают, что удлинение здоровой жизни позволит сохранить средства, а не потратить[15]. Они полагают, что поддержание более долгой здоровой жизни уменьшит, а не увеличит нагрузку пожилого населения на экономику. В той же книге экономист Дана Голдштейн отмечает, что для учета такого демографического сдвига, возможно, потребуется изменить структуру нашей сегодняшней системы социального обеспечения[16], – то есть рассматривать экономические вопросы действительно придется. В любом случае бороться с неравенством в доступности медицинской помощи в современном мире необходимо, но это не научная проблема – мы уже знаем, как с ней бороться, теперь нужны политические решения.
Мы знаем, как жить дольше
Если задуматься об увеличении продолжительности жизни, придется признать, что мы уже знаем способы достижения полного жизненного потенциала. Большинство решений связаны со здоровым образом жизни: здоровое питание, достаточное количество физических упражнений и сна, профилактика и решение медицинских проблем, предотвращение избыточного стресса. И в этом отношении нам уже известен простой способ жить дольше: нужно быть богатым. Это неравенство часто выражается в том, что называют “выбором образа жизни” (и иногда морали), тогда как на самом деле выбор определяется экономическими факторами. К примеру, питание: всем известно, что для сохранения здоровья нужно есть больше овощей и фруктов, но они часто стоят дорого и не всегда доступны в “продовольственной пустыне” городов. Кроме того, богатые люди не меняют рацион питания в зависимости от месячной зарплаты. Физические упражнения – тоже роскошь: богатые люди могут хвастаться, сколько часов в неделю они уделяют спорту, как пробежали последний марафон или позанимались на велотренажере, но им не приходится заботиться о том, чтобы накормить детей. В социальных сетях они могут жаловаться на стресс, но, скорее всего, они не боятся, что на них нападут возле собственного дома. Им вряд ли приходится испытывать ежедневный стресс по поводу своих прав на работе и в школе и расспросов со стороны властей, в том числе полиции. Наконец, богатые люди часто проходят профилактические медицинские осмотры, имеют возможность решить медицинские проблемы до обращения в скорую помощь, и им не приходится выбирать, лечиться или нет. Это неравенство в доступности медицинской помощи оказывает долгосрочное влияние на продолжительность жизни. (Единственный неправильный выбор, который в последнее время делают некоторые состоятельные люди, – недоверие к преимуществам вакцинации, но при этом они эгоистично полагаются на популяционный иммунитет, так что вряд ли будут страдать от последствий своего решения.)
Кроме генетики, все эти элементы – питание, физические упражнения, сон, стресс и надлежащее медицинское обслуживание – являются главными факторами, определяющими продолжительность жизни. В дополнение к влиянию образа жизни так называемое взаимодействие генов и окружающей среды определяет, каким образом наше генетическое строение позволяет нашей биологии справляться с различными видами внешнего стресса, что тоже сказывается на продолжительности жизни. В лабораторных условиях с помощью модельных организмов мы обычно пытаемся воспроизвести оптимальные условия и поэтому часто не учитываем влияние стресса, вызванного экстремальным социально-экономическим неравенством. Но нужно признать, что наилучший способ для реализации максимального жизненного потенциала – быть богатым и находиться в привилегированном положении, имея возможность выбирать оптимальный для долголетия образ жизни.
Продление здорового отрезка жизни: снижение уровня заболеваемости
Нас часто спрашивают: “Не приведет ли удлинение жизни к тому, что люди будут дольше болеть?” Это возможно, но только если действовать неправильно. Вообще говоря, можно допустить, что сейчас мы как раз движемся неверным путем: пытаемся победить одну болезнь за другой, даем лекарства от одной болезни, потом от другой, вместо того чтобы повлиять на причину возрастных заболеваний, а именно – на старение. И поскольку пока мы не знаем, как предотвратить нейродегенеративные заболевания, мы поддерживаем здоровье тела, но не поддерживаем когнитивные функции, что ведет к потенциально катастрофическому увеличению числа людей с болезнью Альцгеймера и другими видами возрастной деменции. Неспособность фармацевтических компаний преодолеть эту проблему (мы видим, что они так и не находят средства от болезни Альцгеймера, сколько ни проводят клинических испытаний) означает, что решить задачу на сегодняшний день могут только академические лаборатории.
Одна из самых больших ошибок в восприятии исследований старения – полагать, будто мы пытаемся продлить только последний отрезок жизни, что, понятное дело, большинству людей не кажется привлекательным. Если я, рассказывая о своей работе, не показываю видео невероятно долго живущих маленьких червячков, большинство людей считают, что мы просто продлеваем последние этапы их жизни, но на записи видно, что червячки-долгожители – молодые и здоровые, а не дряхлые. Это долгоживущие мутанты с удлиненным здоровым отрезком жизни. Именно этого мы хотели бы добиться для людей – увеличить продолжительность здорового отрезка жизни. Главная задача исследований старения заключается, как выразился Джим Фрайс, в сокращении фазы болезней[17]. Идея в том, чтобы максимально продлить здоровый отрезок жизни, а затем быстро состариться, максимально укоротив “хрупкую” фазу. Полагаю, большинство людей признают, что это достойная цель исследований, поскольку все согласны, что от продления жизни без улучшения здоровья пользы мало. Действительно, в последнее время исследования в этой области сдвинулись от курса на достижение максимальной продолжительности жизни к развитию новых способов анализа здорового отрезка жизни – различных аспектов качества жизни, изменяющихся с возрастом. Изучение этой фазы здоровой жизни поможет нам одновременно увеличить продолжительность жизни и сократить фазу болезней и угасания[18]. В конечном итоге при исследовании старения нам следует изменить определение долгой жизни таким образом, чтобы включить в него условие высокого качества жизни. Вполне вероятно, что в результате этой работы мы продлим отрезок здоровой жизни, причем не только для самых богатых или для тех, кто озабочен долголетием, но и для всего населения в целом.
Как же мы будем это делать? Сначала нужно понять механизмы регуляции старения и долгожительства, а затем найти способы активации этих механизмов в организме человека. И в основном в этой книге я буду рассказывать о механизмах, которые не только увеличивают продолжительность жизни, но и улучшают здоровье.
Понятно, что это относится к беременному человеку любого пола, но в большинстве демографических исследований информация о беременности у мужчин еще не учитывается.
О влиянии пандемии SARS-CoV-2/COVID-19 на среднюю продолжительность жизни мы узнаем только через несколько лет, но первая волна заболевания снизила продолжительность жизни афроамериканцев мужского пола на два года; о влиянии следующих вариантов вируса мы узнаем позднее. В начале пандемии в большей степени пострадали пожилые люди (старше 65 лет), но демография смертности изменилась после появления вакцин: на момент распространения варианта “дельта” вакцинация людей старше 65 лет продвигалась значительно быстрее, чем вакцинация более молодых людей. В результате в последующие месяцы выросла смертность среди молодых людей, и общее количество смертей превысило показатель смертности от гриппа в 1918 году. В июне 2022 года журналист Дэвид Леонхардт предположил, что в результате усилий по проведению вакцинации среди людей африканского и испанского происхождения с одной стороны и отказа от вакцинации и использования масок среди белого населения (особенно республиканцев) с другой стороны разрыв в расовых показателях сократился, и показатели смертности, вероятно, изменились, поскольку смертность среди белого населения в середине 2022 года оказалась выше (David Leonhardt. 2022. “COVID and Race”. New York Times, The Morning, June 9, 2022, https://www.nytimes.com/2022/06/09/briefing/covid-race-deaths-america.html). Однако мы не знаем, насколько в этом исследовании учитывались возрастные показатели и не является ли это отражением парадокса Симпсона. На самом деле возможно, что черные американцы вообще живут недостаточно долго и не попадают в эти возрастные категории из-за многочисленных проявлений расового неравенства в обществе и в доступности медицинской помощи, не связанных с пандемией.
Эта книга создавалась во время пандемии SARS-CoV2, так что статистические данные пока недоступны, но в первых отчетах сообщалось о более высоких показателях смертности пожилых людей, особенно мужчин, в Китае. Пока неизвестно, подтвердится ли такая же статистика в других странах во всех возрастных группах.
Преэклампсия – опасное для жизни состояние, характеризующееся гипертензией и протеинурией. (Прим. перев.)
Крионика – технология замораживания тел или клеток человека и животных в надежде на возможное исцеление в будущем. (Прим. перев.)
Глава 2
Почему мы стареем?
Мы воспринимаем старение как естественную часть жизни, но, вообще говоря, почему мы должны стареть? Обязательно ли это? В этой главе я представлю старые и новые теории старения. На фундаментальном уровне старение представляет собой нарушение гомеостаза – неспособность устранять повреждения с такой скоростью, чтобы организм не изменялся со временем. Одна простая модель постулирует, что в процессе развития и в молодые годы организм затрачивает энергию, чтобы устранять повреждения для сохранения возможности воспроизводства; однако после завершения репродуктивного периода уже нет или почти нет эволюционного давления, предотвращающего ухудшение здоровья в результате повреждений, поэтому на репарацию расходуется меньше энергии, что ведет к накоплению повреждений, – это и есть старость. Необходимость реагировать на изменяющиеся внешние условия приводит к снижению скорости воспроизводства и параллельно к появлению механизмов удлинения жизни, что в определенных условиях обеспечивает более позднее воспроизводство. Следовательно, старение можно рассматривать не как результат отбора, а скорее как побочный продукт от прекращения поддержания здоровья организма после завершения репродукции. При обсуждении подходов к исследованиям старения полезно принимать во внимание представление о старении как о прекращении поддержания здоровья при потере репродуктивной способности, которое можно предотвратить или замедлить.
В конце 1990-х мне представилась возможность побывать на Кубе, и одним из самых удивительных впечатлений в Гаване для меня стало изобилие старых, ярко раскрашенных американских автомобилей. Эти реликвии 1950-х годов как будто остановили ход времени, по крайней мере на вид (после революции 1959-го Фидель Кастро запретил ввоз иностранной продукции). Забавно, что так много старых машин все еще бегали по дорогам, переживая починку и смену ценных деталей на протяжении многих лет. Судя по состоянию машин, их поддержание требовало времени и сил.
В отношении старения наши тела часто сравнивают со старыми машинами, постепенно разваливающимися со временем. Но это сравнение теряет смысл, когда вы понимаете, что мы затрачиваем энергию на репарацию наших клеток и способны регулировать скорость увядания посредством генетических механизмов. Наши клетки постоянно исправляют и заменяют поврежденные части, используя для этого энергию. При наличии соответствующей технологии мы можем научиться делать то же самое за счет активации естественных механизмов организма, с помощью лекарств, индуцирующих репарацию, или, быть может, путем замены клеток. В нескольких потрясающих работах последних лет было показано, что нам под силу замедлить или даже обратить некоторые аспекты старения. Например, ооциты червей “омолаживают” все свои белки непосредственно перед оплодотворением[1], так что новая яйцеклетка всегда свежая, вне зависимости от того, сколько времени она провела в материнской матке. Исследователи, изучающие старение, надеются, что в будущем мы сможем инженерным путем создавать новые части клеток для замены старых, что позволит восстанавливать функциональное тело – возможно, путем соединения и подгонки деталей, как в ярко раскрашенных старых американских машинах на Кубе.
Многих людей в отношении старения больше всего интересует вопрос, почему мы вообще должны стареть. Прежде всего замечу: наука хорошо умеет объяснять, как что-то происходит, но ответить на вопрос, почему что-то происходит, труднее: для установления причины нам нужно восстановить прошлое на основании экспериментально наблюдаемого настоящего, и такие выводы имеют естественные ограничения. По этой причине на протяжении многих лет разные теории старения появлялись, а затем исчезали по мере накопления новых данных[7]. Хотя моя книга скорее посвящена обсуждению наших современных знаний о молекулярных механизмах регуляции старения и продолжительности жизни, чем изложению эволюционных теорий старения, быстрый обзор этих теорий поможет понять, как такие механизмы могли развиваться.
Вместо того чтобы задавать вопрос, почему мы стареем, возможно, полезнее вывернуть вопрос наизнанку и спросить: а почему мы не должны стареть? Животные, как и все, что существует во вселенной, подчиняются второму началу термодинамики: общая энтропия изолированной системы со временем только увеличивается. Как поддержание чистоты в доме, так и сохранение здоровых функциональных клеток и генома требует работы. Без постоянной работы энтропия берет верх, а дальше, как вам известно, все приходит в беспорядок, и никто не знает, где что лежит (как у нас дома). Клетки потребляют энергию и используют ее для исправления повреждений и очистки, но им постоянно приходится бороться за поддержание порядка. Тот факт, что ограничение потребления калорий увеличивает продолжительность жизни, казалось бы, в таком контексте противоречит здравому смыслу, но дело в том, что клетки способны регулировать интенсивность своей функции (особенно синтез белка), снижая уровень повреждений и расход энергии на репарацию. Так же и мой дом оставался бы в чистоте, если бы остальные члены семьи отсутствовали и я неделю пробыла в доме одна.
Одна из наиболее понятных и давних теорий старения – простая модель “физического износа”. В таком ключе рассуждают о старой машине: чем больше ее используют и чем она старее, тем больше она изнашивается и тем чаще требуется ремонт. Известный физиолог Уолтер Кеннон, который во время Первой мировой войны спасал солдат, находившихся в состоянии шока (он добавлял им в кровь бикарбонат натрия для снижения кислотности), впервые выдвинул концепцию гомеостаза для описания своих наблюдений о механизмах поддержания функций и равновесия в организме. В упрощенном виде старение – это такое состояние, когда клетки не могут достаточно быстро исправлять повреждения. Потеря “клеточного гомеостаза” приводит к накоплению повреждений и – в конечном итоге – к клеточной дисфункции. На молекулярном уровне этот процесс проявляется, например, в окислительном повреждении белков и в мутациях ДНК.
Однако мы, в отличие от машин, не начинаем “терять стоимость” от активного использования и “стареть от момента рождения”, как принято утверждать. Я часто слушаю доклады на тему старения, и меня раздражает один слайд, который регулярно используют в начале доклада: изображение головы ребенка, потом взрослого человека, человека среднего возраста и старика. Этот рисунок подразумевает, что старение – непрерывный нисходящий процесс, начинающийся от рождения, и он не учитывает наших знаний из области биологии: клетки и ткани молодых людей прекрасно исправляют и заменяют сами себя для поддержания своей функции. Мы проходим несколько жизненных этапов, и, хотя трудно точно определить дату, когда мы “начинаем стереть”, мы не считаем, что подростки “старее”, чем дети в начальной школе. Генетические программы направляют развитие человека от подросткового до репродуктивного возраста. Мы развиваемся до взрослого возраста и только потом в какой-то момент начинаем стареть. (Если вам больше сорока, вы уже могли это заметить.) Повреждения накапливаются, но, судя по всему, накапливаются с разной скоростью у разных организмов и даже в одном и том же организме в разном возрасте. Следовательно, скорость старения регулируется каким-то более сложным образом.
Разные механизмы должны обеспечивать замену клеток молодого организма и репарацию существующих клеток, и умение управлять этими механизмами открыло бы перед нами большие возможности. Вообще говоря, на свете мало бессмертных организмов. Многие организмы, которые кажутся бессмертными, постоянно обновляют свои клетки. Можно сказать, что некоторые морские животные, плоские черви типа планарий и некоторые деревья “почти не стареют”, поскольку их клетки постоянно заменяются новыми. Эти организмы обновляют себя за счет активности стволовых клеток – “материнских” клеток, которые в результате деления могут дать начало клеткам любого типа. Разрежьте планарию на множество фрагментов, и из них вырастут целые новые животные, поскольку их стволовые клетки распределены по всему телу. Под влиянием стресса японская “бессмертная медуза” (Turritopsis dohrnii), по сути, обращает вспять процесс развития (как Бенджамин Баттон, Макс Тиволи[8] или Мерлин) и возвращается к ювенильному состоянию полипа в процессе “трансдифференцировки”. Это означает, что такие животные не являются поистине бессмертными, а поддерживают постоянство функций за счет производства новых клеток для замены старых. Давайте уточним: сохранение стволовых клеток является важнейшим условием и нашего с вами здоровья, они нужны нам для поддержания иммунной системы, мышц, кожи и даже головного мозга. Поиск возможностей использования стволовых клеток для предотвращения возрастных проблем – одно из главных направлений в исследованиях старения. Мы никогда не станем бессмертными, но можем попытаться понять и использовать приемы, с помощью которых сохраняются “бессмертные” животные.
Одним из первых, кто всерьез занялся изучением старения, был русский ученый Илья Мечников. Он был удостоен Нобелевской премии (в 1908 году) за открытие макрофагов и другие выдающиеся исследования в области иммунологии и микробиологии, и он же предложил термины “геронтология” и “танатология” (изучение смерти, а не персонажа комиксов Marvel). Он продемонстрировал роль иммунной системы и микробиоты в старении и возможность замедлять старение с помощью пробиотиков (см. главу 16). С его именем также связывают идею гормезиса (“Мой общий вывод из этих данных заключается в существовании логичного принципа, в соответствии с которым высшие элементы нашего тела могут усиливаться под воздействием малых доз подходящих цитотоксических сывороток”[2])[9], и его исследования стали одним из источников для формулировки теории программируемой смерти, которая на первый взгляд напоминает идею Августа Вейцмана о программируемости старения (но они по-разному отвечали на вопрос, является ли естественная смерть эволюционным преимуществом). По сути, Мечников был твердым сторонником борьбы со старением, поскольку полагал, что многие факторы, включая плохое питание, болезни и инфекции, способны укорачивать потенциальную продолжительность жизни человека. По этой причине его можно считать одним из основателей геронтологии и “науки о долголетии”, задача которых заключается в поиске практических методов замедления старения.
В 1928 году Раймонд Перл выдвинул теорию о скорости жизни, в основе которой лежит предположение, что конечность ресурсов является лимитирующим фактором продолжительности жизни: в таком ключе чем быстрее животное перерабатывает энергию, тем короче его жизнь. Эта идея соответствует общему наблюдению, что мыши живут меньше слонов, однако существуют животные такого же размера, как мыши, которые живут очень долго (например, летучие мыши или голые землекопы). Таким образом, летучие мыши и голый землекоп имеют очень высокий “коэффициент долголетия”[3], поскольку их продолжительность жизни намного больше, чем предсказывает их размер. Кроме того, эта теория не согласуется с наблюдением, что маленькие суетливые собачонки обычно живут дольше крупных собак.
Еще одна из ранних теорий старения, теория накопления мутаций, была предложена в 1952 году Питером Медаваром; она напоминает модель старения автомобиля и предполагает случайное накопление повреждений после завершения репродуктивного периода. На первый взгляд теория кажется разумной: большинство людей среднего возраста согласятся, что с какого-то момента системы организма начинают рассыпаться. Теория накопления мутаций предполагает, что после завершения репродуктивного периода уже не происходит отбора против возрастных проблем, в частности вызванных случайными мутациями, и поэтому они могут разрушать организм и вызывать старение. Медавар использовал аналогию со старыми пробирками: даже если пробирки не выглядят старыми, по прошествии достаточно длительного времени они разваливаются и распадаются случайным образом – как древний свадебный фарфоровый сервиз или машины на Кубе.
Теория антагонистической плейотропии была предложена Джорджем Уильямсом в 1957 году; она учитывает различие между ранними и поздними фазами жизни[4]. Уильямс предположил, что некоторые гены на ранних фазах жизни могут обеспечивать организму определенные преимущества (например, быстрое развитие и большое количество потомков), однако активность тех же генов в поздней фазе оказывает пагубное влияние и способствует возрастным изменениям. К числу таких факторов может относиться механизм, связывающий количество питательных веществ и скорость старения. (В ходе нашего обсуждения я приведу несколько примеров подобных моделей.) Теория антагонистической плейотропии лучше согласуется с наблюдением, что животные с меньшей продолжительностью жизни часто созревают быстрее и активнее воспроизводятся.
Заметим, Уильямс считал маловероятным, что мы “справимся со старением” и найдем отдельные причины или отдельные гены, влияющие на продолжительность жизни; “этот вывод говорит о том, что существование «источника молодости» невозможно с научной точки зрения”[5]. Конечно, как я расскажу позднее, открытие мутаций отдельных генов, приводящих к удвоению продолжительности жизни червей, а позднее и дрозофил, опровергает утверждение Уильямса о невозможности продления жизни[10][6]. Идея, что отдельные гены не способны влиять на продолжительность жизни, была настолько широко распространена, что на годы затормозила исследования процессов старения и ограничила понимание некоторых экспериментальных результатов (до сих пор часто повторяют, что отдельные гены не могут влиять на продолжительность жизни, хотя за 30 лет накопилось большое количество данных, опровергающих эту теорию). Как мы обсудим в последующих главах, есть особые мастер-гены, управляющие целыми каскадами нижестоящих генов и поэтому одновременно контролирующие работу сотен других генов, ни один из которых сам по себе не оказывает значительного влияния, – что соответствует теории Уильямса. Но все же отдельные гены могут быть важнейшими регуляторами продолжительности жизни. Теории, которые не принимают в расчет этот факт, устарели, и это следует разъяснять.
Шон Каррен, Гэри Равкан и другие исследователи решили проверить один из аспектов теории антагонистической плейотропии путем отключения генов после завершения фазы развития с помощью РНК-интерференции[7]. Они обнаружили, что отключение во взрослом возрасте многих важных и высококонсервативных генов (таких, без которых животные не могут нормально развиваться) на самом деле увеличивает продолжительность жизни. Почему это так? Анализ протеома показывает, что эти гены образуют избыточное количество связанных с возрастом агрегирующих белков[8], а эти белки с годами могут терять свою функцию и действовать как центры агрегации (вязкие комки, которые разрастаются и повреждают клетки), причиняющие вред. Конечно, отключение не любого важного гена приводит к увеличению продолжительности жизни, и не любой ген, обладающий антагонистическим плейотропным действием, критически важен, но анализ генов в более поздние годы жизни позволяет отличить их влияние от их функции в период развития.
Представлению о старении как о результате случайных повреждений противостоит гипотеза Михаила Благосклонного о “квазипрограммируемой” природе старения[9]. Его гипотезу квазипрограммируемой гиперфункции развития можно назвать механистическим расширением теории антагонистической плейотропии – некоей антагонистической плейотропией стероидов (честно говоря, я не уверена, что это принципиально отличается от гипотезы антагонистической плейотропии). Теория гиперфункции предполагает, что активность систем, задействованных в процессах развития, но ставших ненужными, постепенно приводит к повреждениям, в конечном итоге убивающим животное. Благосклонный приводит сравнение с ванной: представьте, что наполняете ванну водой, и если она заполнена, а кран все еще открыт, произойдет катастрофа (квазипрограммированное затопление квартиры). Он считает, что гиперфункция процессов развития у человека приводит к таким патологиям, как диабет, ожирение, опухоли, гипертензия и другие, – фактически ко всем проявлениям возрастных заболеваний. Можно предположить, что после завершения репродуктивного периода неполное отключение некоторых репродуктивных функций вызывает разрушительные последствия, описанные Благосклонным.
Эту теорию связывают с ранее описанным накоплением белков развития. В двух независимых исследованиях, посвященных изучению возрастных морфологических нарушений у C. elegans, Делия Гариган и Синтия Кеньон (в 2002 году) и Лаура Херндон и Моника Дрисколл (тоже в 2002-м) сообщали о постепенном накоплении в теле животных – особенно короткоживущих – связывающихся с липидами белков, называемых вителлогенинами, которые в норме содержатся в развивающихся ооцитах[10]. Это подтверждает идею о разрушительном влиянии пострепродуктивного накопления и агрегации таких липопротеинов в тканях, не имеющих отношения к репродукции, когда липиды больше не нужны или неправильно упаковываются в развивающихся яйцеклетках. Действительно, в нашей работе с Синтией Кеньон мы обнаружили (а другие ученые позднее подтвердили), что у долгоживущих мутантов синтез вителлогенинов подавляется, и снижение уровня этих белков, переносящих липиды, увеличивает продолжительность жизни[11]. Позднее было высказано предположение, что аномальное накопление вителлогенинов у стареющих червей после завершения репродуктивного периода служит примером квазипрограммируемой гиперфункции, о которой говорил Благосклонный: продолжение процессов развития с возрастом становится губительным для организма[12].
Одна из самых старых и популярных теорий старения (такая популярная, что никак не умрет!) гласит, что одним из главных факторов старения являются повреждения, вызванные действием активных форм кислорода (АФК). С наибольшей вероятностью именно об этой теории вы могли узнать из популярной литературы о старении. Один из зачинателей исследований молекулярных основ старения, Денхам Харман, впервые предложил свободнорадикальную теорию старения в 1956 году, и на протяжении десятилетий она оставалась доминирующей. Знаменитый химик из Калифорнийского технологического института, дважды лауреат Нобелевской премии Лайнус Полинг развивал следствия из этой теории, утверждая, что лучшее средство против старости – антиоксиданты. (Рассказывают, что Полинг поглощал мегадозы витамина С, как конфеты, и трудно установить, прожил ли он от этого дольше или нет, поскольку он умер в 93 года, а Харман – в 98 лет! Однако не проверяйте на себе, поскольку избыток витамина С просто выводится из организма, а прием чрезвычайно высоких доз способствует образованию камней в почках.)
Теория АФК была так широко распространена, что не подвергалась сомнению, и, честно говоря, в начале 2000-х годов, когда я начала заниматься вопросами старения, ее невозможно было обойти. В то время основная модель старения предполагала, что только супероксиддисмутаза (СОД) и каталаза – два фермента, которые действуют совместно и устраняют радикалы кислорода, ответственны за большую продолжительность жизни у долгоживущих животных и у животных с мутациями инсулиновых сигнальных путей (основных путей долгожительства) и что у долгоживущих мутантов усилена экспрессия генов этих ферментов[11]. Была популярна идея, что долгоживущий вариант C. elegans с мутантным геном daf-2, кодирующим рецептор инсулина/инсулиноподобного фактора роста, обязан своим долгожительством исключительно повышенной экспрессии гена супероксиддисмутазы sod-3[12]. Действительно, Хонда и Хонда показали, что экспрессия этого гена очень сильно повышена у животных с мутантным геном daf-2[13]. Супероксиддисмутазы работают в паре с каталазами, избавляя клетки от опасных супероксидных радикалов. Однако мы в экспериментах по изучению экспрессии генов долгоживущих червей с мутантным геном daf-2 с помощью микрочипов (см. главу 6) показали, что у этих животных повышена экспрессия сотен генов, а не только генов СОД и каталазы, и, следовательно, маловероятно, что за увеличение продолжительности жизни мутантов отвечает только пара ферментов СОД/каталаза. Еще важнее: за счет отключения функций отдельных генов мы установили, что каждый из этих активно экспрессируемых генов (в том числе генов СОД и каталазы) отвечает лишь за небольшое (5–10 %) увеличение продолжительности жизни мутанта. Для достижения невероятно долгой жизни мутанта daf-2 необходимо сложение активности всех этих генов, а не только генов антиоксидантов. Таким образом, победа над АФК – не единственный фактор, способствующий сохранению здоровья долгожителей с мутантным инсулиновым рецептором. (К сожалению, в нескольких статьях и обзорах, где упоминалась наша работа, говорилось, что мы подтвердили роль генов антиоксидантов в увеличении продолжительности жизни – поскольку они были в списке генов с повышенной экспрессией, но при этом ничего не говорилось о десятках других генов, которые оказывали такое же действие, и в результате смысл нашей работы полностью терялся.) И правда, в 2012 году Джереми ван Раамсдонк и Зигфрид Хекими показали, что при отключении всех пяти генов супероксиддисмутаз (sod-12345) черви становятся более чувствительными к стрессу, но в отсутствие стресса имеют нормальную продолжительность жизни[14]. Таким образом, хотя АФК могут быть частью проблемы, вряд ли они – единственная причина старения.
Тем не менее продолжают накапливаться данные в поддержку теории Хармана об АФК. Например, в 2010 году Стив Аустад и его студенты из Лаборатории морской биологии в Вудс-Хоуле во время курса по изучению старения провели сравнительное исследование двух видов моллюсков из одинаковой среды, но с разной продолжительностью жизни: необыкновенного долгожителя Arctica islandica (максимальная продолжительность жизни – до 400–500 лет!) и родственного моллюска Mercenaria mercenaria с небольшой продолжительностью жизни (“всего” 100 лет). Из их результатов следует, что в целом долгоживущий вид лучше справляется с окислительным стрессом[15]. Однако некоторые ткани оказались исключением из этого правила, и базовая антиоксидантная активность двух организмов была одинаковой, а это показывает, что устранение свободных радикалов – не единственная причина невероятного долгожительства Arctica islandica. Это исследование, как и многие другие, отчасти доказывает справедливость теории АФК, но не позволяет делать вывод, что защита от окислительного стресса – единственный механизм, обеспечивающий долгожительство. Рошель Баффенштейн (у нее в лаборатории занимаются изучением удивительно долгой жизни голых землекопов – подробнее см. в главе 4) обозначила это со всей ясностью в 2005 году в статье, озаглавленной “Антиоксиданты не объясняют различие в продолжительности жизни мыши и самого долгоживущего грызуна – голого землекопа”[16].
Теория АФК стала постепенно рассыпаться по мере накопления новых данных о том, что антиоксиданты не только не являются единственным источником долголетия, но в некоторых случаях наносят вред. Например, у мышей, получавших витамин С на протяжении 18 месяцев, подавлялась экспрессия некоторых антиоксидантных генов, таких как ген супероксиддисмутазы, и, возможно, именно поэтому они не жили дольше[17]. Антиоксиданты, включая те, на которые уповал Лайнус Полинг, способны наносить вред при применении в условиях легкого стресса, обычно удлиняющих жизнь; иными словами, животные, которым давали антиоксиданты в стрессовых условиях, хуже переживали этот период. Еще неприятнее тот факт, что среди здоровых молодых мужчин, занимавшихся физическими упражнениями на протяжении четырех недель и принимавших или не принимавших витамины C и E, пользу от упражнений получали только те, кто не принимал витамины![18] Не очень хорошая новость для производителей антиоксидантов. Все эти данные вкупе позволяют предположить, что некоторые окислительные повреждения бывают благотворными или как минимум необходимы для проявления других благотворных эффектов. Возможно, дело в том, что окислительное повреждение служит сигналом к проведению более обширной репарации.
Это подводит нас к концепции гормезиса, несколько в ницшеанском духе: условия стрессовые, но не убивающие животное, помогают ему жить дольше. Например, в лабораториях Тома Джонсона (в 2002 году) и Гордона Литгоу (в 2006-м) было показано, что повторяющиеся условия нелетального стресса на ранних этапах жизни, такие как окислительный стресс или тепловые импульсы, увеличивали продолжительность жизни C. elegans[19]. Получается, что небольшой стресс действительно усиливает выработку АФК, но эти соединения не вызывают повреждения, как утверждает теория, а усиливают реакцию животного на стресс, что увеличивает продолжительность жизни. Поначалу было принято думать, что это происходит за счет прямой активации стрессового ответа, но позднее выяснилось, что между внутриклеточными компонентами, особенно митохондриями, и клетками, индуцирующими гормезисный стрессовый ответ и передающими этот сигнал, существуют более сложные сигнальные пути. В лаборатории Майкла Ристоу в Политехнической школе Цюриха было показано, что применение антиоксидантов притупляет эти сигналы и в результате животные не вырабатывают такую реакцию на стресс, которая давала бы им защиту, а вместо этого умирают раньше.
Таким образом, несмотря на распространенность идеи о роли АФК в научной и популярной литературе и несомненный вклад АФК в некоторые аспекты старения, окислительные повреждения вряд ли являются единственной причиной старения. Более того, прием большого количества антиоксидантов вряд ли спасет нас, но может даже ослабить нашу способность справляться с некоторыми стрессовыми условиями. Тем не менее АФК и ответ на них действительно играют роль в регуляции продолжительности жизни, и нам нужно в этом разобраться.
Некоторые теории связывают продолжительность жизни с репродуктивной функцией. В 1979 году Томас Кирквуд выдвинул теорию одноразовой сомы, предположив, что ресурсы (то есть энергия) направляются либо на поддержание зародышевой линии, либо на поддержание сомы (остальных частей тела), но не на то и другое одновременно[20]. Привлекательна теория тем, что указывает на компромисс между долгожительством и воспроизводством, согласующийся с нашим интуитивным представлением о невозможности обладать всем. Идея о распределении ресурсов и компромиссе высказывается регулярно, и основные выводы этой модели в целом подтверждаются тем обстоятельством, что многие долгоживущие организмы лишь несколько раз производят крупное потомство, а не многократно мелкое – и, кроме того, многие условия, способствующие долгожительству, снижают репродуктивные показатели.
Теория одноразовой сомы предсказывает, что стерильность должна увеличивать продолжительность жизни – и тому есть несколько забавных подтверждений. Например, средняя продолжительность жизни корейских евнухов на 14 лет больше, чем у мужчин с таким же или близким социально-экономическим статусом[21], а среди кастратов численность людей, переживающих столетний юбилей, выше в 130 раз (хотя эти заявления оспаривались)[22]. Казалось бы, из этого следует, что стерильность увеличивает продолжительность жизни. Однако авторы исследований предлагают и второе объяснение: увеличение продолжительности жизни может быть связано со снижением выработки мужских гормонов – и в главе 9 мы подробнее обсудим это предположение, которое кажется более правдоподобным.
Синтия Кеньон и ее ученица Хонор Синь провели детальное исследование C. elegans как раз с целью ответить на вопрос: увеличивает ли стерильность продолжительность жизни? Хонор Синь начала работать в лаборатории Кеньон в Калифорнийском университете в Сан-Франциско еще подростком, пока получала домашнее образование. С помощью серии элегантных экспериментов, используя червей и узкий пучок лазерных лучей, они развенчали идею, будто стерильность является единственной причиной продления жизни.
Чтобы объяснить, что они сделали, я должна сказать несколько слов о раннем развитии C. elegans. На первой, личиночной стадии, называемой L1, у червя еще немного клеток зародышевой линии и гонад; вообще говоря, предшественниками клеток обоих типов являются всего четыре клетки: Z1, Z2, Z3 и Z4 (да, всего четыре!). Прелесть C. elegans в том, что все его клетки каждый раз развиваются одинаковым образом (так называемое стереотипное развитие). Все клетки C. elegans идентифицированы и имеют названия, что позволяет тщательно отслеживать их развитие. И поэтому мы знаем, во что превратится каждая клетка, и отчасти поэтому этот червь стал такой мощной генетической модельной системой. Две внутренние клетки, Z2 и Z3, в результате деления образуют пролиферирующие клетки зародышевой линии, тогда как внешние клетки, Z1 и Z4, являются предшественниками всех поддерживающих, не зародышевых клеток, которые называют соматическими гонадами.
Кеньон и Синь воспользовались простотой этого процесса, чтобы ответить на вопрос о влиянии стерильности. С помощью лазерного пучка они сжигали (убивали) клетки-предшественники, которые в норме должны были превратиться в зародышевые клетки (Z2 и Z3), и в результате получали червей с соматическими гонадами, но без клеток зародышевой линии. Удаление клеток зародышевой линии делало червей стерильными и намного увеличивало их продолжительность жизни. Казалось бы, это подтверждало, что ресурсы перенаправлялись от репродукции к соме, как и постулирует теория одноразовой сомы. Однако Кеньон и Синь провели еще один эксперимент: в отдельной группе червей они удалили еще и клетки, являющиеся предшественниками соматических гонад (Z1 и Z4), тем самым уничтожив как клетки зародышевой линии, так и клетки поддерживающих их окружающих тканей, так что у этих червей репродуктивная система не формировалась вовсе. Такие черви, не имевшие ни клеток зародышевой линии, ни поддерживающих соматических тканей, тоже были стерильными (и, следовательно, не расходовали энергию на воспроизводство), однако они не были долгожителями (илл. 1)[23].
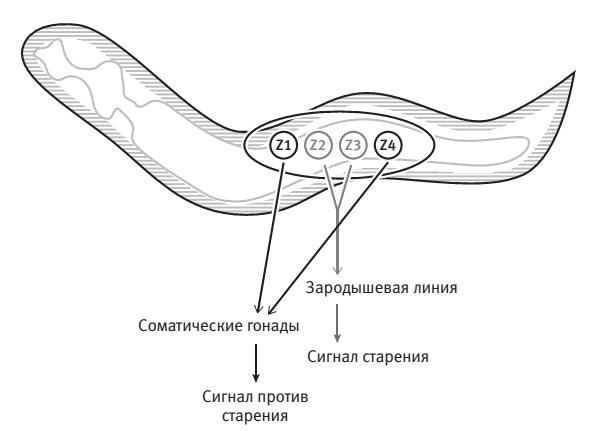
Илл. 1. Удаление клеток зародышевой линии или их предшественников (Z2 и Z3) делает червя C. elegansстерильным и долгоживущим, тогда как удаление одновременно соматических гонад и клеток зародышевой линии (всех четырех клеток-предшественников) делает животное стерильным при нормальной продолжительности жизни. На этом основании можно предположить, что зародышевые клетки и гонады посылают антагонистические сигналы, способствующие и препятствующие старению соответственно. Эти результаты также свидетельствуют против прямого механизма, который постулирует теория одноразовой сомы.
В результате Синь и Кеньон смогли отделить стерильность от долгожительства. Увеличение продолжительности жизни животных, лишенных клеток зародышевой линии, не может объясняться только перераспределением ресурсов, но скорее потерей сигнала, возможно исходящего от здоровых клеток зародышевой линии, который в норме способствует старению. На самом деле данные Синь и Кеньон позволяют предположить, что существуют два антагонистических сигнала: сигнал от клеток зародышевой линии способствует старению, а сигнал от соматических гонад – увеличению продолжительности жизни. В сумме равновесие этих сигналов – в зависимости от состояния клеток зародышевой линии и гонад – сообщает остальным частям сомы (телу), как долго животное будет жить. Когда нет клеток зародышевой линии, функционирует только сигнал долгожительства, и животное живет дольше. Когда нет обоих сигналов, продолжительность жизни нормальная. (А позднее в нашей лаборатории было показано, что спаривание максимально усиливает сигнал, способствующий старению[24].) Таким образом, какие-то элементы теории одноразовой сомы могут быть справедливы, но все не так однозначно, как предполагалось изначально: животные не направляют ресурсы напрямую на одну из функций, а следуют программам и сигналам, которые контролируют продолжительность жизни, как будто предвидя последующие репродуктивные нужды. В рамках такой модели предполагается, что контроль продолжительности жизни осуществляется с помощью гормональных сигналов, а не напрямую за счет отказа от воспроизводства и перераспределения ресурсов.
Следует отметить, что нам неизвестны долгоживущие мутанты или условия, в которых никак не затрагивается репродукция, а значит, обе функции каким-то образом связаны между собой, однако эта связь вовсе не обязательно причинная. Связь между воспроизводством и продолжительностью жизни, возможно, не столь непосредственна, как предполагает теория одноразовой сомы, поскольку существуют мутанты, которые живут очень долго (иногда в десять раз дольше обычного) и при этом с очень небольшой потерей репродуктивной способности, никоим образом не пропорциональной увеличению продолжительности жизни[13]. Более того, в 2002 году Эндрю Диллин и Синтия Кеньон показали, что снижение производства рецептора DAF-2 (рецептора инсулина/ИФР-1) только у взрослых червей – что позволяет избежать какого-либо влияния на развитие или репродукцию – по-прежнему удваивает продолжительность жизни[25]. Иными словами, черви с мутантным геном daf-2 могут жить дольше и при этом не обязательно производят менее многочисленное потомство. Эта работа, продемонстрировавшая отсутствие прямой связи между репродукцией и продолжительностью жизни, играет чрезвычайно важную роль в опровержении теории одноразовой сомы, но она не так хорошо известна в научной среде, как следовало бы. Этот вывод недавно был подтвержден в работе, выполненной в лаборатории Коллина Эвальда. Исследователи показали, что разрушение рецепторного белка DAF-2 после завершения репродуктивного периода увеличивает продолжительность жизни[26], что дополнительно подтверждает отсутствие прямой связи между продолжительностью жизни и репродукцией, о чем раньше уже сообщали Диллин и Кеньон. В нашей лаборатории недавно было показано, что некоторые черви, имеющие большое потомство и/или более длительный репродуктивный период, также живут дольше[27], и это еще раз подтверждает, что теория одноразовой сомы, возможно, неприменима к отдельным животным, но способность более длительного воспроизводства может быть связана с большей продолжительностью жизни, как показали Перлс и его коллеги в отношении женщин, рождающих детей относительно поздно[28]. Приведенные данные показывают, что нет абсолютной необходимости ослаблять воспроизводство или изменять сигнальные пути во время репродуктивного периода, чтобы увеличить продолжительность жизни. И это хорошая новость для большинства из нас!
Правда ли, что смерть животных “запрограммирована”?[29] Все мы слышали о стремительной кончине тихоокеанского лосося, который поднимается вверх по течению на сотни миль, чтобы отнереститься и умереть. Повышение уровня кортикостероидов у этих рыб приводит к подавлению функции иммунной системы, что, в свою очередь, вызывает быстрый отказ органов и смерть. Эти так называемые семельпарные животные размножаются один раз в жизни (воспроизводство “большим взрывом”), а затем умирают сразу после завершения процесса воспроизводства, что вполне можно считать примером запрограммированной смерти. Существование семельпарных видов поддерживается за счет производства большого количества детенышей при полном или почти полном отсутствии родительского воспитания (эта репродуктивная стратегия называется r-отбором), хотя самки лосося все же пытаются повысить шансы мальков на выживание, защищая кладку, пока не умрут. В случае лосося старение (или как минимум смерть), безусловно, можно назвать запрограммированным.
Еще одна теория, которая сначала расцвела, а потом угасла (и снова расцветает?), называется теорией группового отбора. Идея в том, что старение и последующая смерть особи приносят пользу всему племени, например, путем освобождения пространства и ресурсов для молодежи; более старые и больные животные с большей вероятностью достаются хищникам, что также благоприятствует молодым[30]. Это альтруистическое видение старения – решение проблемы перенаселенности в духе истории из фильма “Бегство Логана”[14]. Вероятно, польза группового отбора связана не с ограниченностью пищевых ресурсов, а с тем, что такой отбор служит механизмом для ускорения эволюции, например, за счет распространения генов, полезных не для отдельных особей, а для группы в целом[31]. В таком случае эволюционное преимущество может сказываться не так прямолинейно, как перераспределение ресурсов между особями разного возраста, но все равно благоприятствует молодым за счет устранения старых.
Я не эволюционный биолог, и мне кажется, что эту теорию чрезвычайно трудно проверить или отвергнуть; возможно, она справедлива, но мне непонятно, какая польза от нее может быть в большинстве ситуаций. Например, люди часто с уверенностью говорят, что старые черви должны умирать, чтобы молодым доставалось больше пищи. Звучит неплохо, но когда вы проводите эксперимент, вы понимаете, что большая часть пищи в любом случае съедается развивающейся молодью: после репродукции старые черви вообще почти не едят, так что их устранение не оказывает значительного влияния на доступность пищевых ресурсов – вне зависимости от того, умрут они через 15 дней или через 50. Однако наши эксперименты выполнены в лабораторных условиях при избытке пищи. Не исключено, что в природе при флуктуациях доступности пищи ситуация может быть иной. (Возможно, есть польза от того, что молодые черви поедают старых мертвых червей или развивающиеся на мертвых телах бактерии производят питательные компоненты для молодых, но в таком случае это опять-таки непрямое влияние.) Может быть, такой эффект выражен ярче у тех видов, которые уже живут в условиях пищевых ограничений и, что важнее, у которых старые особи поглощают значительную долю доступной пищи, так что их устранение действительно идет на пользу молодым. В таких условиях полезно ускорять развитие и максимально увеличивать репродукцию в благоприятные периоды.
Также важно учитывать влияние внешней среды и роль хищников. Классический пример влияния хищников на продолжительность жизни – разница между мышами и летучими мышами: два вида млекопитающих примерно одинакового размера с десятикратной разницей в продолжительности жизни (2–3 года и 30 лет). Раньше считалось, что разница эта главным образом объясняется способностью летучих мышей впадать в спячку. Однако исследователи из группы Стива Аустада отклонили это объяснение удивительно долгой жизни летучих мышей, поскольку, во-первых, не все долгоживущие летучие мыши впадают в спячку и, во-вторых, защитное влияние зимней спячки может объясняться просто отсутствием хищников[32]. Проследив за жизнью 19 видов зимующих млекопитающих, Тарбил с коллегами также пришли к заключению, что зимняя спячка сама по себе не обеспечивает бóльшую продолжительность жизни, даже если такие летучие мыши имеют максимальную продолжительность жизни по сравнению с другими видами животных того же размера[33]. Однако зимняя спячка связана с меньшим риском хищничества (меньшей вероятностью быть съеденным) и более медленным жизненным ритмом. Конечно же, еще одно важнейшее различие между двумя млекопитающими заключается в умении летучих мышей летать, поэтому выдвигается гипотеза, что бóльшая продолжительность жизни связана с умением ускользать от хищников. Способность избегать хищников может объяснять долгожительство вида при отсутствии необходимости быстрого воспроизводства, а это, в свою очередь, влияет на процесс старения. Конечно, переход от короткоживущих / имеющих большое потомство / бескрылых животных к долгоживущим / с небольшим потомством / крылатым животным мог быть довольно сложным в эволюционном плане, но он оказал значительное влияние на продолжительность жизни.
Вполне возможно, что отсутствие угрозы хищничества в значительной степени сказывается на продолжительности жизни и других животных, включая рыб и некоторых головоногих. По-видимому, у глубоководных осьминогов нет врагов[34], и они доживают до 20 лет, тогда как обитающие на мелководье осьминоги, лишившиеся защитной оболочки, имеют сравнительно небольшую продолжительность жизни (два года), несмотря на удивительный диапазон защитных приспособлений для камуфляжа и мимикрии. Резник с соавторами (2006) проверили влияние хищничества на разных этапах жизни рыб (в предрепродуктивном, репродуктивном и пострепродуктивном периодах), изучая рыбок гуппи (Poecilia reticulata) из водоемов в Тринидаде с разным количеством хищников[35]. Переселяя гуппи из водоемов с большим количеством хищников в условия с небольшим количеством хищников, они обнаружили, что вопреки предсказаниям смертность среди переселенных гуппи снижается как на начальных этапах, так и в более поздний период жизни, что обеспечивает более высокий показатель средней продолжительности жизни и более высокие показатели воспроизводства. Исследователи также выяснили, что все гуппи жили дольше после завершения репродуктивного периода. Таким образом, из результатов этой работы следует, что только продолжительность репродуктивного периода, которая напрямую влияет на приспособленность особи, подвергается отбору в соответствии с такими внешними факторами, как наличие хищников. (Дальнейшие исследования на диких животных, например червях или рыбах киллифиш, позволят проверить и другие теории о зависимости продолжительности жизни от экологических условий, а также об эволюции продолжительности жизни.)
Однако способность ускользать от хищников имеет предел. Как объясняет Шон Кэрролл в книге “Закон «джунглей»”, некоторые животные эволюционировали до больших размеров и в результате стали слишком велики для хищников[36]. Казалось бы, неплохая стратегия, но за размер приходится расплачиваться гораздо более высокой чувствительностью к изменениям доступности пищи. При ограниченности ресурсов важную роль играет умение адаптироваться к колебаниям доступности источников пищи за счет изменения репродуктивного развития.
Животные, никогда не выходившие из репродуктивной фазы жизни, поскольку погибали в зубах у хищников, никогда не старели. Так что вопрос должен звучать не “Почему мы должны стареть?”, а “Почему мы живем так долго после завершения репродуктивного периода?”. В эволюционном плане это сравнительно новая ситуация. Продолжительность жизни человека увеличилась лишь недавно, и лишь несколько видов животных продолжают жить по окончании репродуктивного периода. У человека эту ситуацию объясняют с помощью “гипотезы бабушек” – положительным влиянием бабушек на выживание внуков[37]. Идея в том, что бабушки, которые сами уже не производят потомство, но помогают выращивать и поддерживать внуков, улучшают эволюционную приспособленность своих потомков, и таким образом создается некое селективное давление для продления жизни женщин. Некоторые исследования подкрепляют эту гипотезу в отношении человека и крупных млекопитающих. Впрочем, мужчины живут всего на несколько лет меньше женщин, и, кроме того, существуют животные с аналогичным длительным периодом жизни после репродуктивного периода, которые совсем не занимаются выращиванием своего потомства. Поэтому возникает вопрос, насколько в действительности важна функция бабушек для регуляции продолжительности жизни у разных видов животных.
Несколько лет назад я занялась исследованием факторов, коррелирующих с продолжительностью пострепродуктивного периода жизни, и взяла себе в помощь студента. В ходе работы Джордж Малиха установил, что у млекопитающих продолжительность жизни в пострепродуктивном периоде пропорциональна отношению массы тела детеныша к массе тела матери[38]. Иными словами, чем крупнее детеныш, тем дольше будет жить мать после окончания репродуктивного периода. Напротив, животные, производящие крохотных детенышей, по-видимому, способны воспроизводиться даже в старости, а затем быстро дряхлеют и умирают, то есть продолжительность жизни после завершения репродуктивного периода у них невелика.
Например, некоторые виды морских ежей могут жить несколько десятилетий и даже столетий[39]. Эти колючие шарики с ножками-трубочками достигают порой довольно крупных размеров и воспроизводятся путем выделения в воду микроскопических яйцеклеток и сперматозоидов, которые затем встречаются друг с другом вне тел родителей. Морские ежи размножаются фактически до самой смерти и в результате имеют очень короткий (почти нулевой) отрезок жизни после завершения репродуктивного периода. Напротив, матери, дающие жизнь сравнительно крупным детенышам, после завершения репродуктивного периода живут долго. В этом есть определенная логика, поскольку для рождения очень крупного потомка мать должна быть в хорошей физической форме и, следовательно, после родов сохраняет “остаточное здоровье”, обеспечивающее более долгую жизнь. В частности, эволюция привела к тому, что новорожденный человек имеет сравнительно крупную голову по отношению к размеру тела матери; эволюция крупной головы коррелирует с развитием крупного мозга, но цена этого – вероятность гибели матери при родах. Тот факт, что продолжительность жизни многих видов животных после завершения репродуктивного периода растет с увеличением отношения размеров тел ребенка и матери, означает, что для объяснения продолжительного пострепродуктивного периода не нужно привлекать гипотезу бабушек. И это хорошо, поскольку мы видим, что гермафродит C. elegans долго живет после появления на свет всего потомства, и при этом черви не занимаются воспитанием детей, а уж тем более внуков. Конечно, это не означает, что гипотеза бабушек полностью ошибочна, но она может свидетельствовать о каких-то изменениях на фоне другого, более значительного биологического явления, которое по другим причинам уже привело к удлинению отрезка жизни после завершения репродуктивного периода.
Демограф Аннет Бодиш (Институт демографических исследований Макса Планка) создала модель для изучения того, как влияет продление жизни после завершения репродуктивного периода на скорость накопления (или фиксации) мутаций, тем самым отрицая предположение, что пострепродуктивный период не влияет на продолжительность жизни. Напротив, ее модель предполагает, что полезные мутации с большей вероятностью закрепятся в популяции с более длительным пострепродуктивным периодом жизни[40]. Иными словами, не только репродукция, но и продолжительность репродуктивного периода и момент смерти могут эволюционировать в ответ на селективное давление – возможно, это новый аспект влияния длительности пострепродуктивного периода на эволюцию старения.
Однажды, только начиная работать в Принстоне, я выступала там с докладом, в основном касавшимся моих исследований экспрессии генов у долгоживущих животных (см. главу 6) и нашего нового проекта по использованию червей для изучения возрастных нарушений когнитивной функции (глава 16). Когда слушатели начали задавать вопросы, один эволюционный биолог поднял руку и заявил, что мои результаты ошибочны (таков был смысл его высказывания), поскольку отбор долгожительства невозможен. Это заявление меня ошеломило, отчасти потому, что долгожительство не было главной темой моего доклада, отчасти – поскольку во вступлении я рассказала слушателям, что черви с мутациями инсулиновых сигнальных путей действительно живут дольше, так что я не видела здесь противоречия. Вскоре стало ясно, что он пришел на мой доклад главным образом с целью сообщить мне, что все результаты в данной области исследований за последние десять лет были неверными. Я ответила, что невозможно отрицать существование мутантов с единственным измененным геном и с сильно увеличенной продолжительностью жизни, вне зависимости от теоретических рассуждений о том, должны они существовать или нет. Более того, эти гены и их влияние на продолжительность жизни консервативны в эволюционном плане, так что это не какое-то странное явление, касающееся только червей. Совершенно очевидно, его не устраивало, что открытие всех мутаций единичных генов червей и дрозофил, связанных с долгожительством, не согласуется с простой теорией Уильямса.
Однако всегда полезно пересмотреть теорию, если появляются противоречащие ей данные. По-видимому, лучше всего наши наблюдения согласуются с теорией регулируемой программы старения. Ее суть в том, что животное иногда вынуждено реагировать на изменяющиеся внешние условия (например, голод) и соответствующим образом подстраивать течение жизни (рост, воспроизводство, продолжительность жизни). Эволюционный биолог был абсолютно прав в том, что никакой отбор после завершения репродуктивного периода невозможен, так что сама по себе продолжительность жизни не является признаком, который может эволюционировать за счет отбора. Вероятно, он реагировал в большей степени не на мой доклад, а на популярное заявление, что существует некая “программа”, задача которой заключается в увеличении продолжительности жизни, и он, вероятно, удивился бы, если бы узнал, что я с ним согласна. Как мы увидим далее, гены, увеличивающие продолжительность жизни, играют важную роль в регуляции других функций, которые могут подлежать отбору, в том числе способности реагировать на доступность пищи для корректировки развития и воспроизводства. Мутации инсулиновых сигнальных путей и пищевые ограничения увеличивают продолжительность жизни и усиливают воспроизводство, что, кажется, противоречит теории одноразовой сомы и невозможности эволюционного отбора продолжительности жизни, но согласуется с представлением о том, что показатели воспроизводства и его временные рамки настраиваются в соответствии с доступностью питательных ресурсов. Пред- и пострепродуктивный период жизни важно выделять и при учете влияния внешних факторов смертности (главный фактор – хищники) в разные периоды жизни, как в примере с гуппи в прудах с разным количеством хищников.
Все эти данные приобретают больше смысла, если рассматривать их в контексте регуляции воспроизводства в ответ на изменение доступности пищи: животные корректируют скорость воспроизводства для оптимального использования пищевых ресурсов, когда они есть, и снижают ее, когда пищи недостаточно. Все эти концепции можно совместить путем одного простого допущения: старение и долгожительство следует рассматривать не как основную задачу животного, а как побочный эффект пострепродуктивного выживания – и, что важно, этот эффект модулируется. Отбору подвергается не долгожительство, а воспроизводство; факторы или сигналы, влияющие на продолжительность жизни, отбираются в первую очередь для оптимизации воспроизводства. Следует говорить не о программах, склоняющих животное к принятию того или иного решения для регуляции продолжительности жизни, а о важных регуляторах, обеспечивающих пластичность – способность гибко реагировать на изменение условий для поддержания воспроизводства.
Оптимизация не всегда означает максимально быстрое рождение потомства: если пищи недостаточно, нет никакого смысла производить детенышей, поскольку они умрут от голода, – следовательно, процесс воспроизводства нужно затормозить. Замедление воспроизводства имеет смысл при соблюдении двух условий: 1) животное сохраняет качество клеток зародышевой линии, так что при возобновлении воспроизводства появится здоровое потомство; 2) животное сохраняет соматические ткани, чтобы при возобновлении воспроизводства мать не умерла до успешных родов. Именно второе условие, заключающееся в поддержании соматических тканей, имеет отношение к продолжительности жизни. Таким образом, для животного важна связь между двумя системами, даже если “отбору” подвергается только репродукция.
Еще один важный аспект, который необходимо учесть: мы говорим об открытой системе. Если есть питательные вещества, энергия может использоваться для поддержания и репарации тканей, по крайней мере пока работают системы поддержания и репарации. В репродуктивной фазе могут действовать сигналы для поддержания и репарации тканей – как зародышевых, так и соматических. Когда воспроизводство завершено, системе больше не требуется поддерживать ни одни ни другие, однако животные с наилучшим состоянием соматических тканей на момент завершения репродуктивного периода после этого проживут дольше, что и подтверждает анализ продолжительности пострепродуктивного периода у многих видов животных.
Как в ходе эволюции возникла такая система настройки? Мы уже упомянули зимнюю спячку, но вы догадываетесь, что существуют и более гибкие механизмы изменения метаболизма в ответ на ограничение доступности пищи, определяющие “скорость” функционирования животных. Если сохраняются неоптимальные условия существования, животное, способное замедлять метаболизм в трудные времена, может одержать победу за несколько поколений, даже если не научится развиваться быстрее всех или производить самое многочисленное потомство. Но если условия стабильные и пища в достатке, в популяции начнут преобладать животные, которые быстрее развиваются и дают более многочисленное потомство. Изменяющиеся условия благоприятствуют распространению животных, способных лучше других реагировать на любые изменения. С учетом этих замечаний легко понять, как мог происходить отбор механизмов, позволяющих использовать сигналы о доступности пищи для настройки скорости метаболизма, поскольку животные, обладающие такими системами, способны делать правильный выбор в любое время. Некоторые животные довели это умение до крайности, например впадают в спячку или переходят в состояние диапаузы (вроде спор), но у нас с ними одинаковые системы метаболической регуляции. Другим чрезвычайно ярким примером подобной метаболической настройки служат общественные насекомые, такие как муравьи и пчелы, у которых есть “касты”, выполняющие в колонии разные социальные функции: королева и рабочая особь в одной и той же колонии имеют одинаковую генетическую основу, но продолжительность их жизни совсем разная (годы и недели соответственно) ввиду разной метаболической программы и распределения ролей. Настройка параметров истории жизни позволяет животным лучше приспосабливаться и выживать в конкретных условиях среды.
Таким образом, мой недовольный коллега был одновременно прав и неправ. И нам стоит пересмотреть наши представления о продолжительности жизни и согласовать наши теории с реальными данными. Результаты одной интересной работы с мышами позволяют предположить, что некоторые манипуляции на поздних этапах жизни благотворно сказываются на здоровье животных, особенно самок[41]. В отношении человека вопрос на миллион долларов все еще звучит так: можем ли мы действительно как-то влиять на продолжительность жизни после завершения репродуктивного периода?
В итоге, если черви могут жить в два или даже в три раза дольше обычного просто в результате изменения функции рецептора инсулина/ИФР-1, почему не бывает “мутантных” людей, живущих до 250 лет? На самом деле люди уже живут довольно долго; с ростом средней продолжительности жизни выросла и максимальная. Все еще ведутся споры относительно максимально возможного срока жизни (и недавняя оценка порогового значения 115 лет была решительно отвергнута – см. главу 1), однако поскольку после какого-то возраста коэффициент смертности начинает выравниваться, маловероятно, что люди вскоре смогут доживать до 250 лет без серьезного медицинского вмешательства. Почему это так? Что удерживает нас в этих рамках?
Концепция ограниченной толерантности дает одно возможное объяснение. Мы доживаем до взрослого возраста только за счет развития в соответствующее время. Мутации, которые могли бы удваивать нашу продолжительность жизни, вполне вероятно, так сильно замедляли бы наше развитие, что мы никогда не достигали бы взрослого возраста[15]. Даже у C. elegans сильные мутации, почти полностью блокирующие сигнальные пути инсулина/ИФР-1, останавливают развитие червей на первой, личиночной фазе или фиксируют их в состоянии диапаузы; и такие мутанты, конечно же, никогда не выиграют борьбу за выживание в дикой природе. Люди с синдромом Ларона, который вызван нарушением сигнальных путей с участием ИФР-1[42], отличаются карликовостью и другими дефектами, но редко умирают от рака и иных возрастных заболеваний. Очевидно, что мы не можем сильно изменять пути инсулина/ИФР-1, особенно в процессе развития, не влияя негативным образом на другие показатели качества жизни, кроме ее продолжительности.
Еще один фактор, объясняющий ограниченную толерантность, – температура. В отличие от беспозвоночных и холоднокровных животных, которые вынуждены подстраиваться под внешние условия, мы поддерживаем внутреннюю температуру тела. И это требование в значительной степени снижает нашу метаболическую пластичность, ограничивая допустимый диапазон метаболических вариаций. Способность тела вырабатывать тепло за счет сжигания бурого жира строго регулируется и реализуется только на самых ранних этапах развития, возможно из-за большой энергетической стоимости процесса. Именно поэтому идея о переводе белого жира в бурый у взрослых людей с целью снижения массы тела, например за счет “митохондриальных разобщителей”, вызывает возбуждение публики. Такие препараты безрецептурного доступа, как 2,4-динитрофенол (ДНФ) и фен-фен, имеют печальную историю и теперь запрещены из-за токсического эффекта. Это не удивительно, учитывая тревожную информацию о воздействии ДНФ: было замечено, что многие рабочие на французских военных заводах, где ДНФ использовали для изготовления взрывчатых веществ, страдали от потери веса, избыточной потливости, повышенной температуры тела (почти до 42 градусов!) и часто умирали. Нарушение регуляции термогенеза убивает нас, как перегрев, так что температурные механизмы влияния на продолжительность жизни можно использовать только в ограниченных пределах.
Наконец, мы вынуждены признать, что даже в модельных системах может иметь место расхождение между естественными процессами и тем, что мы наблюдаем в лабораторных условиях при работе с мутантными организмами. Не исключено, что в природе даже C. elegans живут не так долго. Долгоживущие мутанты процветают в лабораториях, но по описанным выше причинам, возможно, никогда не встречаются в природе. В природных условиях они не могут конкурировать с червями “дикого типа”[16] (обычными червями), которые лучше переживают изменения условий окружающей среды, тогда как мутанты-долгожители зафиксированы в одном состоянии. Иными словами, отсутствие способности изменяться в ответ на изменения внешней среды в дикой природе является недостатком. Но все это не означает, что информация о долгоживущих мутантах бесполезна для человека. Скорее всего, у этих экстремальных мутантов изменены те же самые гены, которые необходимо будет модифицировать по достижении взрослого возраста, когда закончено развитие и воспроизводство, чтобы добиться такого же эффекта продления жизни у человека. Возможно, ответ заключается в небольших вариациях генов, как в случае однонуклеотидных полиморфизмов (SNP), которые выявляют методом полногеномного поиска ассоциаций (genome-wide association studies, GWAS); вообще говоря, изучение геномов людей, доживших до 100 лет, позволяет сделать именно такой вывод: минимальные изменения функции генов белков, участвующих в сигнальных путях инсулина/ИФР-1, могут увеличивать продолжительность жизни[43].
На вопрос “Почему мы должны стареть?” мы сможем ответить лучше, если глубже на молекулярном уровне поймем этот переход от развития к поддержанию организма, а затем к потере гомеостаза по мере старения. Хотя Добржанский правильно заметил, что “в биологии все имеет смысл только в свете эволюции”, мы лучше поймем пути, по которым шла эволюция, если идентифицируем общие молекулярные и сигнальные пути, регулирующие продолжительность жизни у разных животных[44]. Вообще говоря, понимание механизмов долгожительства на молекулярном уровне уже позволило отказаться от нескольких самых старых и популярных эволюционных теорий старения. Нам следует корректировать теории с учетом новых данных, а не наоборот. Судя по всему, для поиска ответа на вопрос, почему мы стареем, сначала нужно понять, как мы стареем, а это поможет понять, как замедлить этот процесс. Чтобы ответить на все эти вопросы, надо проанализировать суть процессов на молекулярном уровне – как увидеть, что происходит под капотом кубинских автомобилей.
Мутанты и гены C. elegans обычно получают названия в связи со своими признаками (фенотипом) и пишутся курсивом. Так, daf означает, что у мутанта нарушен переход к состоянию торможения, диапаузы (defective for proper formation of dauers). Мутанты daf либо переходят в диапаузу в неположенное время, как в случае daf-2, либо не переходят в положенное время, как daf-16.
Работы, выполненные на гермафродитах C. elegans, могут приводить к ошибочным выводам, если не производится спаривание гермафродитов с самцами. Дело в том, что количество потомков у гермафродитов ограничено количеством спермы, производимой самим животным до его переключения на производство ооцитов. Однако животные все еще имеют избыток ооцитов, которые они могут использовать при спаривании с самцом, и это позволяет рассчитать общее количество потомков. Поскольку потомство от собственных сперматозоидов не отражает общего репродуктивного потенциала животного, такие данные не следует использовать для интерпретации связи между количеством потомков и продолжительностью жизни, однако их довольно часто приводят как подтверждение теории одноразовой сомы.
Рассказываю молодым: фильм “Бегство Логана” (Майкл Андерсон, 1976) – антиутопия о мире, где из-за недостаточности ресурсов все люди, достигавшие тридцатилетнего возраста, подлежали уничтожению; сюжет фильма основан на одноименном романе-комиксе Уильяма Нолана и Джорджа Клейтона Джонсона, выпущенном в 1967 году.
Медицине известны случаи мутаций, когда развитие полностью останавливается примерно в двухлетнем возрасте.
Следует отметить: при наличии “тяжелых” версий генов (аллелей) мутанты развиваются медленно, что согласуется с теорией антагонистической плейотропии. Но после фазы развития эти аллели можно отключить, и это все равно увеличит продолжительность жизни.
На самом деле статья в журнале Nature, где говорилось, что потеря sod-3 полностью отменяет увеличение продолжительности жизни долгоживущих червей C. elegans с мутантным геном daf-2, кодирующим рецептор инсулина/инсулиноподобного фактора роста, была отозвана, когда выяснилось, что “двойной мутант” не содержал мутаций ни daf-2, ни sod-3, то есть это был организм дикого типа с обычной продолжительностью жизни! Неловко получилось.
В биологии диким типом называют самый распространенный вариант признака или гена в популяции. (Прим. науч. ред.)
Бенджамин Баттон – герой американского фильма 2008 года “Загадочная история Бенджамина Баттона”; Макс Тиволи – герой романа Эндрю Шона Грира “Невероятная история Макса Тиволи”. (Прим. перев.)
Для более подробного изучения рекомендую книгу: Steven Austad. Why We Age. New York: John Wiley, 1996.
Концепция гормезиса предполагает, что нелетальный стресс вызывает иммунный ответ, который в конечном итоге способствует усилению организма.
Глава 3
Генетика долгожительства у человека.
Чему мы можем научиться у людей, живущих до 100 лет?
Никакой другой вопрос на свете так не замутнен тщеславием, обманом, фальсификациями и преднамеренным мошенничеством, как предел человеческого долголетия.
Книга рекордов Гиннеса, 1984
Примерно раз в год появляется новый претендент на самое смертельное в мире звание самого старого человека на Земле. Пока я писала книгу, звание удерживала японка Канэ Танака, которой было 119 лет. Танака принадлежит к постепенно разрастающемуся сообществу исключительных долгожителей, или супердолгожителей, возраст которых превысил 110 лет. Конечно, в оценках максимальной продолжительности жизни много неясностей, поскольку сто лет назад рождение людей в разных уголках Земли зачастую никак не регистрировалось. В результате у некоторых народов появлялись легенды о людях, проживших невероятно долгую жизнь. Например, утверждалось, что индонезийцу по имени Содимеджо, также известному как Дедушка Готто, на момент смерти в 2017 году было 146 лет, однако, понятное дело, нет никаких документов, подтверждающих это заявление. Но уже есть много примеров, когда люди (особенно женщины) с достоверной датой рождения живут больше 110 лет.
Наверное, самая известная среди всех супердолгожителей – француженка Жанна Кальман, дожившая до 122 лет и пережившая даже своего адвоката, который на протяжении 30 лет платил ей деньги в расчете, что после ее смерти сможет жить в ее квартире. Замечу между делом: пока я писала книгу, российский математик Николай Зак выдвинул предположение, что невероятно древний возраст Кальман – результат мошенничества со стороны ее дочери Ивонны, не желавшей платить налог на наследство после смерти Жанны (которую зарегистрировали как смерть Ивонны) в 1934 году[1]. Зак считает, что подмена была произведена с целью обмануть не демографов, а налоговые органы. Тем не менее Ивонна, которая была на 23 года младше матери, прожила такую долгую жизнь (либо 99 лет, либо 122 года, если она и в самом деле была Жанной), что стала национальным достоянием французов как “самый старый человек в мире”, и раскрыть правду было уже слишком неудобно. В подтверждение своей гипотезы Зак представляет несколько вполне убедительных фотодокументов, исторических фактов и свидетельств, но также делает некоторые сомнительные заявления – например, отмечает пикантные подробности о совместном воспитании сына Ивонны “Жанной” и ее “зятем” (что он считает одним из самых ярких обвинительных доказательств). Эта история до сих пор вызывает дискуссии (некоторые утверждают, что Зак ошибается и Жанна действительно прожила 122 года), но следует отметить, что, даже если Жанна Кальман не может носить звание главного долгожителя, это место заняла Канэ Танака, поскольку ее поразительный возраст 119 лет не подвергается сомнению.
Споры о максимальной продолжительности человеческой жизни все еще продолжаются. В какой-то степени этим спорам способствовала публикация в журнале Nature широко известной статьи, в которой говорилось, что максимально возможный возраст человека составляет 115 лет[2]. Как я отмечала выше, этот анализ учитывает только современное состояние дел, то есть продолжительность жизни без каких-либо специфических манипуляций для ее увеличения, а лишь при нынешних возможностях медицины, и это не означает, что мы никогда не сможем жить дольше при появлении новых возможностей. В любом случае авторы статьи предполагали, что мы уже достигли максимальной продолжительности жизни: они использовали возраст Кальман на момент ее смерти в качестве крайней точки, что повлияло на характер всей зависимости с плато на уровне 115 лет.
Заявление Вейга о “стопятнадцатилетнем максимуме” вызвало волну комментариев и несколько писем с опровержением[3]. Некоторые указывали, что в исследовании использовались единственная точка, соответствовавшая возрасту Жанны Кальман – 122 года в 1997 году, и странный “дробный” подход, в рамках которого все данные рассматривались не как единое целое, а разбивались на две группы, что сдвигало регрессию и заставило авторов определить максимальную продолжительность жизни на уровне 115 лет. В моем любимом комментарии группа исследователей проиллюстрировала недостаток этого анализа на примере прыжков в длину[4]. Используя такой же “дробный” подход (а именно, оценку максимального ежегодного показателя длины прыжка отдельно после рекордного прыжка Майка Пауэлла в 1991 году и до него, вместо того чтобы объединить все данные начиная с 1960 года в единый массив), они показали, что этот метод анализа приводит к ошибочному выводу о снижении показателей прыгунов с течением времени. Прочтите еще раз: следуя такому аналитическому методу, мы приходим к заключению, что после 1991 года спортсмены стали хуже прыгать в длину – из-за исключительного достижения Майка Пауэлла. Конечно же, это смехотворный вывод. На самом деле с 1960-х годов происходит неуклонный рост показателей, а результаты Боба Бимона и Пауэлла были выбросами, как и уникальная продолжительность жизни Жанны Кальман. Кроме того, рост количества очень старых людей в таких странах, как Япония, предполагает, что мы пока не знаем максимально возможной продолжительности человеческой жизни и она, судя по всему, еще не достигнута. Позднее Джеймс Ваупел с коллегами выдвинули еще одно спорное предположение, что смертность (то есть вероятность умереть) вопреки ожиданиям перестает расти около 105 лет, а не продолжает увеличиваться с возрастом[5]. Это означает, что, если человек доживает до 105 лет, дальше риск смерти не увеличивается. Таким образом, с увеличением популяции столетних людей увеличивается и вероятность появления все большего количества людей, доживающих до 115 лет.
Так в чем же секрет супердолгожителей? Трудно сказать, какой практический совет можно извлечь из историй этих людей, поскольку их опыт по определению является исключительным, то есть статистически незначимым, и они знают только то, что делали сами, так что это ни в коем случае нельзя назвать контролируемым экспериментом. Хотя многие долгожители объясняют свою продолжительность жизни употреблением специфических продуктов и напитков, из описания их питания и образа жизни нельзя вывести никаких состоятельных заключений, кроме, пожалуй, удивительно частого упоминания алкоголя и “избегания мужчин”, что, возможно, лишь бытовой аспект, поскольку большинство супердолгожительниц намного пережили своих сверстников мужского пола. Вообще говоря, десять первых женщин из списка долгожительниц пережили всех долгожителей среди мужчин; номер 10 в этом списке, Мисао Окава, прожила более 117 лет, тогда как проживший дольше всех мужчина Дзироэмон Кимура умер в возрасте 116 лет.
Один важный аспект, который может показаться очевидным, но который все же необходимо подтвердить, заключается в том, что долгожители – здоровые люди. Этот вопрос находится в центре исследований старения, поскольку бытует мнение, что продление жизни увеличивает лишь период дряхления, тогда как хотелось бы увеличить продолжительность здоровой жизни. Можно предположить, что некоторые очень слабые люди каким-то образом живут в таком состоянии и дотягивают до 100 лет. Или, напротив, супердолгожители могут походить на наших червей с мутантным геном daf-2: дольше сохраняют здоровье и именно поэтому дольше живут. Замечательно, что чаще всего супердолгожители напоминают наших мутантов – живут дольше, поскольку дольше остаются здоровыми. При изучении людей с очень большой продолжительностью жизни в рамках Проекта по изучению генов долгожительства и Исследования столетних людей в Новой Англии на предмет возникновения у них возрастных заболеваний (рака, болезней сердца, диабета, гипертонии и др.) было установлено, что они действительно не страдали от этих нарушений и сохраняли хорошее здоровье дольше, чем другие участники исследований[6]. Фаза болезней у них действительно оказывалась более сжатой, как и предполагал Фрайс[7]. Будущие супердолгожители, судя по всему, дольше живут без возрастных заболеваний, чем их современники с обычной продолжительностью жизни.
Однако, несмотря на отсутствие возрастных заболеваний, поддержание здорового образа жизни супердолгожителями скорее исключение, чем правило. Парижанин Робер Маршан перестал участвовать в соревнованиях по велосипедному спорту только в возрасте 106 лет (а кататься продолжал до 108 лет) и после этого прожил еще три года, но такой спортивный образ жизни выглядит исключением, поскольку большинство супердолгожителей не связывают свою продолжительность жизни с физическими упражнениями или здоровыми привычками. Вообще говоря, кажется, что многие из них прожили удивительно долго, невзирая на нездоровое поведение, такое как курение, употребление алкоголя и странные пищевые пристрастия. Известный пример – Жанна Кальман, которая большую часть жизни курила (но ведь также можно сказать, что из-за курения кто-то прожил “всего” 99 лет?). В ответах на вопрос “Что для вас ключ к долгой жизни?” часто упоминались алкоголь, мороженое и бекон. Джек Рейнолдс (106 лет), который каждый год в день рождения попадал в Книгу рекордов Гиннесса, уверял, что волшебная пуля – это два стакана виски в день, тогда как Агнес Фентон (110 лет) предпочитала пиво Miller High Life и виски Johnny Walker Blue. Тереза Роули (104 года) связывала свое долголетие с кока-колой без сахара, но признавала, что более важную роль, возможно, сыграло долголетие ее отца, который прожил 102 года, причем диетической колы при его жизни еще не было. Вообще говоря, приходится признать, что, если вам предназначено прожить чрезвычайно долго, ваш образ жизни не имеет значения – бесполезная информация для всех остальных смертных. Судя по всему, долгожители и супердолгожители, не подчиняющиеся никаким правилам и устойчивые против любых укорачивающих жизнь диет и пристрастий, не являются эталоном здорового образа жизни.
Чтобы понять, какие элементы образа жизни могут играть важную роль, лучше сосредоточиться на изучении специфических культур и целых групп людей с высокими показателями продолжительности жизни. Майкл Пулейн, Джованни Пес и другие идентифицировали так называемые “голубые зоны”, где проживают люди с самой большой продолжительностью жизни[8]. К их числу относятся жители Окинавы в Японии, Сардинии в Италии, Икарии в Греции, полуострова Никоя в Коста-Рике и адвентисты седьмого дня из Центральной Калифорнии. Долгожительство в этих “голубых зонах” связывают со здоровым питанием, расслабленным образом жизни, здоровыми общественными отношениями и положительным настроем. Важная роль отводится средиземноморской диете, которая в значительной степени основана на употреблении растительной пищи, оливкового масла и красного вина, или низкокалорийной диете Окинавы. Долгожительство населения Икарии связывают не только со средиземноморской диетой, но и с особенностями культуры – размеренным образом жизни, низким уровнем стресса, ходьбой и социальной интеграцией. Большинство из этих параметров совершенно понятны, но перестали быть нормой во многих активно развивающихся современных культурах.
На основании изучения “голубых зон” велосипедист, участвовавший в гонках на выносливость, и участник проектов National Geographic Дэн Бюттнер предположил, что можно жить дольше, осуществив девять важнейших изменений в образе жизни, среди которых: усиление естественной двигательной активности, такой как ходьба; отказ от курения; снижение уровня стресса; принадлежность к какому-либо сообществу; наличие целенаправленной деятельности; употребление в пищу большего количества овощей и фруктов; легкое недоедание (до 80 % насыщения); и предпочтительное общение с семьей и друзьями[9]. В настоящее время в городе Альберт-Ли в Миннесоте проводится социальный эксперимент, в рамках которого рекомендации “голубых зон” воплощаются в жизнь в масштабах всего города[17]. В рамках проекта предусмотрено изменение движения транспорта и образование новых пешеходных зон, велосипедных дорожек, парков и мест общественного пользования, введение новых программ на рабочих местах и в школах, а также изменение ассортимента пищевых продуктов в ресторанах и продовольственных магазинах. С момента начала реализации проекта сообщалось, что город сэкономил миллионы долларов на нужды здравоохранения, главным образом за счет сокращения употребления табачных изделий и благоприятных изменений в связи со снижением массы тела жителей. Считается, что благодаря этим изменениям средняя продолжительность жизни должна вырасти на 2,9 года, но даже если люди не станут жить дольше, такие изменения приведут к улучшению здоровья общества в целом, повышению качества жизни и сокращению затрат на медицинское обслуживание. Этот последний результат следует подчеркнуть особо, поскольку такие инфраструктурные перемены в масштабе целого города следует рассматривать как долгосрочную инвестицию, а не какую-то необоснованную статью расходов.
Конечно же, люди доживают до 100 лет не только в “голубых зонах”. В Японии, Италии, Португалии и Испании до ста доживают примерно 40–50 человек из 100 тысяч (как ни странно, по данным проверки, около 200 тысяч японцев старше 100 лет оказались неучтенными, и, следовательно, это неточные данные). В целом люди, преодолевшие столетний рубеж, все реже вызывают удивление. Быть может, не все определяется образом жизни, и снова возникает классическая дилемма “наследственность против среды”. Возможно, представители каких-то популяций живут дольше (после сокращения числа детских и инфекционных заболеваний) благодаря своему генетическому строению, и в таком случае их геномы могут раскрыть секреты долголетия. По некоторым оценкам, от четверти до половины вариаций продолжительности жизни людей имеют генетическую основу[10]. Вообще говоря, наилучший предсказательный фактор вашего долголетия – это наличие долгожителей среди членов вашей семьи, что указывает на очевидный генетический компонент. Для человека, чей брат или сестра дожили до столетнего возраста, вероятность также дожить до ста лет увеличивается в 17 раз, однако узнаете вы об этом, понятное дело, очень поздно. Семья Кан представляет собой один из удивительных примеров долгожителей среди братьев и сестер. Четверо из них – Ирвин (109 лет), Хелен “Хэппи” Рейхерт (109 лет), Питер Кин (103 года) и Ли (101 год) – жили удивительно долго и до самого конца сохраняли отличное здоровье, что иллюстрирует модель “сокращения фазы болезней”, которую Фрайс и другие считают наилучшим сценарием для долгой жизни. Анализ геномов таких семей может выявить важную информацию о долгожительстве.
Но как найти эту генетическую информацию? С помощью метода полногеномного поиска ассоциаций (GWAS) ученые пытались выявить в образцах ДНК долгожителей последовательности, отличающиеся от аналогичных последовательностей у других людей. Такие исследования, основанные на данных для большого количества людей, позволяют обнаруживать в ДНК замены отдельных нуклеотидов (SNP), которые чаще встречаются среди долгожителей, чем среди обычных людей. Метод GWAS очень хорошо зарекомендовал себя в анализе некоторых заболеваний, связанных с изменениями единичных генов, но это не простой метод[18]. Его можно сравнить с поисками иголки в стоге сена – однако, если иголок много, вы с большей вероятностью что-то найдете, так что увеличение частоты встречаемости искомого признака очень помогает. Чтобы метод GWAS сработал, исследователь должен иметь много образцов с искомой болезнью или фенотипом и без него, что позволит статистически достоверно установить, что данный вариант ДНК действительно связан с конкретным заболеванием, а не является совпадением. Подбор достаточного количества людей с конкретным фенотипом и особенно с одинаковыми вариантами ДНК занимает много времени. Поскольку при изучении долгожителей не существует “контрольной группы” людей такого же возраста, часто для контроля проводят сравнение потомков долгожителей с их сверстниками.
Вторая преграда на пути активного внедрения метода GWAS – стоимость получения информации. Поначалу в методе использовали SNP-микрочипы (микрочипы не со всей геномной ДНК, а только с репрезентативными вариантами однонуклеотидных полиморфизмов), но такие чипы дороги, что ограничивало объем получаемой информации. Позднее для анализа и секвенирования стали использовать небольшую часть (около 5 %) генома, которая транслируется в белки (так называемый экзом), однако при этом, понятное дело, не учитываются SNP в некодирующих регуляторных последовательностях, которые также могут играть важную роль[11]. Раньше секвенирование целого генома стоило очень дорого; постепенно благодаря снижению стоимости технологии секвенирования его стали применять чаще, но и анализ SNP тоже все еще используется для поиска генетических различий, влияющих на продолжительность жизни (или для выяснения, существуют ли такие различия в принципе). Ученые анализировали данные для долгожителей с общностью происхождения, таких как жители Окинавы, евреи-ашкеназы, немцы, датские близнецы, близкородственное население Исландии и финны[12]. Кроме того, проводились исследования в различных группах населения (например, среди долгожителей в Новой Англии[13], в Проекте по выявлению генов долгожительства, в исследованиях семей долгожителей, представителей религиозных орденов, медицинских сестер и во Фрамингемском исследовании) и даже в более гетерогенных группах. (Интересно было бы узнать, какова связь между образом жизни населения “голубых зон” и генетикой этих людей.) В любом случае, поскольку все больше людей доживают до глубокой старости, а стоимость секвенирования генома продолжает снижаться, вскоре у нас появится более обширная информация относительно генетического аспекта долгожительства.
Так что же показывает анализ генома людей с большой продолжительностью жизни? Прежде всего, давайте внесем ясность и определим, что может и чего не может метод GWAS. Результатом каждого такого исследования становится выявление стойкой корреляции между фенотипом (в данном случае долгой жизнью) и конкретным основанием ДНК в геноме (вариантом нуклеотида в одном конкретном месте – однонуклеотидным полиморфизмом, SNP). Значимость (надежность) этих результатов описывается p-значением, которое показывает, какова вероятность, что данная корреляция не реальная, а лишь результат совпадения (таким образом, очень малая величина p-значения говорит о высокой вероятности устойчивой корреляции). Мы предполагаем, что конкретный ген имеет отношение к фенотипу, если он расположен вблизи от известного SNP: SNP может находиться внутри кодирующей последовательности гена, в промежутке (интроне) между кодирующими последовательностями (экзонами) или в регуляторной области, отвечающий за экспрессию гена. Но человеческий геном устроен сложно, и бывает так, что важный SNP в участке ДНК, контролирующем экспрессию гена, находится на значительном расстоянии от самого гена (так называемый энхансер), что усложняет интерпретацию результатов. Мы с большей уверенностью можем утверждать, что какой-то ген важен для данного признака, если на него указывают разные SNP, выявленные в нескольких исследованиях.
Однако метод GWAS не позволяет ничего сказать о том, каким образом конкретный ген влияет на продолжительность жизни, – то есть понять механизм влияния генов на продолжительность жизни. Если какой-то SNP (замена генетического кода в конкретном участке) вызывает очевидный признак, например мутацию, укорачивающую или “разрывающую” белок, мы уверены: в норме функция этого гена препятствует удлинению жизни. Однако такие очевидные изменения встречаются редко, поскольку подобные мутации, как правило, производят разрушительное и даже фатальное действие на ранних этапах жизни (вспомните о теории антагонистической плейотропии, которую мы обсуждали в предыдущей главе), так что при изучении долгожительства с помощью технологии GWAS мы с наибольшей вероятностью будем обнаруживать какие-то гораздо более тонкие различия. Вообще говоря, ДНК в целом (если не учитывать мутации) – устойчивый, или “статичный”, элемент центральной догмы, в отличие от РНК и белков, подверженных динамическим колебаниям. Поэтому наличие SNP, коррелирующего с болезнью, ничего не говорит о том, в какой момент жизни она может проявиться. Несмотря на эти ограничения, GWAS служит полезным инструментом для начала изучения молекулярных основ заболеваний и снабжает нас некоторой информацией относительно генетических основ долгожительства.
Ранние исследования продолжительности жизни с помощью GWAS показали, что некоторые варианты генов APOE и FOXO3A коррелируют с большой продолжительностью жизни, и эти данные многократно воспроизводились. Позднее было показано, что долгожительство также связано с никотиновым ацетилхолиновым рецептором CHRNA3/5. Чаще всего в исследованиях долгожительства с применением GWAS идентифицируют именно эти три гена[14]. Совсем недавно стал регулярно выявляться SNP 5q33.3 с неизвестной генетической функцией[15]. Что же это за гены и почему они могут быть связаны с долголетием? Вы могли слышать о белке APOE в связи с болезнью Альцгеймера. Этот белок участвует в регуляции метаболизма липидов и уровня липопротеинов высокой плотности (ЛПВП). Высокий уровень содержания ЛПВП (“хорошего холестерина”) связан с лучшим прогнозом для состояния сердечно-сосудистой системы и большой продолжительностью жизни. APOE существует в нескольких вариантах: ε2, ε3 и ε4. Самый распространенный вариант – ε3, вариант ε4 в наибольшей степени связан с риском развития болезни Альцгеймера, а вариант ε2 – с возрастной дегенерацией макулы и потерей слуха. Однако, несмотря на связь с продолжительностью жизни, которая воспроизводится в анализе GWAS, мы еще не знаем, как именно варианты APOE влияют на долголетие.
Выяснилось, что SNP в гене APOE находятся в “неравновесии по сцеплению” с геном TOMM40: это означает, что SNP генов APOE и TOMM40 встречаются вместе чаще, чем по воле случая и, следовательно, связь с продолжительностью жизни в какой-то степени может объясняться действием гена митохондриального белка TOMM40. Пос
