Занимательная наука
Предисловие
Увлечение наукой начинается обычно с наблюдений и опытов. В книгах, сети Интернет можно найти много простых, полезных и захватывающих экспериментов, с которыми могут справиться юные любители опытов. Именно такие опыты вы найдете в нашей книге.
Большинство из них было описано ранее в научных журналах. Именно поэтому мы подобрали очень простые опыты, которые можно сделать из веществ, часто используемых в быту. Найти их можно в домашней аптечке или на кухне. К каждому опыту есть описание, научное обоснование и получившийся результат, который можно увидеть на рисунке. Наш художник постарался, чтобы все выглядело, как в жизни.
Обращаем внимание на то, что в книге описаны некоторые опыты, которые необходимо делать только вместе со взрослыми и обязательно соблюдать правила пожарной безопасности.
Опыты подобраны так, чтобы не только заинтересовать юных естествоиспытателей, но и показать им привлекательность самостоятельного исследования.
Загадочный и прекрасный мир науки
Мы живем в мире, полном удивительных явлений. Можно даже сказать, что нас окружают чудеса. Они везде и всюду. Для юных естествоиспытателей — это научные чудеса.
Шум воды, гроза, стрекотание кузнечика, кипение чайника, ветер — все явления, с которыми мы сталкиваемся в нашей повседневной жизни, имеют научное объяснение. Объяснить нам эти явления помогает знание научных законов, которые есть в физике и химии.
Например, такое природное явление, как гроза, издревле у человека вызывало страх. Страшны были всполохи молнии и раскаты грома, порывы ветра и обложной дождь. Сегодня ученые могут объяснить это природное явление и даже предсказать его. И, зная научное объяснение, уже не страшно пить чай в садовой беседке во время грозы, ведь всегда можно рассчитать, на каком расстоянии от нашей беседки находится эпицентр грозового облака. А дождю мы всегда рады!
То же самое относится, например, и к электричеству. Еще каких-то сто лет назад к лампочке, которая вспыхивала от нажатия выключателя на стене и горела долго, даря много света, было отношение, как к чуду. Сегодня мы можем самостоятельно на уроке физики собрать электрическую цепь и рассчитать силу тока.
Таким образом, то, что считалось чудом, попадая в круг научных интересов, сразу перестает им быть и включается в нашу обыденную жизнь.
Именно наука и ученые помогают нам в этом. Именно научные объяснения происходящего помогают понять и постичь этот интересный мир. Ведь, наука — это красиво и интересно. А если интересно, тогда — вперед! В новый мир научных открытий!
Зачем мы экспериментируем?
Слово «Экспериме́нт» происходит от латинского слова experimentum — проба, опыт. Само название говорит нам о том, что, если мы хотим что-то узнать, надо сначала попробовать, что может получиться.
Химики и физики всегда экспериментировали или проводили опыты и пробы. Не всегда опыт получается с первого раза. Бывает и такое, что часто эксперимент «проваливается», а ученый раз за разом продолжает его делать, снова пробует, строит новое оборудование или делает новую подборку веществ. Такая научная настойчивость и пытливость часто приводила к тому, что в конце концов эксперимент завершался успешно, а ученый с удовольствием приступал к следующему исследованию.
Почему мы об этом говорим? Потому что многое в нашей жизни — это наши научные эксперименты: приготовление еды, изучение языка, решение математической задачки — многое из того, что мы делаем, требует экспериментального подхода. Так, после неудачных попыток приготовить вкусный торт, мы, наконец, научимся его печь; после неправильного написания слова на иностранном языке, мы, многократно заучив его, легко используем в письме; после неправильного выбора способа решения математической задачки, ищем другой способ ее решения. Это наши эксперименты.
Не обязательно стать в конце концов физиком или химиком. Главное — пробовать, а если не получилось, то не унывать и пробовать снова. И загадочный мир научных экспериментов станет простым и понятным, а значит интересным.
Давайте знакомиться или наши правила
Собрались мы снова вместе,
Чтобы было интересней!
Много нового узнаем,
Что ж, ребята, начинаем!
Давай познакомимся.
Я, естествоиспытатель Леонардо — исследователь и ученый. Я познакомлю тебя с удивительным миром науки, миром опытов, экспериментов и новых открытий.
Рис.1 Давайте знакомиться.
Для начала ты должен усвоить несколько правил. Эти правила знакомы всем исследователям и экспериментаторам.
Правило первое. Строго и точно необходимо соблюдать все рекомендации и инструкции по проведению опытов. Ведь одна и та же химическая реакция может идти по-разному, если изменить условия опыта. Например, если повысить температуру, или добавить в пробирку какое-либо вещество, или добавлять вещества в иной, чем указано, последовательности.
Правило второе. Никогда нельзя смешивать два реактива для того, чтобы проявить любопытство и посмотреть, что получится. Не всегда получается хорошо. Совсем другое дело, если ты точно знаешь, что образуется в результате реакции и как она идет.
Правило третье. Нельзя использовать для опытов посуду, из которой едят. Для опытов нужна своя, отдельная посуда. И еще, никогда не пробуй вещества на вкус (кроме тех случаев, когда в описании опыта прямо сказано, что продукт можно попробовать).
Правило четвертое. Хранить реактивы необходимо в отдельных коробках или склянках. Чтобы не было путаницы, наклей этикетки и напиши, что находится внутри. Если препарат больше не нужен (или если опыт закончен, а продукты реакции вам ни к чему), то немедленно выбрось ненужные вещества — так спокойнее, и не будет путаницы.
Правило пятое. Нельзя оставлять грязную посуду. Это связано с тем, что ее будет потом трудно отмыть, а кроме того, некоторые вещества окисляются на воздухе, реакции между ними могут продолжаться и после того, как опыт закончен, и в результате таких реакций может получиться нечто такое, на что мы с вами не рассчитывали.
Правило шестое. Никогда не бери реактивы руками, не наклоняйся над склянками, в которых идут реакции, не нюхай вещества с едким запахом, не затыкай пробирку пальцем при смешивании. Береги и одежду, и кожу, и, прежде всего, глаза от брызг и крупинок. Будь всегда осторожным!
Правило седьмое. Приступать к опыту можно только после того, как будут ясны все действия. Еще до начала работы внимательно прочти описание опыта от начала до конца. Запиши все, что может понадобиться: посуда, реактивы, штатив, держалки. Разложи их на рабочем месте так, чтобы все было под рукой. И только после такой тщательной подготовки приступай к работе.
Что мы знаем о воде?
А теперь я расскажу вам, ребята, одну историю. Эта история об одном из самых главных веществ на Земле — воде.
Когда-то, давным-давно Земля была безжизненной планетой.
Рис.2. Что мы знаем о воде?
И только ветры и ураганы свободно гуляли по поверхности Земли. Именно в это время «бомбили» нашу Землю космические тела, принося с собой в пыли, замерзшую воду — лед.
Об этом пишут и планетологи. Они пишут, что источником воды на Земле были кометы и астероиды [1].
Можно себе вообразить, какое количество небесных тел, космической пыли попало на Землю, чтобы сформировались океаны и моря.
Однако, как считают ученые, «воды на Земле мало, немного ее и на Луне, Меркурии, Венере и Марсе. Возможно, на Венере и Марсе раньше было больше воды. Основной резервуар воды в рамках орбиты Юпитера — пояс астероидов» [1].
Вода есть везде — на поверхности Земли она образуем моря, реки, океаны, ледники. В воздухе вода — это облака и тучи. В глубинах земли вода может образовывать большие озера и подводные реки.
Воду мы можем найти не только в воздухе или на поверхности Земли.
Вода в виде пара присутствует даже в нашем дыхании. Подышите на зеркальце, и через некоторое время вы увидите, что оно затуманилось и на поверхности появились чуть заметные капельки. Это произошло потому, что выдыхаем мы воду в виде водяного пара. Для нас это остается незаметным. Однако если мы будем использовать «специальный уловитель» — зеркальце, мы сможем обнаружить воду даже в выдыхаемом нами воздухе.
Информационные источники:
1. https://lenta.ru/articles/2017/07/10/water/
Опыты с водой
Я и туча, и туман,
И ручей, и океан,
И летаю, и бегу,
И стеклянной быть могу!
(Вода).
Вода не имеет формы и принимает форму того сосуда, в который налита. Давайте поверим, так ли это.
Вылейте немного воды в тарелку. Что произошло с водой? Она растеклась.
Рис.3. Опыты с водой.
Вспомните, ребята, где и как разливаются лужи или чай на столе.
А еще вода не имеет вкуса и запаха. Отпейте немного воды из стакана. А если добавить вводу сахар или соль, то у воды появится вкус, попробуйте.
Если понюхать воду, то мы ничего не почувствуем. Однако суп, сверенный мамой или бабушкой так замечательно пахнет!
Вот мы и познакомились с некоторыми свойствами воды, об остальных свойствах воды мы узнаем с вами дальше.
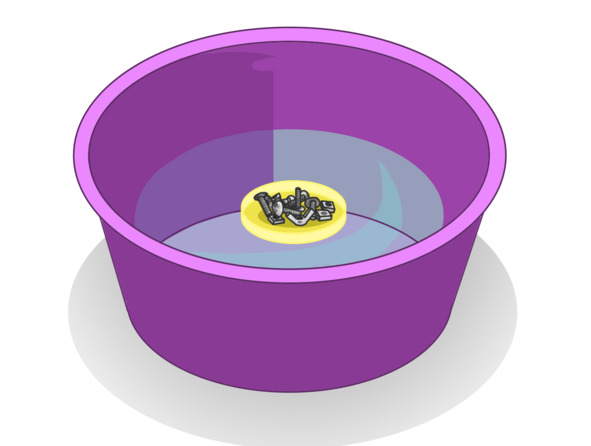
Шарики
Пришло время позвать ученого Леонардо, который нам расскажет о свойствах воды, твердых тел, покажет увлекательные опыты.
Леонардо решил показать нам интересный опыт с водой, но ему нужна наша помощь. Давайте сначала все подготовим.
Для опыта надо взять воздушные шарики, камни, тазик с водой, насос для надувания шаров.
Положите по одному камню в шарик. Первый шарик не надувайте, а завяжите его, как можно ближе к камню.
Второй шарик надуйте насосом. Завяжите шарик, как можно ближе к его концу.
Теперь налейте воду в тазик и положите оба шарика в миску с водой.
Надутый шарик будет плавать на поверхности, а шарик с камнем опустится на дно.
Рис.4. Шарики.
Как вам кажется, ребята, почему это произошло?
Если никто не догадался о причине, по которой шарик плавал, нам подскажет Леонардо.
— Действительно, надутый шарик остался на поверхности воды, не смотря на то, что в него мы тоже положили камень. Это произошло потому, что воздух, который мы закачали в шарик с помощью насоса, удерживает на поверхности воды наш шарик и не дает ему утонуть. И мы с вами это наблюдали, ведь первый шарик (без воздуха) утонул.
Леонардо призадумался:
— Ребята, как вы думаете, явление, которое мы с вами только, что наблюдали, встречается в природе?
— Встречается, например у рыб. У них нет камня внутри, но они могут плавать около дна, почему? У рыб есть специальный орган, который работает, как воздушный шарик. Это плавательный пузырь. Если в нем много воздуха, рыба всплывает, а если мало — опускается на дно.
Пузырьки в воде
Наш ученый Леонардо опять думает. И думает он над такой научной проблемой, — как можно увидеть воздух?
— Ребята, а как же можно увидеть воздух? Как его обнаружить?
Возьмем для этого опыта стаканчики с питьевой водой и трубочки для коктейля.
Давайте возьмем трубочки и побурлим с помощью них в стакане. Что вы увидели в воде? Мы увидели пузырьки воздуха на поверхности воды. Их хорошо видно в воде, потому что воздух и вода не смешиваются.
Поэтому, когда мы пьем вкусный кислородный коктейль, мы пьем не смешиваемый с жидкостью кислород, который полезен для нашего организма.
Рис. 5. Пузырьки.
Почему собака дразнится?
Сегодня наш ученый Леонардо был не в духе. Было очень жарко, и Леонардо вышел на улицу, чтобы подышать свежим воздухом. Но ему почему-то показалось, что собаки, которые пробегали мимо, дразнили его, высунув язык. Что же произошло с собаками? Почему они вдруг решили дразнить нашего Леонардо?
Рис. 6. Почему собака дразнится?
Ответ был найден. Почти вся поверхность тела собаки покрыта шерстью. Поэтому собаки очень хорошо защищены от холода, но уязвимы для жары. Когда температура на улице тридцать градусов по Цельсию, то человеку очень жарко, течет пот и становится тяжело дышать. Примерно те же чувства испытывает собака. Причем температура тела собаки гораздо выше температуры тела человека.
Потовые железы собаки расположены на поверхности носа и также в пасти. Это единственные места, через которые организм собаки охлаждается. Если у человека — это вся поверхность кожи, то у собаки лишь небольшой участок. Поэтому не стоит удивляться, почему собака высовывает язык, таким образом, она пытается сбить повышенную температуру тела организма.
Когда собаке становится жарко, ее пульс начинает учащаться, а, следовательно, и учащается дыхание. Поэтому, мы можем наблюдать, как коты и собаки в жару высовывают язык и дышат с открытой пастью. Для того, чтобы температура тела собаки пришла в норму, ей необходимо охлаждаться.
Давайте узнаем, как собака охлаждается через язык.
Для этого эксперимента мы возьмем стакан с водой, ватные палочки.
Обмакните ватный шарик в воде и выжмите излишки. Проведите ватным шариком по поверхности руки. Поднимите и держите руку на расстояние десяти сантиметров ото рта. Подуйте на мокрый участок на руке. Что вы почувствовали?
Эксперимент «Сухая салфетка»
Сегодня Леонардо превратился в настоящего фокусника. Он пришел с целой сумкой всякой всячины. В сумке были миска (не менее десяти сантиметров в высоту и пятнадцати сантиметров в диаметре), линейка, вода, салфетка, одноразовый стаканчик, платок.
А мы будем его помощниками — ассистентами.
Сейчас мы научимся с вами оставлять бумагу сухой, опуская её в воду. Повторяйте за Леонардо, делайте вместе с ним.
Итак, наполните чашку водой почти до краев. Чтобы проверить, сколько воды мы налили. Давайте возьмем линейку и замерим уровень воды.
Сомните салфетку в комок и положите на дно стаканчика. Переверните стаканчик вверх дном. Салфетка должна находиться на самом дне стаканчика. Если она сползает или выпадает, немного разверните салфетку, приклейте скомканную салфетку на дно стакана. Возьмите стаканчик, держа вверх дном. Опустите его вертикально в чашку с водой, так, чтобы края достали дна чашки. Только не наклоняйте чашку.
Леонардо накрыл миску платком, произнес волшебные слова: «Ахалай, махалай». Он снял платок, вытащил стаканчик из воды, продолжая держать его вертикально.
Леонардо вытащил скомканную салфетку из чашки и осмотрел её. Салфетка осталась сухой.
Рис. 7. Сухая салфетка.
У вас тоже салфетка оказалась сухой?
Почему так произошло?
Сейчас Леонардо нам все расскажет:
— Воздух занимает определённый объём. Воздух можно легко поймать, так как он повсюду вокруг нас. Он заполняет все пустые пространства, в том числе и пустой стаканчик. В стакане есть воздух, в каком бы положении он ни находился. Когда вы переворачиваете стакан кверху дном и медленно опускаете в воду, воздух остаётся в стакане. Вода из-за воздуха не может попасть в стакан. Давление воздуха оказывается больше, чем давление воды, стремящейся проникнуть внутрь стакана. Бумага на дне стакана остается сухой. Если стакан под водой перевернуть набок, воздух в виде пузырьков будет выходить из него. Тогда сможет попасть в стакан.
Эксперимент «Цветная вода»
Можно ли вода быть цветной? Можно ли раскрасить воду в разные цвета? На эти вопросы нам снова даст ответ ученый Леонардо.
Он приготовил шесть бутылочек с крышечкой, гуашь шести цветов.
Для того, чтобы провести этот эксперимент, нужно заранее густо покрасить крышки бутылок с внутренней стороны разными цветами гуаши. Затем наливаем в бутылки воду так, чтобы они были заполнены не полностью.
После того, как Леонардо все подготовил, он аккуратно выставил бутылки так, чтобы не смешать воду с краской.
И снова Леонардо произносит волшебные слова, чтобы на фокус-эксперимент получился:
— Ахалай, махалай.
Потрясем бутылочки и… Мы видим, как вода моментально окрашивается в разные цвета.
Таким образом, мы убеждаемся в том, что вода прозрачная и не имеет цвета, но легко окрашивается.
А сейчас раскроем секрет нашего фокуса-эксперимента. Открутите крышки бутылок — на крышке есть остатки краски.
Этот заранее подготовленный фокус можно показывать, чтобы вызвать удивление друзей.
Рис.8. Цветная вода.
Эксперимент «Исчезающая монетка»
Сегодня Леонардо снова пришел к нам с целой сумкой вещей. Здесь и стеклянная банка с крышкой емкостью 1 литр (или одноразовый стаканчик), бутылка с водопроводной водой, монетка.
— Я заставлю монету исчезнуть, — сказал Леонардо.
Нальем в банку водопроводной воды и закроем крышку. Возьмем монетку и убедимся, что это действительно самая обычная монета и в ней нет никакого подвоха. Положим монету на стол. Поставим на монетку банку с водой. Скажем волшебные слова, например: «Вот волшебная монета, вот была, а вот и нету».
А теперь посмотрите сквозь воду сбоку банки и скажите, видна ли монетка теперь?
Скажем другие волшебные слова, например: «Как монетка провалилась, так она и появилась».
Теперь уберите банку, и монета снова окажется на месте. Когда мы ставим на монетку банку с водой, кажется, что монетка исчезла.
Рис. 9. Исчезающая монетка.
Эксперимент «Звезда»
Леонардо так понравились эксперименты с водой, что он придумал еще один фокус. Он показал нам, как несколько капель воды могут сделать из спичек звезду.
Для этого эксперимента мы взяли 5 спичек и одноразовую тарелочку, пипетку.
А теперь давайте проведем фокус со спичками.
Надломите все спички посредине, согните под острым углом и положи на блюдце.
Как сделать из этих спичек пятиконечную звезду, не прикасаясь к ним? Всего лишь нужно уронить несколько капель воды на сгибы спичек! Постепенно спички начнут расправляться и образуют звезду.
Рис.10. Эксперимент «Звезда».
Почему спички расправились? Как получилась звезда?
Леонардо рассказал нам, что волокна дерева впитывают влагу. Она поднимается все дальше по капиллярам. Дерево набухает. Его уцелевшие волокна «толстеют». Став толстяками, они уже не могут так сильно сгибаться и распрямляются.
Мы с вами попробовали себя в роли настоящих фокусников и узнали еще одно свойство воды, вспомните его.
Правильно, это свойство…
Эксперимент «Разбегающиеся спички»
Леонардо так был заинтересован экспериментом со спичками, что он решил провести еще один опыт. Для опыта он взял чашку с водой, спички, мыло, 1 кусок сахара.
Давайте сделаем этот опыт так, как сделал его Леонардо. Аккуратно положим несколько спичек в чашку с водой, соберем их посередине вместе в виде звездочки. Медленно, еле погружая в воду заостренный кусочек мыла, коснемся им воды в середине звездочки. Мы увидим, что спички тут же разбегутся во все стороны.
Коснемся теперь воды в середине чашки кусочком сахара, и спички соберутся вместе.
Как объяснил Леонардо, на поверхности жидкость как бы покрыта тонкой и эластичной пленкой. Кусочек мыла, растворяясь в середине звездочки из спичек, уменьшает эластичность этой пленки в этом месте. Получается передвижение жидкости от центра чашки к краям, оно не заметно нашему глазу. Поэтому спички расходятся в стороны.
Кусочек сахара, впитывающий в себя воду, вызывает, наоборот, передвижение воды от краев к сахару. Спички снова собираются вместе.
Эксперимент «Из воды в воду»
Ученый Леонардо сегодня сделал удивительное открытие. Оказывается, вода может перемещаться с одного предмета на другой предмет, а мы этого даже можем не заметить. Хотите узнать, как он сделал это открытие?
— Это удивительное свойство воды было открыто за завтраком. Леонардо налил себе чашку горячего чая и уже хотел было выпить его, но тут зазвонил телефон. Конечно же, Леонардо пошел искать телефон и долго по нему разговаривал, а чтобы чай не остыл, накрыл чашку блюдцем. Когда Леонардо вернулся и открыл чашку, то увидел, что на блюдце появилась вода. Это несказанно удивило Леонардо, ведь он накрывал чашку совершенно сухим блюдцем.
Рис.11. Эксперимент «Из воды в воду».
Как же вода оказалась на блюдце?
Проведем эксперимент.
Для эксперимента мы взяли стакан горячей воды, два блюдца — одно холодное, другое теплое.
Давайте потрогаем блюдце и убедимся, что оно совершенно сухое. А теперь нароем блюдцем стакан с горячей водой. Осторожно, не обожгитесь.
Чтобы на блюдце появился конденсат нужно подождать некоторое время.
А теперь давайте откроем наш стакан. Посмотрите, на блюдце появились капельки воды, так как же они туда попали?
Вот как это явление объясняет Леонардо. Вода стала испаряться и осаждается на холодном блюдце в виде горячего пара, затем она снова остывает и превращается в воду. Этот процесс называется конденсацией. Конденсация — это переход вещества из газообразного состояния в жидкое.
Давайте повторим наш эксперимент, но с тёплым блюдцем. На тёплом блюдце воды нет, таким образом, процесс превращения пара в воду происходит при охлаждении пара.
Чтобы опыт получился, какая вода должна быть в стакане холодная или теплая?
Что появится под блюдцем, которым накрыт стакан?
Какое явление мы наблюдаем? (Явление конденсирования).
Эксперимент «Почему плавает железо?»
Может ли железо плавать? Вряд ли, скажете вы. И наверное будете правы, а может быть и нет. А наш ученый Леонардо решил провести эксперимент и узнать, плавает ли железо. Ученые всегда проводят эксперименты, когда они хотят получить точный ответ.
Для эксперимента возьмем миску, скрепку, бумажное полотенце, емкость с водой, ножницы, зубочистку, любые железные предметы.
Итак, налейте воду в емкость. Давайте посмотрим, плавает ли железо в воде. Опустите любые железные предметы в воду. Все железные предметы оказались на дне — утонули. Значит, железо не плавает.
А теперь возьмем бумажное полотенце, ножницы, зубочистку, миску и емкость для воды, скрепку. Возьмем скрепку и опустим скрепку в воду. Что случилось со скрепкой? Скрепка утонула.
Достанем скрепку из воды и хорошо ее оботрем. Давайте наполним миску водой примерно на три четверти. Вырежем из бумажного полотенца квадратик (5 на 5 см) и положим в его середину скрепку.
Опустим квадратик в воду так, чтобы он плавал на поверхности. Осторожно надавливая зубочисткой на бумагу, утопим ее так, чтобы скрепка осталась на поверхности воды. Будет ли плавать скрепка и как долго?
Рис.12. Почему плавает железо?
Леонардо говорит, что скрепка может оставаться на поверхности воды сколько угодно времени. Если присмотреться, то можно увидеть, что уровень воды возле скрепки слегка снижен.
Как нам объясняет Леонардо, молекулы воды связаны между собой силами притяжения. Это особенно ярко проявляется на поверхности, которая из-за этого похожа на упругую пленку вроде надутого шарика. Благодаря этому скрепка, как и другие легкие тела, может плавать по воде. Вот поэтому железная скрепка плавает и не тонет.
Как утопить железо, которое не тонет?
Однако Леонардо не успокаивался. Он все же решил найти способ, чтобы утопить скрепку. Он снова взял металлическую скрепку, жидкое мыло, бумажное полотенце, емкость с водой.
И Леонардо решил провести эксперимент. Он осторожно положил бумажное полотенце на воду, а на него — скрепку. Добавил в воду немного жидкого мыла, но не рядом со скрепкой, а в стороне. А затем резко выдернул полотенце из-под скрепки. Что произошло? Скрепка опустилась на дно. Это произошло потому, что, растворяясь в воде, жидкое мыло ослабляет ее поверхностное натяжение настолько, что оно оказывается не в состоянии больше выдержать вес скрепки
Эксперимент «Перегруз»
Леонардо предложил игру в кораблики. Он взял миску с водой, широкую пластиковую крышку. Только это будет не обычная игра. Каждый кораблик (пластиковую крышку) мы будем нагружать различными мелкими предметами: монетами, скрепками, шурупами.
Опустите в воду крышку. Немного понаблюдайте за ней, как она плавает, насколько погружена в жидкость.
А теперь давайте попробуем затопить наше судно.
Леонардо поместил в центр нашего «корабля» скрепку. Затем он положил в крышку еще один предмет. После этого поместил туда шуруп, потом еще один.
Леонардо заполнял крышку предметами.
Что же будет происходить с нашим «корабликом» по мере заполнения его предметами?
Чем больше предметов, тем глубже крышка погружается в воду. Вскоре, она не выдержит и пойдет ко дну.
Плавает тело или тонет, определяется соотношением его веса и выталкивающей силы. Пока вторая больше первого, тело держится на плаву, а когда вес превышает выталкивающую силу, тело тонет.
Рис.13. Эксперимент «Перегруз»
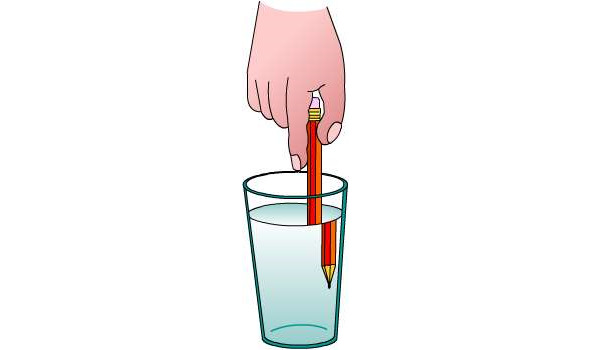
Эксперимент «Оптический обман»
— Давайте побудем настоящими фокусниками! — предложил Леонардо. Начинаем научное волшебство.
Наполните стакан водой чуть больше половины. Держите карандаш перед собой.
— Сейчас я сломаю карандаш, просто опустив его в стакан с водой, хотите узнать, как я это сделаю? — сказал Леонардо.
Ученый опустил карандаш вертикально в воду, чтобы его кончик оказался примерно посередине между дном стакана и поверхностью воды. Обратите внимание, что я держу карандаш в задней части стакана.
— А теперь поводите карандашом туда-сюда в воде, держа его вертикально. Что мы наблюдаем?
— Достаньте карандаш из воды, — Леонардо достал карандаш из воды, отряхнул его и продолжил объяснение.
Нам покажется, что карандаш сломался. Для зрителей та часть карандаша, что находится под водой, слегка смещена относительно той части, что находится над водой.
— Я вам объясню, ребята, почему так получается. Такой эффект возникает благодаря явлению рефракции. Свет распространяется по прямой, но, когда луч света переходит из одного прозрачного вещества в другое, его направление меняется. Это и есть рефракция. Когда свет переходит из более плотного вещества, например, воды, в менее плотное, например, воздух, происходит рефракция, или видимое изменение угла падения луча. Свет в веществах разной плотности распространяется с разной скоростью. Свет, отраженный от карандаша, проходя сквозь воздух, кажется зрителям, находящимся в одном месте, а сквозь воду — в другом.
Рис. 14. Пример рефракции.
Эксперимент «Склеим бумагу водой»
Леонардо придумал новый фокус, давайте посмотрим получится ли у ученого сделать его.
— Возьмите два листа бумаги, приложите их один к другому и попробуйте их сдвинуть следующим образом: один в одну, а другой в другую сторону. Затем смочите листы водой, приложите их друг к другу и слегка прижмите, чтобы выдавить лишнюю воду.
Леонардо ловко проделал все эти манипуляции и на удивление не смог сразу легко сдвинуть листы. Почему так получается?
Ответ на удивление прост. Вода обладает «склеивающим» действием. Таким же эффектом обладает и сырой песок, в отличие от сухого.
Эксперимент «Рукам своим не верю»
Леонардо задумался: одинаково ли ощущают наши руки — левая и правая? Как настоящий ученый он решил провести эксперимент. Взяв две емкости с горячей и холодной водой, Леонардо опустил в них руки (одну руку в емкость с горячей водой, другую руку в емкость с холодной водой) и стал ждать.
Через несколько минут он погрузил обе руки в воду комнатной температуры.
Рис.15. Эксперимент «Рукам своим не верю».
Какой кажется вода горячей или холодной? Оказывается, что на каждой руке будет выявляться своя индивидуальная чувствительность. Та рука, которая была в емкости с холодной водой «согрелась» от воды комнатной температуры. Та же рука, которая была в горячей воде, охладилась.
Оказывается, наше тело охлаждается и нагревается неравномерно.
А теперь задумайтесь, всегда ли можно доверять своим рукам?
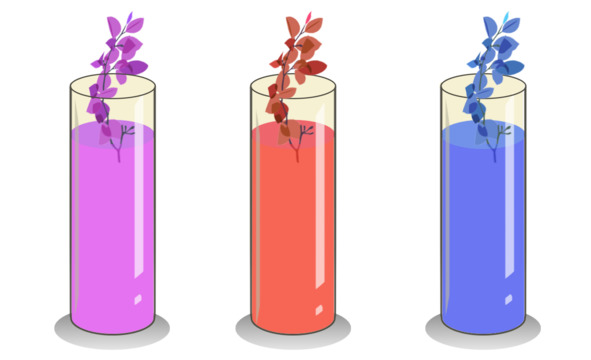
Эксперимент «Вода — скалолаз»
Переливая воду из емкости в емкость Леонардо задумался: а может ли вода не только растекаться, образуя тончайшую пленку, но и подниматься, например, по трубочке? Не долго думая, Леонардо взял несколько стеклянных банок, налил туда подкрашенной разными чернилами воды. Срезав несколько веточек растений, он поставил их в банки и стал наблюдать. Мало-помалу подкрашенная вода заполнила все сосуды растения, окрашивая само растение и цвет прожилок в листьях.
Вот это чудо! Красные, синие и фиолетовые листья!
Как настоящий ученый, Леонардо смог все объяснить. Что же он нам расскажет?
Вода поднимается по стеблю благодаря тому, что растение пронизано тончайшими сосудами — капиллярами, как о трубочкам. По капиллярам жидкость движется вверх тем быстрее, чем они тоньше. Если бы у вас был стеклянный капилляр диаметром 0,02 мм, то вода могла бы подняться по нему на три метра!
Если сделать на каждой ветке несколько поперечных срезов, то можно увидеть, как расположены капилляры. Именно по ним и поднимается вода, окрашивая растение.
Рис. 16. Эксперимент «Вода — скалолаз».
Вода не только может подняться по стеблю. Вода может подняться вверх и в стакане или в прозрачной кружке.
Для того, что увидеть этот чудесный опыт, наливаем в тарелочку или в блюдце небольшое количество воды. Кладем на поверхность небольшой кусочек пробки. Мы делаем это для того, чтобы было видно, как вода поднимается. Для нашего опыта лучше взять прозрачную кружку, которую надо ополоснуть кипятком. Перевернем кружку и поставим в тарелку с водой. Нам останется только наблюдать, как вода поднимается вверх.
Какая сила поднимает воду в прозрачной кружке? Эта сила называется атмосферное давление. С помощью кипятка мы нагрели в кружке воздух, давление его возросло, часть газа вышла наружу.
Когда воздух снова остыл, но при охлаждении его давление уменьшилось, под стакан вошла вода, вгоняемая туда давлением наружного воздуха.
Опыт Рене Декарта или пипетка-водолаз
Сегодня Леонардо пришел нарядный, он «светился» от счастья. Оказывается именно сегодня исполнялось триста лет одному замечательному опыту — опыту Рене Декарта. И Леонардо пообещал нам показать этот опыт.
Он взял пластиковую бутылку с пробкой, пипетку и, как обычно, воду. Наполнил бутылку водой, оставив два-три миллиметра до края горлышка. В пипетку ученый набрал немного воды и опустил в горлышко бутылки. Она должна своим верхним резиновым концом быть на уровне или чуть выше уровня воды в бутылке. При этом нужно добиться, чтобы от легкого толчка пальцем пипетка погружалась, а потом сама медленно всплывала. Закрыв пробку и сдавив бока бутылки, Леонардо наблюдал, как пипетка пойдет на дно бутылки. А если ослабить давление на бутылку, пипетка снова всплывет.
Рис. 17. Пипетка — водолаз.
Как же объясняет это чудо Леонардо?
— Дело в том, что мы немного сжали воздух в горлышке бутылки, и это давление передалось воде. Вода проникла в пипетку — она стала тяжелее (так как вода тяжелее воздуха) и утонула. При прекращении давления сжатый воздух внутри пипетки удалил лишнюю воду, наш «водолаз» стал легче и всплыл. Если в начале опыта «водолаз» вас не слушается, значит, надо отрегулировать количество воды в пипетке. Когда пипетка находится на дне бутылки, легко проследить, как от усиления нажима на стенки бутылки вода входит в пипетку, а при ослаблении нажима выходит из нее.
Опыты с различными жидкостями.
«Башня плотности»
Можно ли заставить предметы зависать в толще жидкости? Давайте попробуем провести эксперимент. Для проведения опыта нам потребуется следующее:
— высокий узкий стеклянный сосуд, например, пустая чистая пол-литровая банка (можно взять банку из-под консервированных оливок или грибов);
— 1/4 стакана (65 мл) кукурузного сиропа или меда;
— пищевой краситель любого цвета;
— 1/4 стакана водопроводной воды;
— 1/4 стакана растительного масла;
— 1/4 стакана медицинского спирта;
— разные мелкие предметы, например, пробка, виноградина, орех.
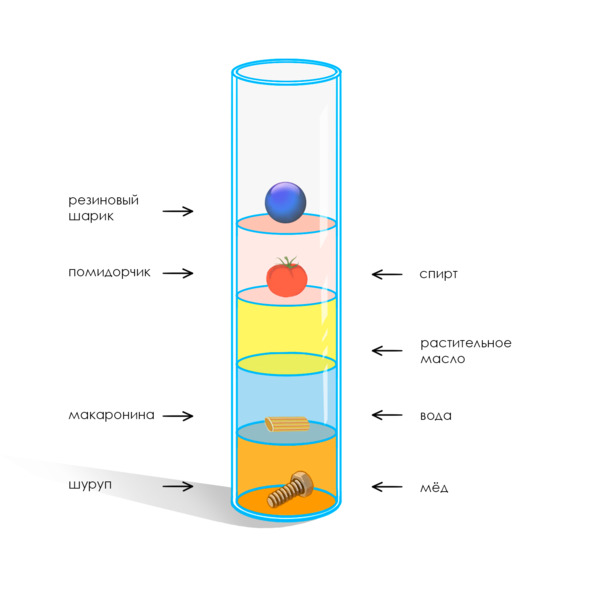
Наполним банку в следующем порядке:
— наливаем на дно банки мед, опускаем шуруп;
— приливаем немного воды и погружаем аккуратно макаронину;
— приливаем растительное масло и погружаем небольшой помидор;
— доливаем спирт и опускаем резиновый мячик.
В результате мы получаем выстроенную по плотности каждой жидкости «башню». Оказывается, что не все жидкости имеют одинаковую плотность. Самым тяжелым оказался мед, растительное масло легче воды и не смешивается с ней, спирт не будет смешиваться с растительным маслом.
Рис. 18. Башня плотности.
Эксперимент «Кипение» холодной воды»
Фокусник заболел и попросил ученого Леонардо показать опыты, так как билеты в цирк распроданы. Давайте ему поможем. Но фокусник оставил только плотную ткань, стеклянный стакан воды, резинку. Что же с этим «богатством» делать? Леонардо придумал! Делаем, как он говорит!
Сначала намочите и выжмите ткань. Налейте полный стеклянный стакан холодной воды. Накройте стакан платком и закрепите его на стакане резинкой. Продавите пальцем середину ткани так, чтобы он на 2—3 см погрузился в воду. Переверните стакан над раковиной вверх дном. Одной рукой держите стакан, другой слегка ударите по его дну. Вода в стакане начинает бурлить («кипит»).
Получилось? Давайте узнаем, как это получается.
Оказывается, мокрая ткань не пропускает воду. Когда мы ударяем по стакану, в нём образуется вакуум, и воздух через носовой платок начинает поступать в воду, всасываемый вакуумом. Вот эти-то пузырьки воздуха и создают впечатление, что вода «кипит».
Эксперимент «Мыльный пузырь»
Леонардо загадал нам загадку.
В мыльной воде родился
В шарик превратился
К солнышку полетел
Да не долетел, лопнул.
(Мыльный пузырь).
Давайте узнаем, почему