автордың кітабын онлайн тегін оқу Патофизиология сельскохозяйственных культур
Информация о книге
УДК 68.01
ББК 48.3я7
К76
Автор: Кошкин Е. И., доктор биологических наук, профессор кафедры физиологии растений РГАУ-МСХА им. К. А. Тимирязева; известный специалист по физиологии продукционного процесса и стресс-физиологии растений.
Рецензенты: Кузнецов В. В., доктор биологических наук, профессор, директор Института физиологии растений РАН, чл.-корр. РАН;
Джалилов Ф. С.-У., доктор биологических наук, профессор кафедры защиты растений РГАУ-МСХА им. К. А. Тимирязева.
В учебном пособии рассмотрены нарушения физиологических процессов у растений под действием биотических и абиотических факторов, оценена их роль в формировании урожая и его качества. Приведены визуальные симптомы некоторых наиболее распространенных заболеваний. Изложены сведения о биохимии иммунитета растений. Особое внимание уделено использованию физиологических показателей в селекции на урожайность и качество урожая растений при патогенезе. Дано физиологическое обоснование некоторых приемов химической защиты растений от болезней и вредителей, показаны возможности использования для этих целей индукторов устойчивости. Приведены данные по генетической инженерии полевых культур с целью повышения устойчивости к инфекционным и неинфекционным заболеваниям.
Предназначено для студентов агрономических специальностей, обучающихся по программам магистратуры, а также аспирантов, преподавателей, научных сотрудников, работников сельского хозяйства.
УДК 68.01
ББК 48.3я7
© Кошкин Е. И., 2015
© ООО "Проспект", 2015
150-летию Тимирязевки (1865–2015 гг.) посвящается
Введение
Патофизиология растений, или фитопатофизиология, изучает структурно-функциональные нарушения, обусловленные действием биотических и абиотических факторов, и их влияние на формирование урожая. Биотические факторы (вредители, болезни) вызывают инфекционные заболевания, а абиотические (гипо- и гипертермия, аноксия и гипоксия, засоление, засуха, кислотные осадки и др.) — неинфекционные. Даже по достаточно скромным оценкам, потери урожая в зависимости от культуры, вида действующего стрессора и его напряженности могут составить 50–70% и более. Особенно вредоносным может оказаться одновременное поражение посевов обеими группами болезней, причем в этом случае обработка посевов, например, против грибных патогенов фунгицидами, что на практике в течение сезона обычно происходит многократно (иногда до 10 раз), может оказаться абсолютно неэффективным. Это объясняется глубокими нарушениями обмена веществ, особенно процессов, связанных с генерацией энергии и ее тратами на адаптацию к новым условиям. Все это указывает на важность оценки физиологического состояния растений перед принятием решений о проведении защитных мероприятий. Необходимо также иметь в виду, что неквалифицированное использование против вредных организмов в посеве (вредители, патогены, сорные растения) химических средств защиты растений (инсектициды, фунгициды, гербициды) может быть далеко не безвредным для самих культурных растений и оказать отрицательное влияние на основные физиологические процессы (водный обмен, фотосинтез, дыхание, транспорт ассимилятов, минеральное питание, рост и др.) и, соответственно, продуктивность. Зачастую ситуацию не спасает даже не сплошная, как было принято ранее, а дифференцированная обработка посевов средствами защиты только по очагам сорных и больных растений в соответствии с технологией точного земледелия. Вышеизложенное со всей очевидностью ставит вопрос о важности систематизированных знаний современной литературы о физиологических основах защиты растений и в более частном порядке — о физиологических особенностях больного растения с целью включения искомых материалов в учебники (учебные пособия) для подготовки специалистов аграрного профиля.
Весомый вклад в исследования физиологии больного растения и проблем иммунитета, особенно активные во второй половине прошлого столетия, внесли сотрудники МГУ, Института экспериментальной ботаники им. В. Ф. Купревича АН БССР, Института биохимии РАН, НИИ фитопатологии РАН и целого ряда других учреждений. Полученные в тот период данные не потеряли своей актуальности и сегодня, в связи с чем автор неоднократно обращался к ним в ходе изложения материала.
Данное учебное пособие предназначено для магистрантов, обучающихся по направлению «Агрономия» и освоивших в рамках бакалавриата базовые программы по фитопатологии, энтомологии, физиологии и защите растений. В излагаемом материале основной акцент сделан на освещении комплексного характера влияния биотических и абиотических факторов на физиологические функции на разных уровнях организации, продукционный процесс, формирование урожая и его качество, а также описаны категории иммунитета растений. Кратко освещены механизмы действия указанных факторов, обсуждены возможности применения ряда антистрессовых препаратов с целью снижения негативного влияния неблагоприятных факторов на растения, а также повышенной пестицидной нагрузки на окружающую среду. Особое внимание уделено созданию устойчивых сортов (гибридов) с использованием методов классической селекции и биотехнологии. С учетом значительного прогресса, достигнутого в последние десятилетия в изучении возможной роли микоризных грибов в регуляции жизнедеятельности полевых культур в неблагоприятных условиях и, в частности, в защитных реакциях против патогенов, отдельная глава посвящена именно этой проблеме. Для лучшей идентификации симптомов заболеваний пособие иллюстрировано цветными фотографиями пораженных растений. Это важно, поскольку симптомы многих инфекционных и неинфекционных болезней весьма похожи. В конце книги приведены также названия болезней и возбудителей, встречающиеся в тексте.
Автор благодарит профессора кафедры защиты растений Джалилова Ф. С. и доцента кафедры физиологии растений Тимирязевки Пильщикову Н. В. за ценные предложения, высказанные при подготовке данного пособия, и надеется, что оно в определенной мере восполнит дефицит информации по данной проблематике. Весьма востребована была также техническая помощь Грачева Д. А., а в информационном обеспечении — сотрудников ЦНБ Тимирязевки и ЦНСХБ, особенно Гончаровой В. М.
Глава 1.
Актуальные проблемы современной защиты растений
Сельское хозяйство России несет огромные потери из-за вредителей, болезней и сорняков. Общая сумма ежегодных потенциальных потерь продукции растениеводства в пересчете на зерно составляет более 100 млн т. При этом наиболее высокие потери от конкуренции сорняков — 39,3 млн т, от вредителей — 27,4 млн т и возбудителей болезней — 34,9 млн т (Захаренко В. А., 2003).
В преимущественно техногенных системах земледелия ключевая роль отводится химическим средствам защиты растений, поскольку в условиях монокультуры и севооборотов с короткой ротацией, резкого уменьшения числа культивируемых видов растений и широкого использования генетически однородных сортов, применения высоких доз азотных удобрений и пестицидов многие механизмы саморегуляции и гомеостаза агробиогеоценозов оказываются разрушенными или подавленными. Так, при чрезмерном насыщении севооборотов зерновыми, техническими и даже зернобобовыми культурами, а также при переходе к беспахотной (нулевой) обработке почвы существенно ухудшается фитосанитарная ситуация, поскольку усиливаются накопление почвенной инфекции и восприимчивость растений к патогенам, резко возрастает поражение растений корневыми гнилями, увеличиваются масштабы семенной инфекции и т. д. Значительно повысила генетическую уязвимость агроценозов замена генетически разнообразных местных сортов новыми высокоурожайными сортами и гибридами с высокой степенью ядерной и цитоплазматической однотипности. К резкому ухудшению фитосанитарной ситуации приводят обеднение видового состава и генетического разнообразия агроэкосистем, подавление и разрушение в них структур и механизмов саморегуляции.
Хотя и известны примеры сдерживания развития отдельных заболеваний растений при поражении их разными патогенами, в большинстве случаев заражение растений одной болезнью повышает их восприимчивость к другой. Одновременно существенно ослабляется устойчивость агрофитоценозов и к действию абиотических стрессоров. В целом техногенно-интенсивные системы земледелия значительно усиливают опасность поражения агроэкосистем и агроландшафтов вредными видами, а следовательно – и их зависимость от применения пестицидов.
В последний период в нашей стране существенно расширились состав и ареалы наиболее вредоносных видов, резко возрос вирулентный потенциал ряда ранее слабопатогенных и малоизвестных возбудителей болезней. Так, во всех регионах интенсивного зернопроизводства России получил распространение септориоз (рис. 1), приводящий к потере 20% зерна и ухудшению его качества; отмечается массовое поражение серых хлебов гельминтоспориозом (рис. 2), ринхоспориозом (рис. 3) и снежной плесенью (рис. 4); прогрессирует поражение озимой пшеницы фузариозом (рис. 5), вредной черепашкой, хлебной пиявицей, злаковыми тлями; вследствие поражения антракнозом практически уничтожены посевы желтого люпина.
Увеличилась также вредоносность возбудителей болезней зерновых колосовых: ржавчинных грибов, корневых гнилей, фузариоза колоса (рис. 6), септориоза. Общий перечень представляющих экономическую опасность возбудителей болезней зерновых, зернобобовых, технических культур, картофеля, овощных, плодовых, ягодных, кормовых в России состоит из 285 видов. Он включает относительно небольшое количество экономически значимых видов и особо опасных, вызывающих чрезвычайные ситуации, видов возбудителей болезней зерновых культур: мучнистой росы (рис. 7), фузариоза колоса, ржавчинных грибов (рис. 8), септориоза, фомопсиса подсолнечника (риc. 9) и фитофтороза картофеля (Захаренко, 2003). Так, появившись в стране в 1990 г. в Ставропольском крае на площади 50 га, за десять лет фомопсис расширил свой ареал до 209,5 тыс. га. Эпифитотийное распространение фомопсиса уменьшило урожайность подсолнечника на Северном Кавказе в 2–3 раза (Санин, 2003).
В настоящее время вредная черепашка является в экономическом плане наиболее значимым вредителем пшеницы, так как даже при повреждении зерна на 2–3% оно уже непригодно для выпечки хлеба. Для борьбы с этим вредителем в мире ежегодно расходуют около 40 млрд долларов, что и в экологическом плане далеко небезопасно (Буссини, 2003).
Обострение фитосанитарной ситуации в условиях преимущественно химико-техногенных систем земледелия в значительной мере обусловлено действием самих пестицидов, создающих жесткий фон естественного отбора устойчивых к ним вредных видов. За последние 20 лет число устойчивых к инсектицидам видов удваивалось каждые 6 лет. К настоящему времени в мире зафиксировано повышение устойчивости к пестицидам более чем у 500 видов насекомых-вредителей, десятков видов возбудителей болезней и сорняков. Характерно, что довольно быстро преодолевается и устойчивость созданных методами трансгенеза сортов. К примеру, способные поражать Bt-устойчивые растения хлопчатника популяции хлопковой совки в условиях Китая появились уже после 18 генераций вредного вида.
Поскольку большинство типов инсектицидов не обладает избирательностью действия, при их использовании численность полезных насекомых обычно уменьшается на 20–70%, а структура фауны изменяется в пользу более вредоносных видов. Отмечается также синергический эффект резистентности или, наоборот, уязвимости растений, связанный с совместным развитием нескольких возбудителей на одной культуре. Так, получены данные об усилении развития септориоза при соответствующем поражении растений бурой ржавчиной. Появление резистентных к пестицидам биотипов паразитов и нарушение экологического равновесия в агроэкосистемах (как ответная реакция на широкое применение пестицидов) – одна из главных причин того, что темпы роста затрат на химические средства защиты растений в несколько раз опережают темпы прироста стоимости дополнительного урожая.
Интересно, что чем выше генетическая однородность сортов и гибридов, чем большие площади они занимают и чем больше лет подряд выращиваются, тем выше опасность их поражения болезнями и вредителями, в том числе за счет появления более вредоносных биотипов. Особенно уязвимы изогенные, в том числе клональные, потомства растений. Неслучайно наибольшая вредоносность сортовой и клональной специфичности вирусов, бактерий, грибов, членистоногих была продемонстрирована на яблоне, сливе, землянике, крыжовнике, винограде, ежевике, т. е. на вегетативно размножаемых культурах.
Снижение устойчивости растений к абиотическим стрессам обычно уменьшает их толерантность к действию биотических стрессоров, и наоборот. Так, применение высоких доз азотных удобрений на зерновых культурах, особенно при их загущении, способствует повышению восприимчивости растений к ложной мучнистой росе и ржавчине (Riley, 1973). Показано, что и численность отдельных видов вредителей (злаковая тля, трипсы, цикадки) на посевах озимой пшеницы при внесении высоких доз азотных удобрений значительно возрастала (Борщевская, 1972). Улучшение водного режима агроценозов за счет орошения благоприятствует размножению патогенов в такой же мере, как и росту растений (Yarwood, 1970). Вспашка и междурядная обработка, вегетативное размножение растений также значительно увеличивают распространение заболеваний, особенно вирусных (Blaszczak, 1964).
В США, где насчитывается около 10 тыс. видов вредных насекомых и клещей, интенсивную борьбу ведут в основном со 100 видами, причем на 10 из них затрачивается около 90% всех химических средств. Стремительный рост численности вредных видов, т. е. возникновение эпизоотии, обычно обусловлен тем, что применение пестицидов резко снижает количество их естественных врагов, восстановление численности популяций которых происходит значительно медленнее, чем их жертв. Так, на посевах сахарной свеклы при увеличении вредоносности свекловичной нематоды и тли (уничтожающих до 30% урожая) хищные нематоды, ограничивающие численность популяций указанных видов, не могут приспособиться к новым условиям и выпадают из состава местной фауны (Захаренко, 2003).
Главной причиной опустошительных эпифитотий на посевах пшеницы, овса, кукурузы, подсолнечника в 1950–1980 гг. явилось широкое распространение сортов и гибридов, характеризующихся высокой степенью ядерной и цитоплазматической однородности. Однако еще в 1920-е гг. высокоурожайные и генетически однотипные сорта пшеницы были поражены различными физиологическими расами стеблевой ржавчины на обширных площадях северной части Великих равнин США. При этом поражение стеблевой ржавчиной (расы 36, 38 и 49) широко возделываемого сорта Marquis в 1927 г. достигло масштаба эпифитотий. Введенный взамен новый сорт Ceres вскоре был поражен расой 56, распространение которой уже в 1935 г. стало повсеместным. Сорт Норе, сменивший Ceres, был «атакован» расой 15В. В 1953 г. стеблевая ржавчина поразила в США 65% всех посевов твердой пшеницы, а в 1954 г. — 75%, в результате чего было потеряно более 25% урожая пшеницы. Аналогичная картина наблюдалась и на посевах овса из-за появления новых рас стеблевой и бурой (листовой) ржавчины.
Массовое поражение в США кукурузы южным гельминтоспориозом в 70-е гг. XX в. связано с тем, что почти 90% посевных площадей под этой культурой были заняты гибридами, полученными на основе линий с цитоплазматической мужской стерильностью типа Texas, которая оказалась исключительно восприимчивой к Т-расе гельминтоспориоза. Эпифитотийный характер поражения генетически однородных посевов пшеницы и ячменя возбудителями мучнистой росы, ржавчины и пятнистости имел место в ФРГ, где, например, в 1977 г. на долю трех сортов озимой пшеницы (Jubilar, Diplomat, Caribo) приходилось свыше 70% площадей, а у яровой пшеницы генетически однотипные сорта занимали 96%. Практика показала, что наиболее эффективным средством предотвращения эпифитотий является увеличение генотипической вариабельности культивируемых видов и сортов растений, а также организация системы информации о появлении новых возбудителей болезней и вредителей в разных регионах мира, позволяющая своевременно начать «упредительную» селекцию.
В зонах, где возделываются устойчивые сорта пшеницы, гессенская муха (Mayetiola destructor Say) в 50-е гг. XX в. потеряла свое былое значение как массовый вредитель пшеницы (Пайнтер, 1953). Однако все больший вред стал приносить стеблевой хлебный пилильщик (Cephus pygmaeus L.). Ежегодно охватывая в России большие площади (около 8–10 млн га), он причиняет существенный ущерб урожаю. Различия в повреждаемости стеблей пшеницы хлебным пилильщиком для Северного Кавказа составили от 0 (сорта Рейхенбахин, Леукомеляноус, Апуликум, Либикум) до 40,1–43,9% (сорта Сивоуска, Альбидум 0721). В то же время на устойчивых сортах численность стеблевых хлебных пилильщиков снижается, по крайней мере, в 120–300 раз.
Широкое распространение неустойчивых сортов пшеницы явилось одной из основных причин изменения характера динамики численности вредной черепашки за последние 50 лет. Этот вредитель ежегодно в широких масштабах повреждает зерно пшеницы и создает постоянную угрозу посевам, особенно качеству зерна на Северном Кавказе, в Поволжье, на юге Украины и в некоторых других регионах. Установлено, например, что плодовитость самок вредной черепашки (Eurygaster integriceps Put) при питании в весенне-летний период растениями мягкой пшеницы сорта Безостая 1 составила 199 яиц, на дикой однозернянке — 70, на культурной однозернянке — 85, на пшенице зандури — 33 (в среднем за 3 года). Заметим, что устойчивость растений к вредителям обычно сохраняется на протяжении 20–30 лет, что намного превышает период толерантности сортов к патогенам. По данным Министерства сельского хозяйства США, рентабельность затрат на селекцию сортов, устойчивых к вредителям, во многих случаях достигает 300% (Шапиро, 1979).
В современном растениеводстве широкое использование сортов и гибридов растений, обладающих комплексной устойчивостью к патогенам, нередко оказывается единственной возможностью возделывания той или иной культуры. Считается, например, что без выращивания сортов озимого ячменя, устойчивых к вирусам желтой мозаики ячменя (Barley yellow mosaic virus) и слабой мозаики ячменя (Barley mild mosaic virus), которые переносятся почвенным грибом Polymyxa graminis и сохраняются в спорах гриба более 20 лет, возделывание озимого ячменя в большинстве регионов Германии было бы сегодня невозможно (Шпаар и др., 2002). Особенно большое значение имеет создание сортов и гибридов с комплексной устойчивостью (multiple resistance). Если отдельные возбудители занимают экологические ниши других патогенов, к которым сорт является устойчивым, требуется, несмотря на частичную устойчивость, применение химических средств. Для обеспечения устойчивости агроценозов должен быть создан многоэшелонированный набор сортов и гибридов, обладающих комплексной устойчивостью к действию биотических стрессоров.
Наряду с вертикальной и горизонтальной устойчивостью (по Ван дер Планку) различают и третий тип — выносливость (толерантность). Уровень выносливости растений как конститутивный признак обусловлен прежде всего экологическими и физиологическими особенностями конкретных видов хозяина (Дмитриев, 2003). Показано, например, что вклад разных органов растения в фотосинтез в период налива зерна различен. Так, у ржи основную роль в фотосинтетической продуктивности растения играют стебель и листовые влагалища, у пшеницы — лист и стебель, у овса — «лист-флаг» (Нальборчик и др., 1985). В зависимости от этого повреждение будет по-разному влиять на формирование урожая. К примеру, потери урожая у ржи даже при сильном поражении составляют около 20%. Однако короткостебельные сорта оказываются менее выносливыми (потери до 40%) (Кобылянский, Солодухина, 1982; Шакирзянов, 1990). Возможно, это связано с укорачиванием стебля, фотосинтез которого у данной культуры играет ведущую роль в процессе формирования зерна. Поскольку пшеница обладает меньшей способностью компенсировать снижение листовой поверхности, ее потери от ржавчины несколько выше, чем у ржи, и обычно составляют 20-30%, а при сильном поражении — до 50% (Чумаков, 1958; Roberts et al., 1984). Наименьшей выносливостью обладает овес, у которого обычные потери при эпифитотиях корончатой ржавчины (рис. 10) достигают 40–50%. Приведенные данные указывают на то, что выносливость растений зависит от архитектуры соответствующей культуры (Жученко А. А., 2004). Таким образом, знание физиологических особенностей культуры (сорта), а также их физиологического состояния должно стать непременным атрибутом грамотного построения системы мероприятий по защите растений от вредителей и болезней.
Контрольные вопросы и задания
1. Чем объясняется резкое ухудшение фитосанитарной ситуации в растениеводстве?
2. Назовите наиболее вредоносные виды вредителей и возбудителей болезней, вызывающих серьезные потери урожая и снижение его качества?
3. Каковы возможности использования химических средств защиты растений в борьбе с болезнями и вредителями?
4. К чему может привести односторонняя ориентация лишь на химические средства защиты растений?
5. Можно ли вывести сорта, устойчивые к вредителям и болезням, с использованием методов классической селекции?
6. Сочетаются ли устойчивости сорта к биотическим и абиотическим факторами?
7. В чем заключается опасность выращивания на больших площадях генетически однотипных сортов?
8. Как сказываются физиолого-биохимические особенности культур на поражаемости болезнями и вредителями?
Глава 2.
Нарушения физиологических процессов и формирование урожая у растений, пораженных инфекционными заболеваниями
По типу питания микроорганизмы разделяют на сапротрофов, некротрофов и биотрофов. Первые извлекают питательные вещества из мертвых тканей, т. е. являются сапрофитами, вторые и третьи — паразиты. Однако некротрофы, прежде чем оккупировать какой-либо участок растения, убивают его своими токсичными выделениями, т. е. фактически, как и сапротрофы, питаются содержимым мертвых клеток, а биотрофы извлекают питательные вещества непосредственно из живых клеток. Различия между ними заключаются в соотношении скоростей гибели зараженной ткани (некроза) и развития паразита в растении. Если некроз опережает распространение паразита, следовательно, тип питания – некротрофный, если же распространение паразита опережает некроз — питание биотрофное.
Существуют переходные формы между биотрофами и некротрофами — гемибиотрофы, которые имеют смешанное питание. Сначала они питаются биотрофно, а после гибели зараженной ткани продолжают развиваться в ней, питаясь некротрофно. Так, возбудитель парши яблони образует внутритканевый мицелий между мезофиллом и эпидермисом, не повреждая клеток (биотрофно), затем, после гибели клеток, распространяется в них некротрофно и, наконец, после отмирания и опадения листьев продолжает развиваться в них сапротрофно (Дьяков и др., 2001).
Для облигатных сапротрофов источником питательных веществ служат только мертвые органические субстраты. Факультативные сапротрофы при определенных условиях могут нападать на живые ткани, в частности на старые, ослабленные и поврежденные или на запасающие органы. К таким паразитам относятся, например, Botrytis cinerea, Rhyzopus nigricans и др. Факультативные сапротрофы — это организмы, которые обычно ведут паразитический образ жизни, но могут существовать и как сапротрофы. В качестве примера можно назвать Phytophthora infestans. Они имеют более узкий круг растений-хозяев и более выраженную специализацию. Облигатными паразитами называются организмы, например Erysiphales, живущие только как паразиты.
Возбудители болезней проникают в растения различными путями. Большая часть патогенов попадает в растения через естественные отверстия: устьица, чечевички, гидатоды (рис. 11). Такой путь присущ бактериям и некоторым грибам. Возбудители, относящиеся к факультативным паразитам, проникают в основном через различные механические повреждения. Некоторые грибы-возбудители настоящих мучнистых рос, цветковые паразиты могут внедряться через целостные покровные ткани, используя для их разрушения токсины и ферменты. Дальнейшее развитие проходит также в основном на поверхности пораженных растений. Часто гриб-биотроф обитает в межклетниках, а питательные вещества получает с помощью гаусторий (лат. haustor — пьющий, глотающий), присосок, врастающих в клетку. Такое сосуществование продолжается до спороношения гриба, после чего растение начинает повреждаться.
Бактерии и грибы в большинстве случаев распространяются от места инфекции на небольшие расстояния по межклетникам. Дальний транспорт их может проходить по сосудам вместе с пасокой (ксилемным соком). Вирусы перемещаются между клетками органа (ближний транспорт) по плазмодесмам, образовав комплекс со специальными белками-переносчиками. Дальний транспорт их происходит по флоэме, поэтому распространение инфекции зависит от скорости и направления флоэмного тока.
2.1. Изменение физико-химических свойств и функционирования клеток
Грибные, вирусные и бактериальные заболевания растений, как правило, сопровождаются существенными изменениями физико-химических свойств протоплазмы, в частности увеличением проницаемости пограничных слоев плазмы, в результате чего возрастает выход неорганических солей и органических соединений из клеток. Так, у растений пшеницы, пораженных ржавчиной, выход органических веществ из клеток возрастает до 5 раз.
Степень воздействия инфекции на проницаемость протоплазмы определяется устойчивостью растения. Так, при заражении картофеля раком проницаемость протоплазмы клеток клубней, ростков и корней у восприимчивых сортов, т. е. неспособных противостоять заражению и распространению патогена в тканях, повышалась, в то время как у устойчивых сортов практически не изменялась. При заражении хлопчатника вертициллезом экзоосмос из листьев устойчивых сортов оказался меньше, чем у восприимчивых сортов. Возрастание проницаемости пограничных слоев протоплазмы приводит к тому, что ряд веществ, выделяемых клетками, попадает в транспирационный ток, чем нарушаются осмотическое давление и тургор клетки. Токсины других патогенов также обладают способностью нарушать проницаемость мембран тканей растения-хозяина. Токсин гриба Нelminthosporium victoriae, например, многократно увеличивает выход электролитов из тканей колеоптилей овса неустойчивого сорта, практически не влияя на ткани устойчивого сорта. Способностью изменять проницаемость тканей растения обладают лишь патогенные штаммы паразитов. В экстракте листьев яблони, инокулированных вирулентным штаммом Erwinia amylovora, обнаружены значительные количества ионов (К, Na, Са, Р, Fe). Сапрофитные штаммы бактерии проницаемость листьев не изменяли.
Способность выделять в окружающую среду вещества, действие которых направлено на увеличение проницаемости протоплазмы растительных клеток, является важным оружием паразитов, облегчающим им использование питательных веществ клеток растения-хозяина. В тканях устойчивых растений подобные условия не создаются, и их способность сохранять проницаемость плазмы практически на уровне здоровых растений следует рассматривать как один из важных элементов защитной реакции. Поскольку проницаемость протоплазмы регулируется клеточными мембранами, изменение этого показателя под влиянием продуктов жизнедеятельности патогена должно быть связано с нарушениями структуры клеточных мембран. Действительно, как показывают электронно-микроскопические исследования, внедрение патогенов в клетку, а также обработка тканей растений токсинами приводят к потере мембранами клетки избирательной проницаемости.
Патогенные грибы, относящиеся к группе факультативных паразитов, образуют и выделяют в ткани растения-хозяина также экстраклеточные ферменты, которые принимают участие в распаде полимерных соединений клетки. Одним из следствий этого процесса может быть выход электролитов. Этим, в частности, объясняется увеличение электропроводности тканей цикория, пораженных бактериальной гнилью. При этом степень увеличения электропроводности соответствует интенсивности поражения. Однако основным продуктом индуцированного патогеном распада полимерных веществ являются растворимые органические соединения. Последние обогащают органическим веществом клеточный сок, вязкость которого, соответственно, увеличивается. Реакция различных сортов неодинакова: если у устойчивого сорта капусты Амагер незначительное увеличение вязкости клеточного сока, отмечаемое через 30 мин после инфильтрации токсина, с удлинением экспозиции практически не возрастает, то у восприимчивого сорта она за 44 ч увеличивается в 3,5 раза. Эти данные указывают на ясно выраженную способность тканей устойчивого сорта противостоять развитию гидролитических процессов, индуцируемых токсинами паразита. Усиление процессов распада в тканях, а следовательно, и понижение уровня их жизнедеятельности, сопровождается подщелачиванием клеточного сока, как, например, у тканей капусты, зараженных Botrytis cinerea. У неустойчивых сортов капусты pH клеточного сока при заражении сдвигается в щелочную сторону, в то время как у устойчивых сортов этот показатель практически не изменяется.
Иной характер воздействия на pH клеточного сока растения-хозяина свойствен облигатным паразитам. Так, под влиянием возбудителя рака картофеля Synchytrium endobioticum клеточный сок ростков и глазков картофеля подкисляется. Аналогичное влияние на pH клеточного сока пшеницы оказывает возбудитель мучнистой росы Erysiphe graminis. Инфекция вызывает также значительные изменения в свойствах коллоидов протопласта клеток растения-хозяина, в частности в структурной вязкости. Так, под воздействием токсина гриба Botrytis cinerea и отдельных активных веществ, выделенных из токсина, структурная вязкость протоплазмы тканей неустойчивого сорта хранящейся капусты снижается, что свидетельствует о нарушениях в свойствах коллоидов. В тканях устойчивого сорта не зарегистрировано никаких изменений структурной вязкости (Рубин, Ладыгина, 1974).
Патогены разрушают растение с помощью секретируемых ими токсинов, гормонов, гидролитических ферментов, взаимодействущих в клетках хозяина со своими мишенями, локализованными, как правило, в клеточных мембранах. В свою очередь, в клеточных стенках растения, а также в вакуоли содержатся ферменты хитиназа и β-1,3-глюканаза, разрушающие хитин и β-1,3-глюкан клеточных стенок грибов. При заражении активность этих ферментов увеличивается. При расщеплении хитина образуются вещества, обладающие антигрибной активностью.
По механизму действия токсины делят на две группы: токсины – ингибиторы ферментов и токсины, повреждающие мембраны. Токсины ряда патогенов способны деполяризовать плазмалемму растения, они влияют на транспорт ионов через мембраны, индуцируют потерю клеткой важных метаболитов, некоторые токсины сами являются источником активных форм кислорода (АФК).
Токсины передвигаются от места инфекции по растению, часто даже быстрее самого патогена, и создают условия для заражения других клеток. По химической природе токсины различны, среди них есть низко- и высокомолекулярные вещества: органические кислоты (щавелевая), кумарины, алкалоиды, циклические пептиды, состоящие из нескольких аминокислот, замкнутых в кольцо, гликопептиды и другие.
Низкомолекулярные токсины — это вторичные метаболиты (терпеноиды, гликозиды). Патогенный микроорганизм, обосновавшись в клетках растения-хозяина, начинает синтезировать их в больших количествах. Именно их вредное влияние на рост и метаболизм ведет растение к гибели.
К высокомолекулярным токсинам относятся пептиды, вызывающие у растений некрозы, а также экзоферменты. При заражении растений грибы и бактерии образуют и выделяют в наружную по отношению к ним среду большие количества различных гидролитических ферментов (пектиназы, целлюлазы, гемицеллюлазы, кутиназы), с помощью которых разрушают клеточные стенки, вызывают мацерацию тканей, повреждают мембраны, превращают вещества клетки в форму, удобную для питания патогена.
Синтез экзоферментов могут стимулировать компоненты клеточных стенок патогена или хозяина, образовавшиеся при разрушении кутикулы. Например, когда патогенный гриб Fusarium solani атакует растение гороха, споры гриба секретируют очень небольшое количество фермента кутиназы, которая вызывает частичный гидролиз кутикулы, покрывающей орган, в результате чего прорастающие споры гриба могут проникнуть внутрь.
Токсины выделяются патогеном в среду, если он является сапрофитом, и в ткани растения, если патоген — паразит. Токсины, выделямые некротрофами, убивают ткани растения; они не обладают специфичностью и способны повреждать многие растения. Эти токсины сами по себе не могут индуцировать болезнь. Наиболее полно симптомы болезни вызываются токсинами паразита, заражающего данный вид. Обнаружены токсины, повреждающие мембраны, нарушающие азотный и энергетический обмен, водный режим растений, обладающие хелатирующим действием.
Коллоиды неустойчивых форм растения отличаются низкой стабильностью свойств и легко подвергаются дезорганизующему влиянию токсинов паразита. Подтверждением этих выводов служит также изменение положения изоэлектрической точки коллоидов (ИЭТ) протоплазмы при заражении. Гриб Botrytis cinerea вызывал сдвиг ИЭТ коллоидов неустойчивого сорта капусты в кислую сторону, в то время как у устойчивого сорта ее положение не изменялось. Аналогичные результаты получены также для коллоидов тканей клубня картофеля, пораженных возбудителем рака Synchytrium endobioticum. Иные закономерности установлены для другого облигатного паразита — возбудителя мучнистой росы пшеницы. Оказалось, что положение ИЭТ белков восприимчивого сорта пшеницы не изменяется при заражении, в то время как у устойчивых сортов и видов пшениц она сдвигается в кислую сторону.
Инфекция вызывает также изменение гидрофильных свойств коллоидов протоплазмы. Степень гидрофильности коллоидов листьев неустойчивых сортов хлопчатника при заражении Verticillium dahliae резко снижается. При поражении картофеля ооспорозом наблюдается уменьшение водоудерживающей способности тканей на 8,8–13,7%. Аналогичные результаты получены для тканей капусты, пораженных Botrytis cinerea. Этот патоген вызывает также значительное увеличение набухаемости коллоидов тканей капусты, причем сильнее этот процесс выражен у неустойчивого сорта. Снижение водоудерживающей способности листьев растений ячменя наблюдается также при заражении Erysiphe graminis.
Характер влияния инфекции на различные органеллы клетки неодинаков и зависит от типа органеллы, устойчивости растения-хозяина, типа питания паразита и т. д. Типичной реакцией на инфекцию является изменение размеров органелл. Отмечено, в частности, уменьшение размеров ядер тканей лука под воздействием гриба Botrytis cinerea. На первых этапах заражения луковицы наблюдается сжатие ядер. По мере развития инфекции остов ядра делится на отдельные участки, а в зоне деструкции клеток (вблизи гиф) ядро исчезает окончательно. На расстоянии 2, 1 и 0,5 см от места внедрения гриба размеры ядер тканей лука, зараженного B. allii, уменьшались соответственно на 63, 82 и 100%. Фильтраты семидневной культуры паразита оказывали аналогичное действие.
Деформирующее воздействие культуральной жидкости B. cinerea на ядра тканей капусты сильнее сказывается на неустойчивом сорте. Иной характер воздействия на ядра клеток растения-хозяина свойственен облигатным паразитам. Эта группа патогенных грибов на первых этапах заражения оказывает мягкое воздействие на ткани растения-хозяина, вызывая иногда даже активирование процессов обмена веществ у последнего. Очевидно, этим и объясняется наблюдавшееся в одном из опытов увеличение ядер и ядрышек листьев пшеницы на 6-й день после заражения ржавчиной и полное их разрушение к 15-му.
Под влиянием инфекции может изменяться также содержание основных белков ядер — гистонов. В частности, отмечено уменьшение содержания гистонов в ядрах пшеницы при ржавчинной инфекции.
Инфекция вызывает также значительные изменения свойств и размеров пластид. Культуральная жидкость Botrytis cinerea, инфильтрированная в ткани капусты, приводит к разбуханию пластид, более значительному у восприимчивого сорта. Напротив, вирусы, поражающие различные растения из семейства крестоцветных, вызывают вакуолизацию и разрушение пластид, а также уменьшение их количества в инфицированных тканях. В листьях кукурузы и сорго, пораженных вирусом карликовой мозаики, также уменьшаются количество хлоропластов в клетках паренхимы (на 17%) и их размеры. Отмечено уменьшение размеров, обесцвечивание и слипание хлоропластов в тканях различных растений, пораженных облигатными и факультативными паразитами, а также вирусами.
Дезинтеграцию тилакоидной системы хлоропластов неустойчивого вида табака Nicotiana tabacum под влиянием вируса табачной мозаики наблюдали Ладыгина и Балнокин (1970). Ультраструктура хлоропластов иммунного вида табака в этих условиях не нарушалась. В зоне, окружающей некроз, увеличивается число хлоропластов, они содержат больше рибосом, наблюдается их деление. Нарушение структуры хлоропластов вызывают также патогенные бактерии. Уже через 18 часов после инфильтрации в ткани листьев яблони суспензии клеток Erwinia amylovora наблюдается дезорганизация ламеллярной структуры хлоропластов.
Под влиянием патогенов изменяются также свойства хлорофилл-белкового комплекса пластид. Так, вирус табачной мозаики (ВТМ) приводит к ослаблению связи хлорофилла с белком в листьях Nicotiana tabacum. В результате извлекаемость пигментов хлоропластов петролейным эфиром увеличивается также при поражении различных растений патогенными грибами, как факультативными, так и облигатными.
Реакция «сверхчувствительности», или СВЧ реакция (см. гл. 3), наблюдаемая в листьях табака при внедрении в них бактерии Erwinia amylovora, сопровождается прогрессирующей денатурацией структурных белков ламелл хлоропластов, что выражается в уменьшении растворимости белков и их способности связывать фосфолипиды. Наряду с этим у восприимчивого к гельминтоспориозу сорта риса наблюдаются количественные изменения аминокислот хлоропластов при заражении. В частности, уменьшается содержание глицина, аспарагиновой и глутаминовой кислот, возрастает количество аргинина, гистидина, тирозина, лейцина, серина, аланина и пролина. Изменения структуры хлоропластов влекут за собой и изменение активности процессов фотосинтеза (см. гл. 2.3).
Хлоропласты, обладая активной системой синтеза белка, интенсивно включают меченые аминокислоты в белок. В период интенсивного размножения ВТМ в листьях табака наблюдается снижение включения Н3-аминокислот в белки, а также Р32 — в РНК рибосом хлоропластов. Подавление процесса синтеза белка в хлоропластах, как и торможение синтеза рибосомальной РНК хлоропластов, индуцированное вирусом, может быть главной причиной наблюдающегося при этом хлороза листьев.
Значительные изменения под влиянием инфекции претерпевают также митохондрии, причем заболевание сопровождается увеличением количества митохондрий в инфицированных тканях. В результате заражения фузариозным вилтом в стеблях растений томата значительно возрастает содержание митохондриального азота. В тканях батата, пораженных Ceratocystis fimbriata, увеличивалась активность цитохромоксидазы. Эта реакция наблюдалась на расстоянии 3–4 мм от места заражения.
Серьезно нарушается также структура митохондрий инфицированных тканей. Так, при поражении вики вирусом желтой мозаики бобовых матрикс митохондрий становится электронноплотным, а кристы разбухают и изменяют форму, принимая вид овальных или прямоугольных блоков с искривленными стенками. В ультраструктуре клеток мезофилла листьев табака, пораженных ВТМ, не обнаружено структурных изменений митохондрий у неиммунного вида табака на начальных этапах воздействия вируса (48 часов), хотя в это время уже наблюдаются сдвиги в их способности к окислительному фосфорилированию. На 7-й день после инокуляции митохондрии Nicotiana tabacum подвергаются дезинтеграции, кристы разбухают, а их содержимое становится более электроннопрозрачным. У иммунного вида табака в зоне, прилегающей к некрозу, наблюдается увеличение содержания митохондрий, а также возрастает число крист. Эти изменения способствуют повышению уровня метаболизма таких тканей и более успешному использованию защитных ресурсов.
Нарушение структуры митохондрий, в том числе митохондриальных мембран, приводит к изменению их проницаемости. Так, ВТМ вызывает увеличение проницаемости мембран митохондрий у неустойчивого вида табака. При этом увеличивается выход эндогенной АТФ из митохондрий, а также скорость набухания органелл. У иммунного вида табака эти показатели не изменяются. Увеличение проницаемости мембран митохондрий является причиной набухания этих органелл клетки при заражении. В тканях восприимчивого к ВТМ вида табака размеры митохондрий увеличивались примерно на 35% через 60 дней после инокуляции вирусом, практически не изменяясь у иммунного вида. Основная масса митохондрий здоровых тканей имеет размеры около 2,25 мк, увеличиваясь при заражении у неустойчивого сорта до 2,45 мк и оставаясь без изменений у устойчивого сорта.
Значительные изменения, вызываемые инфекцией в структуре митохондрий, сказываются также на биосинтезе белка. Митохондрии из листьев табака, пораженных ВТМ, более активно включали С14-лейцин в белки, по сравнению со здоровыми тканями. Инфекция вызывает значительное увеличение скорости включения 14С-лейцина в белки митохондрий устойчивого сорта Амагер и небольшое — у неустойчивого сорта (Рубин, Ладыгин, 1974).
Облигатные паразиты также вызывают увеличение синтеза рибосомальной РНК. В тканях пшеницы, зараженных ржавчиной, включение Р32 во фракцию рибосомальной РНК увеличивалось на 80—100%. Аналогичная тенденция отмечена в тканях пшеницы и фасоли. В работе Рубина с сотр. (1971) установлено, что в тканях растений огурца под влиянием мучнистой росы изменяется количество рибосом, причем направление этих изменений зависит от устойчивости сорта: в тканях восприимчивого сорта огурца содержание рибосом при заражении снижается, в то время как у устойчивого сорта — увеличивается.
Вирусы также оказывают влияние на количество этих органелл. Так, в листьях китайской капусты, зараженных вирусом желтой мозаики, содержание 83S рибосом увеличивалось, количество же 114S полирибосом при этом не изменялось. Из тканей гипокотилей фасоли через 42 ч после инокуляции вирусом коровьего горошка экстрагировалось в 1,5 раза больше рибосом, чем из тканей здоровых растений. При этом содержание моно- и полирибосом изменялось одинаково.
Таким образом, структура протопласта теснейшим образом связана с протекающими в клетке биохимическими процессами. Воздействие токсинов, выделяемых паразитом, вызывает целую цепь взаимообусловленных изменений физико-химических свойств и метаболических функций протопласта. Характер этих изменений определяется, помимо свойств патогенного агента, биологическими особенностями растения-хозяина, степенью его восприимчивости или резистентности.
2.2. Водный обмен
Заболевание растений, как правило, сопровождается некоторым обезвоживанием тканей. Однако симптомы нарушений водного баланса и их причины при отдельных заболеваниях не одинаковы. Различают ряд факторов, влияющих на потерю воды больными растениями. Основные из них — это усиление транспирации, связанное с повреждением поверхностных тканей растения, и нарушение поступления воды вследствие повреждения корней или сосудистой системы. Одной из причин уменьшения проходимости проводящих путей является разрастание мицелия паразита в полости сосудов (рис. 12). Как показали анатомические исследования, при трахеомикозном увядании хлопчатника гифы Verticillium образуют в сосудах стебля значительные скопления, которые, однако, не могут полностью прекратить ток воды, как и мицелии Fusarium. Причиной частичной закупорки сосудов могут служить также токсины, выделяемые паразитом. Под их влиянием клетки сердцевинных лучей образуют в полости сосудов своеобразные выросты — тиллы, что, в частности, обнаружено в сосудах хлопчатника, пораженного вилтом. Тиллы формируются в нормальных условиях или в ответ на заражение. Они задерживают проникновение грибов по сосудам в другие органы растения.
Часто тиллы возникают в сосудах на большом протяжении, приводя к их полному закупориванию. Поражение корней и стеблей грибными и бактериальными болезнями также снижает поглощение и восходящий транспорт воды (рис. 13 и 14). Кроме того, грибная инфекция листьев может приводить к неэффективной потере воды при транспирации (рис. 15).
Для многих видов растений, инфицированных патогенами, характерно изменение проницаемости клеточных мембран корней. В результате снижается способность клеток перецикла и кортекса поглощать и транспортировать ионы в ксилему и устанавливать, таким образом, нормальный осмотический градиент, по которому могла бы двигаться вода. В клетках корня перца, инфицированного вирусом, изменения в проницаемости мембран были установлены по выходу К+ и Na+ за 24–48 часов до появления визуальных симптомов увядания. Искомые изменения предшествовали снижению ИД на 12–24 часов, а цитологические изменения — на 24–48 часов, что подтверждает ключевую роль проницаемости мембран в патогенезе. Вместе с тем в систематически поражающихся листьях не обнаружено изменений проницаемости, и причиной завядания является скорее невозможность для воды достичь ксилемы быстрее, чем произойдет блокирование транспорта воды непосредственно в ксилеме. В клетках гипокотиля подсолнечника поражение белой гнилью, вызванное Sclerotinia sclerotiorum, снижало проницаемость мембран для воды и ионов, в результате чего пораженные растения оказались не в состоянии адаптироваться к дефициту воды (Hancock, 1972).
Гибель клеток инфицированного корня не оказывает немедленного влияния на поглощение воды, которое может продолжаться в течение некоторого времени по неживым клеткам. Однако при этом из-за потери селективности при поглощении ионов в тканях может возникнуть серьезный дисбаланс ионов. Изучение специализированного корневого паразита (Ophiobolus graminis), вызывавшего офиоболез у зерновых, показало, что вторжение в живые клетки флоэмы представляет особенно существенный элемент инфицирования корня (Clarkson et al., 1975). Оно снижало транспорт 36Rb в апикальную меристему корня, в результате чего прекратился рост корня растяжением, а через два-три дня — транспорт ионов из наружного раствора в ксилему. Оба процесса связаны с углеводным голоданием, причем транспорт 14С углеводов в апексы корня из пораженных зон прерывался.
В полевых условиях обезвоживание является самым очевидным симптомом поражения растений офиоболезом. Зародышевые корни сильнее всего поражались этим грибом, что проявилось в замедлении их роста. Однако это компенсировалось лучшим развитием придаточных корней. Кроме того, тормозился рост молодых листьев растяжением. Подобная специфика роста листьев и корней инфицированных растений обусловлена индуцированным патогеном водным стрессом и указывает на важность учета взаимодействия донора (лист) и акцептора (корень) при анализе особенностей водного режима больных растений. При этом необходимо иметь в виду, что у здорового растения растяжение листа является одним из наиболее чувствительных к водному дефициту процессов.
Не менее важную роль играет возникающее под влиянием ферментов паразита расщепление пектиновых веществ, заключенных в прилегающих к сосудам клетках. Из поврежденных клеток освобождаются фенольные вещества, окисляющиеся и конденсирующиеся до меланинов. Вместе с коллоидным раствором пектата кальция продукты окисления дубильных веществ образуют темноокрашенные студнеобразные пробки в сосудах, в результате чего транспирационный ток значительно замедляется. Так, скорость транспорта пластических веществ по ксилеме стеблей томата, пораженного фузариозом, составляет 0,01 см/сек, тогда как для здоровых растений эта величина равна 0,25 см/сек, т. е. в 25 раз быстрее. Интенсивность транспирации снижается при этом только втрое.
Токсины патогена понижают водоудерживающую способность протоплазмы и увеличивают проницаемость ее пограничных слоев. В результате их действия наблюдается резкий подъем транспирации, приводящий к значительному водному дефициту в тканях растений. Считается, что под влиянием токсина клетки растения выделяют большое количество воды, поступающей в транспирационный ток. Однако основная роль в явлениях увядания принадлежит не потере воды, а снижению осмотического давления клеток. Вследствие нарушения избирательной проницаемости мембран осмотически активные вещества клеток поступают вместе с водой в транспирационный ток, и клетки теряют тургор. Увядание растений под влиянием токсина может наступать даже в атмосфере, насыщенной влагой.
Интенсивность транспирации (ИТ) оказывает решающее влияние на водный баланс растительных тканей, причем ее изменения при отдельных заболеваниях не всегда однотипны. Факультативные паразиты обычно повышают интенсивность транспирации пораженных органов. Инфицирование ржавчиной также сопровождается в большинстве случаев повышением транспирации, что обусловлено повреждениями покровных тканей и изменениями характера устьичных движений. Первое обычно приводит к усилению кутикулярной транспирации и ослаблению устьичной. Например, при заражении ячменя Erysiphe graminis f. sp. hordei кутикулярная транспирация увеличивалась и составляла 50% от общей транспирации, в то время как у здоровых растений на долю кутикулярной транспирации приходится лишь 10–20%. У томата, пораженного бактериальной пятнистостью (рис. 16), заболевание не только увеличивает устьичную аппертуру (в среднем на 30%), но и нарушает нормальный режим устьичных движений. Кроме того, больные растения теряют способность снижать отрицательное действие высоких температур путем регуляторного уменьшения аппертуры устьиц. Последняя увеличивается также у листьев картофеля при поражении фитофторозом, причем в темноте такие устьица не закрываются, что заметно усиливает потери воды.
Патогены, вызывающие увядание растений, обычно снижают транспирацию. Так, у картофеля, пораженного вертициллезным увяданием (рис. 17), наблюдается снижение как устьичной, так и кутикулярной транспирации. Нарушается также ее суточная периодичность вследствие меньшей потери воды в дневное время. Завядание растений в данном случае является результатом не повышенной потери воды листьями, а нарушения ее поступления в них. Поражение фасоли Uromyces phaseoli уменьшало открытость устьиц в 2,5–5 раз, что снижало на 35% интенсивность транспирации. Кроме того, при прогрессировании заболевания может уменьшаться транспирационная поверхность вследствие развития некротических пятен на листьях или отмирания части листового аппарата. Снижение интенсивности транспирации у томата, зараженного Fusarium oxysporum f. sp. lycopersici, связано с понижением проницаемости сосудов ксилемы для воды (Duniway, 1971). В ряде случаев зависимость интенсивности транспирации от заболевания носит более сложный характер. В частности, листья фасоли, пораженные мучнистой росой или ржавчиной, обычно транспирируют сильнее ночью и слабее днем, чем листья здоровых растений.
Интенсивность транспирации больного растения часто зависит от степени развития болезни. Так, на первых этапах заражения ячменя мучнистой росой (7–8-й день) транспирация зараженных листьев была ниже таковой у здоровых. Когда пораженная часть листа достигала 50%, наблюдались повреждения кутикулы, общая потеря воды увеличивалась.
Патогены и продукты их жизнедеятельности могут нарушать и другие стороны водообмена растения. В частности, полисахариды, являющиеся составной частью многих токсинов, вызывают механическую закупорку межмицеллярных пространств клеточных стенок и конечных разветвлений сосудов. В результате нарушаются обе стороны водообмена — как поступление, так и отдача воды, что приводит к необратимому увяданию при почти неизменном содержании воды в растении.
При вертициллезном вилте хлопчатника наблюдается снижение транспирации, скорости поглощения воды и прохождения растворов через стебли. Эти изменения отчетливо выражены у неустойчивых и среднеустойчивых сортов хлопчатника. У устойчивых сортов изученные показатели практически не изменялись.
Целый ряд листовых патогенов, воздействуя на устьичную и кутикулярную транспирацию, оказывает значительное влияние на эффективность использования воды на уровне целого растения, характеризуемую продуктивностью транспирации (ПТ) (Ayres, 1981). Так, поражение корончатой ржавчиной растений овса, выращиваемых в теплице, снижало ПТ (г сух. массы / кг Н2О) на 50%, по сравнению с непораженными. При заражении восприимчивых растений, начиная с фазы проростков, ПТ с учетом надземной массы составила 3,1 и 1,7 соответственно для здоровых и для пораженных растений. Различия между ними резко возрастают при расчете ПТ на массу зерна, поскольку Кхоз в искомых вариантах составил 0,40 и 0,02. В результате ПТ снизилась от 0,88 до 0,04 г/кг Н2О, т. е. на 95%, или в 22 раза. Полученные данные характеризуют эффективность использования воды при экстремально сильном инфицировании растений, нереальном на практике. Однако даже при умеренной пораженности ПТ в расчете на массу зерна оказалась на 40% ниже, чем у здоровых растений. Аналогичные тенденции отмечены также при сравнении АТО здоровых и зараженных растений ячменя, пшеницы, фасоли, тыквы и других культур. Однако ассимиляционно-транспирационное оношение (АТО), рассчитываемое как соотношение интенсивностей фотосинтеза (ИФ) и транспирации, определяется путем их измерения на свету и не характеризует потенциальные потери воды за ночной период, когда устьица у больных растений частично открыты. В этом отношении интересные результаты получены при изучении газо- и влагообмена растений у 10 сочетаний растения-хозяина и патогена при поражении листьев (Shtienberg, 1992). Вне зависимости от типа патосистем, ИФ изменялась примерно однотипно — уменьшалась линейно с увеличением натурального логарифма степени поражения листьев. Однако снижение было больше, чем можно было ожидать на основании только определения площади непораженных участков листа. Что касается относительной транспирации, равной соотношению ИТ больного и здорового растений, степень снижения определялась патосистемой, что частично зависело от типа трофических связей между патогеном и растением-хозяином. Так, при низкой пораженности (< 10%) ржавчиной ИТ у больных растений кукурузы и пшеницы оказалась даже выше, чем у здоровых. При сильном поражении ИТ снизилась, но в меньшей мере, чем ожидалось, исходя из доли пораженной поверхности листьев. Грибные патогены, вызывающие некротические повреждения у хлопчатника, снизили ИТ до ожидаемых величин, а мучнистая роса у пшеницы — гораздо более сильное уменьшение транспирации. Таким образом, АТО, определенное на свету, может снижаться при поражении ржавчиной, повышаться — при поражении мучнистой росой и практически не меняется при инфицировании грибными патогенами, вызывающими некрозы (Grimmer et al., 2012).
Устьица являются одним из основных путей проникновения патогенов в растения. Для большинства сочетаний патогенов и растения-хозяина установлено уменьшение устьичной апертуры листьев в ответ на инфицирование, за исключением поражения оомицетами. Причиной закрывания устьиц является, как правило, повреждение фотосинтетического аппарата (Meyer et al., 2001). Так, тентоксин, образуемый грибами Alternaria alternata, ингибирует АТФ-азу хлоропластов, что вызывает необратимое закрывание устьиц (Dahse et al., 1990). Как и ИФ, устьичная апертура уменьшается при воздействии целого ряда компонентов, накапливающихся в ответ на патогенез: салициловой кислоты (Chaerle et al., 1999), моноксида азота (NO) (Neill et al., 2002; Del Rio et al., 2004; Mur et al., 2005), фeнольных соединений (Plumbe et al., 1986) и фитогормонов — АБК и ауксина (Grabov, Blatt, 1998). Снижение ИФ в патогенезе, в свою очередь, обусловлено уменьшением активности РБФ-карбоксилазы/оксигеназы и проводимости мезофилла для молекул СО2 (см. гл. 2.3).
При инфицировании растений ячменя гемибиотрофом Rhynchosporium secalis (рис. 3) и дальнейшем прогрессировании болезни в сторону споруляции доля устьиц, не закрывающихся в темноте, возрастала, в cравнении со здоровым растением (Ayres, Jones, 1975). Это может быть обусловлено тем, что в результате синтеза цитокинина гемибиотрофом его содержание в пораженных листьях резко возрастает. Это в конечном итоге вызывает открывание устьиц у ячменя. Интересен в этом отношении факт сохранения устьиц кормовых бобов открытыми ночью при инфицировании растений некротрофом склеротинией, синтезирующей оксалат, который и не позволяет устьицам закрыться. Это подтверждено на оксалат-дефицитных грибных мутантах, которые резко уменьшили открытость устьиц растений в темноте и, соответственно, их восприимчивость к патогену (Guimaraes, Stotz, 2004). Важно отметить, что АБК — зависимое закрывание устьиц у здоровых листьев при обработке оксалатом заметно снизилось. Это указывает на то, что в условиях засухи устьица у пораженных листьев закрываться не будут, что может усугубить проблему водообеспеченности больных растений.
Таким образом, изменения водного режима клеток растения, возникающие под воздействием паразита, являясь одним из основных симптомов при ряде заболеваний, оказывают многостороннее влияние на растение-хозяин и нередко могут стать основной причиной его гибели.
2.3. Фотосинтетическая активность
Заболевание растений в большинстве случаев сопровождается значительным снижением ИФ, что может вызываться разнообразными причинами. При многих заболеваниях, вызываемых факультативными паразитами, фотосинтез снижается вследствие частичного отмирания листовой ткани. Так, при поражении мучнистой росой ассимилирующая поверхность листа покрывается налетом мицелия, что уменьшает освещенность и, соответственно, фотосинтез (рис. 7).
Под воздействием большинства фитопатогенных грибов снижается содержание хлорофилла в листе, что, в частности, отмечено у хлопчатника при вертициллезном увядании. Соотношение содержания хл. а/хл. b при этом не изменяется. Уменьшение содержания хлорофилла в тканях растений вызывают также ржавчина и вирусы, причем содержание обеих форм хлорофилла снижается в одинаковой степени. Вместе с тем мучнистая роса, вызывая уменьшение содержания хл. а в листьях ячменя, не оказывала влияния на содержание хл. b (Paulech, Haspelova-Horvatovicova, 1970). Снижение содержания хлорофилла связано с разрушением хлоропластов под воздействием паразитических микроорганизмов. Один из основных путей распада хлорофилла в инфицированных тканях — гидролиз связей хлорофилла с белком, катализируемый протеолитическими ферментами. Так, на примере растений томата, пораженных возбудителем оливковой пятнистости Cladosporium fulvum, показано снижение содержания хлорофилла в пораженных листьях по мере увеличения активности протеолитических ферментов. Разрушению хлорофилла способствует также активирование хлорофиллазы при заражении. В частности, в семядольных листьях огурца при заражении вирусом мозаики возрастает активность хлорофиллазы и резко снижается содержание хлорофилла (Baillis, 1970). Уменьшение содержания хлорофилла в инфицированных тканях может явиться также результатом нарушения процессов его биосинтеза. Так, ВТМ вызывает снижение содержания хлорофилла в листьях неустойчивого вида табака на фоне одновременного подавления активности дегидратазы 6-аминолевуленовой кислоты — фермента, катализирующего конденсацию двух молекул 6-аминолевуленовой кислоты в молекулу порфобилиногена, предшественника порфирина (Рубин, Ладыгина и Тукеева, 1974).
Вместе с тем есть заболевания, при которых содержание хлорофилла в тканях, окружающих очаг инфекции, напротив, повышается. Наблюдается образование так называемых «зеленых островков», что характерно для заболеваний, вызываемых облигатными паразитами и вирусами (см. раздел 2.8.2). Эти участки ткани отличаются повышенным содержанием крахмала, а также усилением в них процессов синтеза белка и активности гликолатоксидазы. «Зеленые островки» фиксируют в пять раз больше 14СО2 при фотосинтезе, по сравнению с незараженной тканью, в них сохраняется хлорофилл и задерживается разрушение хлоропластов.
Снижение ИФ при грибной инфекции ограничивалось главным образом пораженной зоной листа (Chou et al., 2000) и коррелировало с меньшим количеством мРНК, кодирующих малую субъединицу РБФК/о. Экспрессия cab генов, кодирующих белки хлорофилл-белкового комплекса, при патогенезе тоже ингибировалась. Растворимые углеводы накапливались в пораженных участках листа, а содержание крахмала, напротив, снижалось. Обратная тенденция наблюдалась в непораженных зонах инфицированного листа.
Каротиноиды в меньшей степени подвержены разрушающему действию инфекции, чем хлорофилл. При заболевании может изменяться соотношение окисленных и восстановленных форм каротиноидов. Так, на 2–6-й дни после заражения ячменя мучнистой росой содержание виолаксантина увеличивалось на 20%, а затем снижалось, и к 9-му дню составляло 60% от здоровых растений. Содержание лютеина и зеаксантина начинало падать сразу после заражения, и через 7 дней эти каротиноиды не обнаруживались в зараженных тканях. Содержание неоксантина и каротина также резко падало к 7-му дню после заражения.
На содержание желтых пигментов оказывает влияние степень поражения растения. Так, в инкубационный период заболевания сливы вертициллезом содержание виолаксантина и лютеина в листьях увеличивается, а с появлением симптомов болезни — падает.
Снижение содержания в листьях пораженного растения хлорофилла не во всех случаях приводит к соответствующему уменьшению интенсивности фотосинтеза, и наоборот. Так, при инфицировании пшеницы Erysiphe graminis на ранних этапах заражения интенсивность фотосинтеза увеличивается, хотя содержание хлорофилла падает. Вместе с тем на более поздних стадиях болезни интенсивность фотосинтеза уменьшается, и с гораздо большей скоростью, чем происходит распад хлорофилла. При этом снижение интенсивности фотосинтеза листьев не коррелирует с площадью пораженных листьев. Вероятно, частичное разрушение хлорофилла, вызванное влиянием фитопатогенных грибов, не является единственной причиной ослабления фотосинтеза. Расчет интенсивности фотосинтеза на единицу хлорофилла свидетельствует о том, что в инфицированных тканях этот показатель также снижается.
Патогены вызывают нарушение световых и темновых реакций фотосинтеза, что, в частности, отмечено при заражении листьев сахарной свеклы вирусом желтухи (рис. 18). В хлоропластах китайской капусты, пораженной вирусом желтой мозаики репы, при локальном проявлении инфекции скорость реакции Хилла и интенсивность циклического и нециклического фотофосфорилирования увеличивались, а при системной инфекции — подавлялись. Вирус табачной мозаики также вызывает подавление реакции Хилла и фотосинтетического фосфорилирования в хлоропластах неустойчивого вида и сорта табака и активирование этих процессов у устойчивых форм. В то же время вирус гравировки не оказывал влияния на скорость этих процессов у табака, хотя фиксация СО2 хлоропластами этих растений подавлялась на 40–50%, что указывает на ингибирование темновых реакций фотосинтеза.
Будучи облигатным паразитом, мучнистая роса вызывает подавление активности ферментов хлоропластов, связанных как с транспортом электронов, так и с фиксацией СО2 у восприимчивого сорта ячменя. Нарушение процессов транспорта электронов и фотофосфорилирования наблюдается также в хлоропластах хлопчатника при вертициллезном увядании, причем нарушение процессов фотосинтеза наблюдается уже на ранних этапах заражения, усиливаясь по мере развития болезни. Степень подавления фотосинтеза зависит в большой мере от фазы развития заболевания и интенсивности поражения.
Заражение облигатными паразитами на протяжении скрытого периода и первых фаз заболевания может не сказаться на фотосинтетической активности растения, а в некоторых случаях – даже активировать ее, как, например, у пшеницы. Однако в дальнейшем ИФ и сухая масса снижаются, уменьшаясь на 10–11-й день на 68 и 29% соответственно. Листья фасоли и пшеницы, пораженные в слабой степени, соответственно, Uromyces phaseoli и Puccinia graminis tritici, вначале фиксировали 14CО2 в два раза активнее, чем здоровые листья. После споруляции паразита скорость поглощения СО2 уменьшалась и составляла 73% от контрольных растений. Эти данные хорошо согласуются с особенностями питания облигатных паразитов. Приспособленность последних к питанию только за счет живых клеток находит яркое выражение в том, что истинные паразиты в начале своего развития могут даже производить некоторый стимулирующий эффект, обеспечивая тем самым наиболее благоприятные условия для своего собственного развития. Это обусловлено тем, что продукты их жизнедеятельности в слабой концентрации оказывают стимулирующее действие на жизнедеятельность растительной клетки. Однако это наблюдается обычно лишь на первых фазах развития болезни, а также при слабом поражении.
При заболеваниях, вызванных факультативными паразитами, снижение ИФ растения начинается уже с начала заболевания и прогрессирует по мере развития последнего.
Рассмотрим подробнее особенности действия вирусов, бактерий и грибов на отдельные звенья процесса фотосинтеза.
Вирусная инфекция. На ранних этапах инфицирования вирусы вызывают незначительное снижение ИФ (He et al., 2004; Rowland et al., 2005) и весьма существенное (50–85%), в сравнении со здоровыми растениями, — на более поздних (Sampol et al., 2003; Bertamini et al., 2004; Rowland et al., 2005). Негативный эффект вирусной инфекции особенно сильно проявляется при дефиците азотного питания. Измерения ИФ и флюоресценции хлорофилла показали, что искомое ингибирование фотосинтеза обусловлено практически полностью неустьичной регуляцией ИФ (Baron et al., 2012). Природа неустьичного ингибирования варьируется в зависимости от вида (штамма) вируса, устойчивости растения-хозяина и факторов среды.
Снижение ИФ в результате вирусной инфекции обычно сопровождается хлорозом и структурными изменениями хлоропластов, снижением проводимости мезофилла для СО2, изменениями в скорости световых реакций фотосинтеза, ингибированием активности ферментов фотосинтеза и транспорта ассимилятов (Sajnаni et al., 2007). Рассмотрим подробнее отмеченные нарушения.
Вирусные патогены влияют на число, размер, морфологию и содержимое хлоропластов, причем эти изменения качественно и количественно определяются спецификой патосистемы (вирус + растение-хозяин). Однако общим для всех них является накопление крахмала, происходящее задолго до проявления симптомов вирусного поражения на инфицированных листьях. Листья растений кабачка, пораженные вирусом огуречной мозаики, обнаруживают повышенную ИФ, по сравнению с неинфицированными листьями. Вместе с тем непосредственно накопление крахмала в процессе инфицирования не требуется для успешного его завершения (Handford, Carr, 2007). Однако углеводный метаболизм влияет на развитие симптомов, хотя накопление крахмала может происходить в зараженных листьях и при отсутствии визуальных симптомов. Нарушения при вирусном патогенезе табака могут включать образования крупных крахмальных зерен в набухших и деформированных пластидах, накопление осмиофильных пластоглобул и дезорганизацию ламеллярных структур в хлоропластах. Накопление крахмала коррелирует с изменениями проницаемости хлоропластных мембран и нарушениями донорно-акцепторных отношений (Hull, 2002). Ингибирование развития ламелл зависит от того, на каком этапе формирования листа происходит инфицирование вирусом.
У растений ячменя, инфицированных вирусом полосатой мозаики (рис. 19), хлоропласты разбухают, агрегируются с частью цитоплазмы и содержат цитоплазматические инвагинации. Аналогичные изменения наблюдаются у пекинской капусты, инфицированной вирусом. Образование пластоглобул может быть связано с разрушением тилакоидов в процессе старения (del Rio et al., 1998). На заключительном этапе инфицирования происходят перекисное окисление липидов (ПОЛ) и деградация тилакоидных мембран. Пластоглобулы могут быть вовлечены в реакции клеток на стресс, а не служат просто пассивным запасающим компартментом (Brehelin et al., 2007).
Нарушения мембранной структуры приводят к снижению скорости электронного транспорта в пораженных листьях, особенно на уровне ФСII. Не исключено, что фотосинтетический электронный транспорт ингибируется ген-продуктами вируса. Наряду со снижением содержания хлорофилла тормозилась также скорость фотофосфорилирования и реакции Хилла. Уменьшение скорости транспорта электронов обусловлено прямым ингибированием ФСII, что в инфицированных листьях винограда связано со снижением содержания белка 33 кДа (Bertamini et al., 2004). Одновременно происходит снижение фотохимической эффективности ФСII (Bueno et al., 2004; Wilhelmova et al., 2005). Скорость электронного транспорта через ФСI практически не изменялась, то есть ФСI, как и ССК, оказались более устойчивыми к действию патогена, чем ФСII (Funayama et al., 1997).
Профилирование экспрессии генов в листьях растений табака, инфицированных тремя видами вирусов, показало, что, в соответствии со степенью поражения, репрессия связанных с пластидами генов, главным образом синтеза белков ядерного кодирования, участвующих в транспорте электронов, светособирающем комплексе (ССК) и цикле Кальвина, была практически одинакова для всех трех видов вирусов (Dardick, 2007). В другом опыте на арабидопсисе (Yang et al., 2007) инфицирование вирусом приводило к ингибированию экспрессии генов, связанных с функциями хлоропластов, использованием сульфатов или растяжением клеточной стенки. Диапазон активации или ингибирования экспрессии генов ответа на вирусную инфекцию независимо от функции гена коррелировал с количеством накопленного вируса.
Таким образом, индуцированное вирусом снижение ИФ вызвано прежде всего неустьичным лимитированием разной природы. Оно может быть обусловлено структурными изменениями хлоропластов, ингибированием скорости световых и темновых реакций фотосинтеза, изменением донорно-акцепторных отношений и торможением транспорта ассимилятов (Baron et al., 2012).
Грибная инфекция. В отличие от вирусов, фотосинтез растения-хозяина под влиянием грибного патогена изменяется в более широком диапазоне. Грибы, вызывающие сосудистое увядание, например Fusarium oxysporum, поражают преимущественно ксилемные ткани растения, вызывая снижение гидравлической проводимости, что приводит к сильному увяданию листьев. Снижение ИФ, вызванное этой группой грибов, может составить 30–90%, в сравнении с контрольными растениями, и обусловлено преимущественно уменьшением устьичной проводимости gs. Неустьичное лимитирование фотосинтеза оказывается вторичным и проявляется лишь при сильном и продолжительном патогенезе. Другая группа грибных патогенов (Puccinia, Alternaria, Septoria, Blumeria, Phytophthora, Erysiphe и др.), поражающая главным образом листья, обитает в клетках мезофилла и влияет на фотосинтез растения-хозяина путем как снижения площади листьев, так и ИФ непораженной части листьев на 30–50% (Baron et al., 2012).
Облигатно-биотрофные грибные патогены (ржавчина, мучнистая роса) существенно снижают ИФ растения-хозяина (рис. 2.1), что обусловлено скорее нарушениями в структуре и функциях фотосинтетического аппарата, нежели в поведениях устьиц. Так, устьичное сопротивление rs у листьев ячменя несколько увеличилось при поражении мучнистой росой и снизилось — при инфицировании бурой ржавчиной. При этом наблюдался повышенный хлороз листьев. Однако изменения содержания хлорофилла у них слабо коррелировали с вариациями ИФ. Хотя в отдельных сочетаниях растения с паразитом фотофосфорилирование не подавлялось, в большинстве опытов снижение ИФ при инфицировании искомыми болезнями по меньшей мере частично обусловлено ингибированием нециклического транспорта электронов. Последнее в свою очередь объясняется резким снижением содержания цитохромов в электронно-транспортной цепи (ЭТЦ) фотосинтеза. Одновременно снижались как активность, так и количество РБФК/о (рис. 2.2), что происходило параллельно уменьшению содержания рРНК в хлоропластах. На листьях ячменя, инфицированных мучнистой росой, было также показано снижение содержания мРНК, кодирующих две субъединицы РБФК. В результате уменьшается содержание хлоропластных белков и ИФ.
Что касается некротрофных грибов, листья в результате инфицирования становятся бурыми, некротичными и, с точки зрения фотосинтеза, бесполезными.
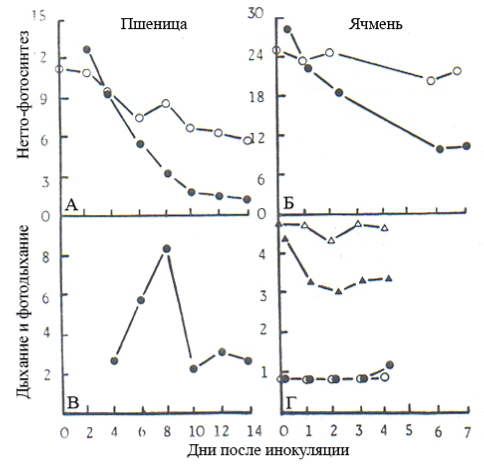
Рис. 2.1. Влияние мучнистой росы на скорость нетто-фотосинтеза
(А, Б: ○ –контроль,● — больные растения), фотодыхания (Г: Δ — контроль, ▲ — больные растения) и темнового дыхания (В и Г: ○ — контроль,
● — больное растение) пшеницы и ячменя. А, Б, Г — в мг СO2 дм–2 ч–1
В — мл O2 мг1 ч–1 (Ayres, 1979)
Снижение нетто-фотосинтеза при патогенезе обусловлено также повышением интенсивности фотодыхания. Так, усиление фотодыхания обнаружено у растений ячменя при поражении бурой ржавчиной.
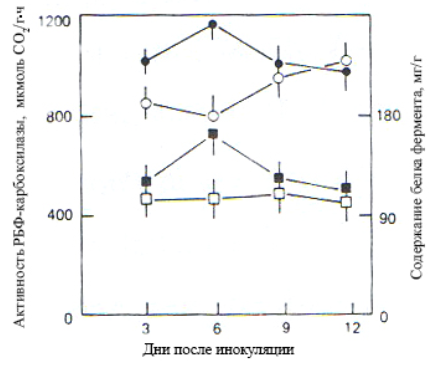
Рис. 2.2. Активность РБФ-карбоксилазы (●) и содержание белка фермента (■) неинфицированного 3-го листа ячменя при двух инфицированных мучнистой росой листьях. Пустые символы — контроль
У ячменя, инфицированного мучнистой росой, напротив, отмечено снижение фотодыхания, что было обусловлено уменьшением активности гликолатоксидазы, глиоксилатредуктазы и рибулезобифосфатоксигеназы (Walters, 1985). Не обнаружено изменения скорости фотодыхания у растений пшеницы при поражении бурой ржавчиной (Mitchell, 1979). Таким образом, в зависимости от сочетания патогена и растения-хозяина, можно ожидать разнонаправленную реакцию фотодыхания и, соответственно, нетто-фотосинтеза на инфицирование (Chou et al., 2000; Swarbrick et al., 2006).
Инфицирование картофеля фитофторой индуцировало снижение параметров максимальной эффективности ФСII, вариабельной или максимальной компоненты флюоресценции хлорофилла, а также увеличение фотохимического тушения хлорофилла (quenching) на ранних этапах патогенеза, что свидетельствовало о нарушениях функционирования ФСII (Koch et al., 1994).
В донорных листьях табака, инфицированного фитофторой, гибель клеток в СВЧ реакции не проявлялась вплоть до полного снижения ИФ (Scharte et al., 2005). При этом отмечено двухфазное снижение ИФ: сначала – за счет закрывания устьиц, а затем — за счет транспорта электронов через ФСI, предотвращающего образование Н2О2 в ФСI (реакция Меллера). В результате строма поддерживается в окисленном состоянии и инактивируются реакции цикла Кальвина. Умеренное фотоингибирование ФСII в зоне инфицирования может быть скорее следствием, чем первичной причиной ограниченного транспорта электронов.
Сравнительно мало экспериментальных данных получено по влиянию активации защитных реакций на фотосинтетически
...